培美曲塞单药维持化疗治疗不同组织学类型晚期非小细胞肺癌的疗效观察
2013-11-13王莉莉蒋玉珑李传红三峡大学第三临床医学院葛洲坝中心医院湖北宜昌443002
王莉莉,蒋玉珑,柯 红,崔 洁,李传红(三峡大学第三临床医学院·葛洲坝中心医院,湖北宜昌 443002)
肺癌的维持治疗指患者完成标准疗程治疗且疾病得到控制后继续接受的治疗,其主要目的是提高肿瘤控制率、优化疗效、延长患者生存期。自2009年始,美国食品药品管理局(FDA)及欧盟委员会先后批准培美曲塞用于进展期非鳞癌的非小细胞肺癌(non-small-cell lung cancer,NSCLC)患者的维持治疗[1-2]。近年来,国内文献已有将培美曲用于维持治疗NSCLC的临床观察报道[3-4],但多数忽略了NSCLC的组织学类型与疗效的相关性。我院自2010年开始对晚期NSCLC标准化疗4周期疾病得到控制者使用培美曲塞维持治疗,并对不同组织学类型者进行疗效比较,结果报告如下。
1 资料与方法
1.1 一般资料
资料来源于2010年11月—2012年10月在葛洲坝中心医院肿瘤科住院治疗的患者,均经病理或细胞学证实为Ⅲb~Ⅳ期NSCLC患者,均接受初期4个周期的双药含铂方案的化疗,达到完全缓解(complete remission,CR)、部分缓解(partial remission,PR)或 稳 定 (stabledisease,SD)。 体 力 状 况(performance statue,PS)评分≤2分(5分法),生存期估计超过3个月,无主要器官的功能障碍,血常规、肝肾功能、凝血功能基本正常,有可测量的或可评估的肿瘤病灶。符合上述标准入组患者共57例,将患者按组织学类型分为非鳞癌组(35例)和鳞癌组(22例),其中非鳞癌组包括腺癌27例、其他类型8例。2组患者一般资料比较,P>0.05,具有可比性,见表1。

表1 2组患者一般资料比较(例)Tab 1 Comparison of general data of patients between two groups(cases)
1.2 方法
2组患者均于第4个周期化疗结束后第21 d开始治疗,给予培美曲塞(江苏豪森药业股份有限公司生产)500 mg/m2,静脉滴注,给药时间>10 min,第1 d给药,21 d为1个周期,直至疾病进展、无法耐受的毒性或合并其他疾病而需停止治疗、患者拒绝继续化疗为止;无疾病进展的患者在达终止观察期时,采用最后一次影像学检查日期作为终点,并做为删失值处理。治疗期间,当出现中性粒细胞计数<0.5×109/L而血小板计数≥50×109/L,培美曲塞剂量减至原剂量的75%,当血小板计数最低值<50×109/L,无论中性粒细胞计数最低值如何,培美曲赛剂量减至原剂量的50%;出现除黏膜炎之外的任何Ⅲ度或IV度非血液学毒性,剂量减至原剂量的75%,出现Ⅲ度或IV度黏膜炎,剂量则减至原剂量的50%。如果患者经历2次剂量调整后,再次出现Ⅲ~IV度血液学或非血液学毒性,应停止本品治疗,如果出现Ⅲ度或IV度神经毒性,应立即停止治疗。
支持治疗:常规行止吐治疗;在使用培美曲塞的前1 d、当日和治疗后1 d口服地塞米松片4 mg,1日2次;首次治疗开始前7 d开始服用叶酸400 μg/d直至维持治疗中止后21 d停止;首次治疗开始前7 d肌内注射维生素B121000 μg,治疗过程中每3个周期重复1次,直至维持治疗中止后。
1.3 观察指标及评价标准
患者治疗期间每周复查血常规及肝、肾功能,每月复查胸部CT评价恶性肿瘤变化,并记录患者一般状况和主观症状的改变。近期疗效评价:治疗2个周期进行疗效评价,并于4周后复核,以CR+PR计算有效率(response rate,RR),CR+PR+SD计算疾病控制率(disease control rates,DCR)。2组患者记录进入维持治疗至疾病进展的时间,作为患者无进展生存期(progress free survival,PFS)。不良反应评价采用世界卫生组织(WHO)化疗药毒副作用评价标准,将毒副作用分为Ⅰ~Ⅳ度,终止治疗时进行统计。
1.4 统计学处理
采用SPSS 16.0软件进行统计学处理。率的比较采用χ2检验,均数比较采用 t检验,PFS采用 Kaplan-Meier法,采用Log Rank进行显著性检验并绘制相应曲线。所有检验水准均为 α=0.05。
2 结果
2.1 临床疗效
57例患者至终止观察期时无失访者,也无因不良反应退出治疗者,非鳞癌组维持治疗2~9个周期,鳞癌组维持治疗1~6个周期。近期临床疗效评价:2组均无CR病例,57例患者总RR为19.3%,总DCR为64.9%;近期疗效比较,鳞癌组与非鳞癌组患者RR及DCR均无显著性差异(P>0.05),见表2;但2组患者PFS中位数比较,有显著性差异(P<0.05),见表3、图1。
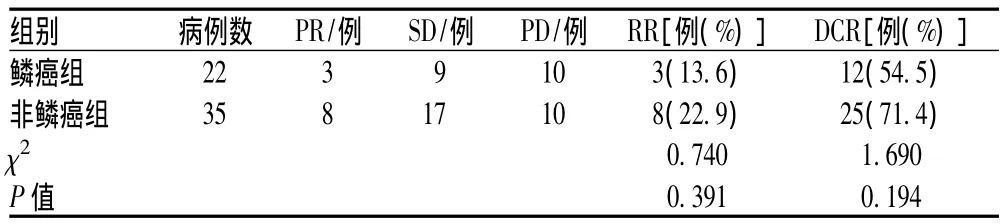
表2 2组患者近期临床疗效比较Tab 2 Comparison of short-term efficacy between two groups
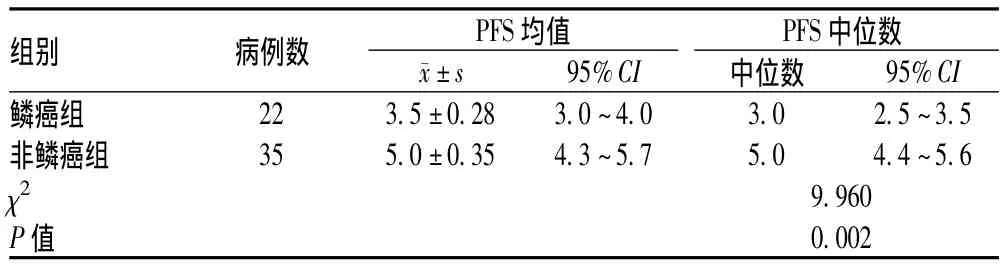
表3 2组患者中位PFS比较(月)Tab 3 Comparison of median PFS between two groups(months)
2.2 不良反应
57例患者中,培美曲塞的主要不良反应为骨髓抑制和胃肠道反应,多数为Ⅰ~Ⅱ度,仅2例患者出现Ⅲ度骨髓抑制。发生不良反应的患者中,骨髓抑制者18例(占31.6%)、恶心呕吐者9例(占15.8%)、腹泻者7例(占12.3%)、肝损害者2例(占3.5%)。不良反应总发生率为47.4%(27/57),其中鳞癌组为36.4%(8/22),非鳞癌组为54.3%(19/35),2组间不良反应发生率比较,差异无统计学意义(χ2=0.64,P=0.423)。
3 讨论
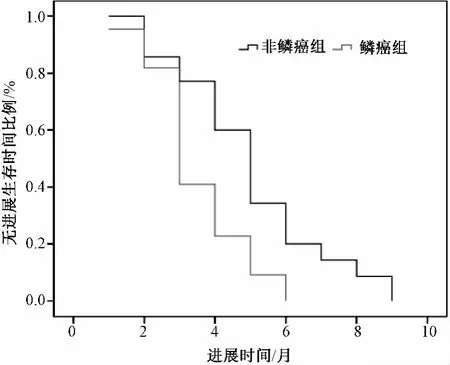
图1 2组患者PFS曲线比较Fig 1 Comparison of progress free survival curve between two groups
晚期NSCLC预后差,1年生存率约为10%,在接受一线标准化疗的患者中有70% ~80%获益,但一般在3个月左右患者病情迅速进展,仅50%~60%的患者有机会接受二线治疗[5]。因此,如何使一线化疗疗效达到SD或PR的患者延缓病情进展和延长带瘤生存时间是国内外肿瘤学界关注的问题。
维持治疗是近几年国外提出的新的肿瘤综合治疗模式,它是在晚期NSCLC一线治疗结束后,对无疾病进展的患者进行维持巩固治疗,目的是提高总生存期和延缓疾病进展。JMEN研究数据显示:培美曲塞在NSCLC维持治疗中显著延长了OS,取得历史性的突破。在一项随机、双盲、Ⅲ期临床试验中[6],对连续应用4个周期含铂化疗后无进展的Ⅲb或Ⅳ期NSCLC患者分别给予培美曲塞或安慰剂联合最佳支持治疗(best supportive care,BSC),结果显示,与BSC比较,培美曲塞组患者的PFS及OS显著延长;在非鳞癌亚组中,采用培美曲塞治疗者的PFS及OS显著延长,而鳞癌亚组患者的PFS及OS并未见延长。该研究证实,培美曲塞作为进展期NSCLC患者的维持治疗具有良好的安全性,其能明显延长患者PFS,尤其是非鳞癌患者获益更多。
目前,国内采用培美曲塞维持治疗NSCLC的临床观察不多,且常忽略了 NSCLC组织学类型[3-4]与疗效的关系。鉴于当前肿瘤的化疗更强调个体化方案,且培美曲塞被批准用于维持治疗的适应证仅限于非鳞癌的NSCLC,因此,我们对经过双药含铂化疗方案4周后未进展的晚期NSCLC患者采用培美曲塞进行维持治疗,并对不同组织学类型者进行了疗效的观察与比较,以期为临床决策维持方案提供参考。
统计结果显示:培美曲塞维持治疗晚期NSCLC时,鳞癌与非鳞癌患者的近期疗效(RR、DCR)相似(P>0.05),但不同组织学类型的病情进展时间有差异,鳞癌患者的PFS均值为3.5个月(95%CI=3.0`4.0),PFS中位数为3个月(95%CI=2.5~3.5),而非鳞癌患者的PFS则长于鳞癌组,其均值为5个月(95%CI=4.3~5.7),中位数为5个月(95%CI=4.4~5.6),2组PFS比较有非常显著的差异(P=0.002)。这说明非鳞癌患者较鳞癌患者对培美曲塞维持化疗更敏感,此结果与国内外文献报道一致[6-9]。此外,肿瘤患者难以接受持续化疗的主要原因常是化疗的累积毒性,培美曲塞具有低毒、易耐受的特点,使其在肿瘤的维持治疗中具有极大的优势。在本项临床观察中,培美曲塞的不良反应发生率与文献报道相似[4,6],且多为Ⅰ ~ Ⅱ度,程度较轻。
综上所述,晚期NSCLC组织学类型对培美曲塞维持治疗的疗效具有显著的影响,培美曲塞在非鳞癌患者的维持治疗中较鳞癌患者有更好的疗效,且不良反应轻微,患者易耐受。因此临床决策晚期NSCLC维持治疗时,在充分考虑患者的基本状况下,应按组织学分型采取个体化治疗方案。
[1]马培奇.美FDA批准培美曲塞二钠用作进行性非小细胞肺癌维持疗法[J].上海医药,2009,30(8):375.
[2]马培奇.欧盟批准培美曲塞二钠用于进展期非鳞癌非小细胞肺癌继续维持治疗[J].上海医药,2012,33(3):50.
[3]毋永娟,崔荣,华云旗,等.培美曲塞与厄洛替尼维持治疗晚期非小细胞肺癌的临床研究[J].中国全科医学,2011,14(9):966-968.
[4]陈俊,熊建萍,应学明,等.国产培美曲塞维持治疗晚期非小细胞肺癌的临床观察[J].江西医学院学报,2009,49(12):73-76.
[5]Stinchcombe TE,Socinski MA.Treatment paradigms for advanced stage non-small cell lung cancer in the era of multiple lines of therapy[J].J Thorac Oncol,2009,4(2):243-250.
[6]Ciuleanu T,Brodowicz T,Zielinski C,et al.Maintenance pemetrexed plus best supportive care versus placebo plus best supportive care for non-small-cell lung cancer:a randomised,double-blind,phase 3 study[J].Lancet,2009,374(9699):1432-1440.
[7]Scagliotti G,Brodowicz T,Shepherd FA,et al.Treatmentby-histology interaction analyses in three phaseⅢtrials show superiority of pemetrexed in nonsquamous non-small cell lung cancer[J].J Thorac Oncol,2011,6(1):64-70.
[8]Mubarak N,Gaafar R,Shehata S,et al.A randomized,phase 2 study comparing pemetrexed plus best supportive care versus best supportive care as maintenance therapy after first-line treatment with pemetrexed and cisplatin for advanced,non-squamous, non-small cell lung cancer[J].BMC Cancer,2012,12(9):423-433.
[9]庄莉,王清泉.影响非小细胞肺癌维持化疗疗效的相关因素探讨[J].昆明医学院学报,2009,30(6):76-79.
