压片机隔离操作器(Isolator)设计研发的思考
2013-10-31伍善根
伍善根
(上海天祥•健台制药机械有限公司,上海 200040)
1 前言
从2011年3月1日开始,《药品生产质量规范(2010年修订)》(GMP)正式实施,新版GMP附录第一部分对无菌生产要求较之以往的要求有了较大幅度的提高。表明政府对无菌制剂的质量管理愈加严格,这就要求相关药品生产厂商对生产环境必须施行更加严格的标准。在硬件设施和软件管理方面进行改造。在新版GMP附录第一部分第四章中,特别指明介绍了隔离操作技术[1]。
高污染风险的操作应在隔离操作器中完成,同时,随着21世纪生物医药、微电子等技术的快速发展,对洁净技术的要求不断提高,传统的洁净室(局部屏蔽)已越来越不能满足使用者的要求,于是无菌隔离器的应运变得越加普及。
目前许多药厂的从业人员,以及药机设备厂的技术人员对有关隔离操作器(Isolator)的知识了解甚少,特别是涉及到压片机的隔离操作器技术。近期笔者有幸参加了2011年在德国杜塞多夫市举行的第19届Interpark展览会和2012年在德国法兰克福举行的第30届Achema展览会,在二个世界制药及流程工业顶级的展览会上目睹了不少制药设备隔离操作器并与参展的外商进行了充分的交流获得一些体会,现择文于此,作一交流。隔离操作器是一种高技术含量的设备,本身亦是在发展过程之中,由于笔者的知识面有限,不当之处,希于谅解。
2 隔离操作器的特点
无菌隔离技术是一种用物理屏障的手段将受控空间与外部环境相互隔绝的技术,而无菌隔离器便是采用无菌隔离技术,突破传统的洁净技术,为用户带来一个高度洁净、持续有效的操作空间,它能最大限度降低微生物、各种微粒和热原的污染,实现无菌制剂生产全过程的无菌控制。
2.1 隔离器技术的应用主要有三方面的考虑
(1)保护无菌药品在生产过程中不受交叉污染或外部环境的影响;
(2)保护操作人员远离高活性、高致敏性和毒性物质的侵害(例如:青霉素类、细胞毒素类、激素类、抗肿瘤药及放射性药物等药品);
(3)保护环境免受高活性、高致敏性和毒性物质在无控制条件下的传播。
按规定关键的工艺核心区即内部一A级IS05标准,隔离操作器周围的环境应基于美国C级/IS08、欧盟C或D级/IS08(动态),新版GMP规定,压片机的外部生产环境应在D级。一个成功的隔离操作器实质是一种人造环境的设计,也是一个小的封闭的操作者不进入的空间。操作者只有停产才能打开设备,平常操作者只能通过手套箱进行操作,密闭的工艺加料,转移通道的密闭设计,去除生物污染,隔离操作器的内部表面消毒,操作者与无菌工艺核心的相互隔离,保证职业卫生标准(有毒药物可暴露浓度),低于0.1μg/m³的水平。
2.2 隔离操作器具有下列优点
①无菌室所需的空间小;②洁净区的概念更清楚;③背景环境简单只需D级或C级;④更衣程序简单;⑤更低的运行成本(空调、无菌服)节省约40%;⑥更好地对操作人员进行保护;⑦更好地保护产品的安全;⑧减少微生物的检测;⑨人员简化易于维护;⑩减少投资费用约20%。
3 压片机隔离操作器的基本要求
3.1 隔离操作器设计研究的课题及目的[2]
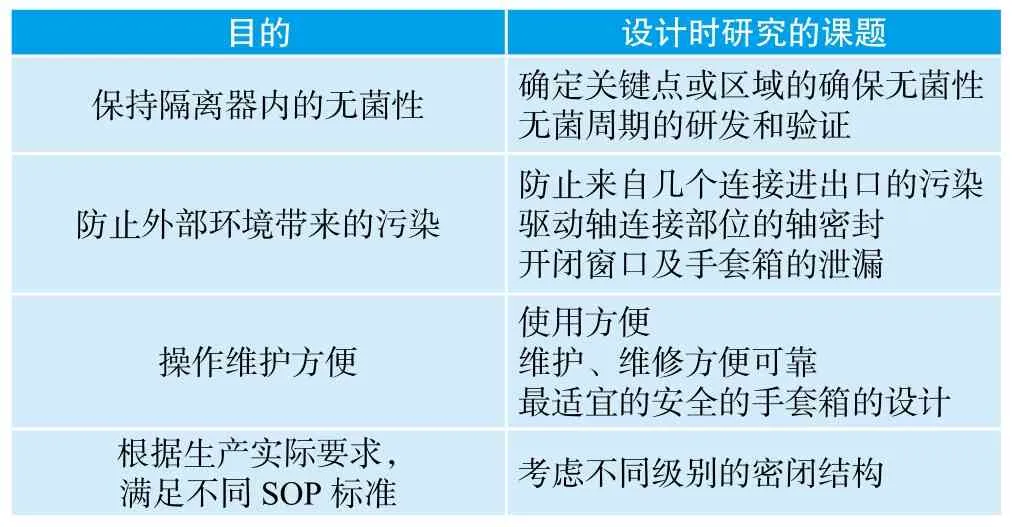
目的 设计时研究的课题保持隔离器内的无菌性 确定关键点或区域的确保无菌性无菌周期的研发和验证防止外部环境带来的污染防止来自几个连接进出口的污染驱动轴连接部位的轴密封开闭窗口及手套箱的泄漏使用方便维护、维修方便可靠最适宜的安全的手套箱的设计根据生产实际要求,满足不同SOP标准 考虑不同级别的密闭结构操作维护方便
3.2 压片机隔离操作器的要求
压片机与其他制剂设备上所使用的隔离操作器有所不同,应根据各个企业不同的SOP标准来准确地计算出生产过程中可能的药物泄漏量,确定所需要使用的密封等级,最终设计出满足这种密封等级的隔离操作器。
压片时药物粉末泄漏的方式有二种。一种是间歇式的泄漏,例如:加料装置的断开及重新连接,附属设备如:筛片机、金检机的断开、清洗以及重新连接;第二种泄漏方式是连续式的泄漏,如:压片生产过程中的泄漏[3]。
各个药厂都会制定出压片生产车间的SOP,其中,规定符合安全生产的最低泄漏量,那么,我们就可以分别计算出压片生产中间隙的泄漏和连续的泄漏,从而选出满足生产要求又投资最小化的不同密封等级的隔离操作器的压片机。
同时,对压片室内粉尘的控制亦必须控制在一定的范围内,否则,压片室内粉尘飞扬,操作者根本无法看见压片室内运转的情况。
3.3 压片机隔离操作器的重要参数
①压差(过滤器前后、隔离器内外);②尘埃粒子;③气流速度(工作面);④温度;⑤湿度;⑥泄漏率(手套箱、隔离器);⑦清洗(WIP、CIP);⑧灭菌(VHP)。
3.4 压片机隔离操作器的设计要点
(1)封闭的系统拥有自身清洁与过滤设备实现一个整体解决方案。
(2)压片机隔离操作器一般均带有大型视窗的端口手套,整个内部非常容易看到并且可以达到。
(3)设计时应充分考虑无死角、大弯道、内部零件的表面光洁、无焊缝、所有管道连接无槽或裂缝,不至于药物粉末积压。
(4)设计上必须处理好与外部环境的几个接口:①快速输送端口,方便工具及模具的进出,不致于在工具或模具进出时造成污染;②物料进口;③片剂出口,例如:采用平铺管热封及切割原理进行密封切断(图1),保证没有污染,或将片剂传递到下一个隔离操作器或容器;④处理好吸尘出口含物料细粉废弃的排放,或经过滤后排放。
(5)设计与建立压片室内的气流模型,保证与外部环境的完全隔离。确认压差,一般情况下隔离器与周围环境的压差可控制在20Pa~50Pa。

图1 平铺管热封及切割
(6)经清洗后的带隔离操作器的压片机有些情况下还需经过过氧化氢(H2O2)的灭菌(以前常用擦拭、喷雾或蒸气技术)。H2O2灭菌的优点是效率高、时间快、无有毒残留物等一系列的优点。经过除湿、调整、灭菌、吹风等四个阶段完成H2O2的灭菌工艺流程。带隔离操作器压片机的设计人员必须注意到这些设备中零部件选择的材料,能够承受H2O2的灭菌。
(7)根据用户的物料和生产工艺,压片机隔离操作器的基本设计理念,要对各个要素进行平衡和控制,以达到无菌的目的。同时,根据用户的要求实现不同级别控制,采用一系列的软件来关联各种基本控制。
(8)设计时还须考虑人体工程学。
设计者应考虑到操作工头部、眼睛的高度、手臂的长度,通过手套箱可以接触到压片室的各个区域,并完成各种压片机的操作和调整。手套箱的高度、窗口位置和大小彼此相配,以及手套箱本身设计的符合性。
4 设计压片机隔离操作器应该遵循的标准和规范
(1)FDA 2004——无菌药品生产工艺指南;
(2)Eu GMP欧盟医药产品指南,附录1;
(3)PIC/S 014-2隔离器在无菌过程和无菌测试的应用;
(4)ISO14644-7洁净室和相关受控环境——隔离装置;
(5)ISO 10648-1隔离器外罩部分设计原则;
(6)ISO 10648-2 隔离器外罩部分泄漏密闭性和相关检查方法;
(7)AGS-G001-2007美国手套箱协会指南;
(8)Contain ment systems design guide隔离器系统的设计指南;
(9)ISO13408-6健康产品无菌工艺——隔离系统。
5 压片机隔离操作器的测试和在线检测
5.1 压片机隔离操作器在试用之前还需作下列项目的测试
(1)过滤器完整性的测试;
(2)洁净度的测试;
(3)风速测试;
(4)压差测试;
(5)气体流向测试;
(6)噪声测试;
(7)照度测试;
(8)微生物的测试;
(9)手套箱泄漏的测试。
5.2 压片机隔离操作器运行过程中的在线检测
(1)洁净度多点在线检测;
(2)风速的在线检测;
(3)微生物的在线检测;
(4)压力差的在线检测;
(5)温度在线检测;
(6)湿度在线检测;
(7)压片工艺在线检测。
6 压片机隔离操作器技术的验证要点
美国FDA和欧盟GMP医药产品指南,附录1中第14条阐述了采用隔离器技术能最大限度的降低操作人员的影响,并大大降低无菌生产中环境对产品微生物污染的风险。高污染风险的操作宜在隔离器中完成,隔离器及其所处环境的设计,应能保证相应区域空气的质量达到认定的标准,物品进出隔离器应特别注意防止污染。无菌操作的隔离器所处环境的级别至少应为D级。第15条,隔离器只有通过适当的验证方可投入使用,验证时应当考虑隔离器的所有关键因素,如:隔离器系统内部和外部所处环境的空气质量,隔离器的消毒、传送、操作以及隔离系统的完整性。第16条,隔离器用的手套应进行常规检测,包括经常进行必要的验证。
6.1 验证的要素
验证的要素包括:高效过滤器的完整性测试、风速检测尘埃粒子计数、噪声、振动、检漏以及无菌隔离器的人体生物验证。
6.2 检测和验证的仪器
粒子计数器、悬浮微粒照度计和信号发生器、相对湿度、温度、风速测定仪、风量仪、压差计、过氧化氢发生器、气体检测仪和风速仪等。
6.3 压片机隔离操作器设计生产者应该提供的文件
(1)设计确认DQ,安装确认IQ,运行确认OQ;
(2)FAT(工厂检测验收);
(3)材质证明;
(4)元器件清单;
(5)备件清单;
(6)封闭泄漏测试校验证明;
(7)布局图、电控图、流程图、管道图;
(8)生产设备的校验证明;
(9)清洁验证的报告;
(10)客户现场验收测试报告;
(11)人体工程学试验报告。
7 国外压片机隔离操作器的发展现状
隔离器技术的开发与成功仅20多年,目前,在医药、电子、核工业等部门中获得广泛应用,亦是医药装备业的重大进步。
到2010年根据ISPE(国际制药工程协会)的统计[4],全世界范围内共有427套隔离器用于制药工业,其中,亚洲仅有64套,其中,以冻干粉针制品分装和液体产品无菌灌装为多,片剂较少。
世界上先进的压片机制造商例如:Fette公司、Korsch公司、SMI等都有带隔离操作器的压片机产品。例如:Fette公司是世界上最著名的压片机生产厂商,较早的开展了压片机隔离技术的研究,并已经在多年的生产实践中证明其生产制造的隔离操作器,职业暴露水平低于0.1μg /m³。
目前Fette公司已经可以提供三种不同类型的隔离器技术的产品:
(1)带筛片机和金属检测一体的隔离操作器;(2)带过程控制技术的隔离操作器;
(3)带筛片机、金属检测以及过程控制的隔离操作器(图2)。
Fette公司还可以将隔离操作器与WIP压片机相结合,则该设备可以实现完全的在位清洗或全自动无人操作。

图2 Fette公司带隔离操作器的压片机
Korsch公司生产的各种型号的带隔离器密闭型的压片机[6](图3)这些压片机具有在线清洗并可清洁验证,满足不同等级的密闭型的结构(有毒药粉可暴露浓度范围OEL>0.1μg/m³可达OEB5级),人体工程学的操作手套,负压控制下更换过滤器,RTP手套可快速传递冲头、工具或其他零件。
还有一种压片机的密闭技术,这是GEA Courtoy公司的专利,该公司将转台、冲模等与药品可能接触的零部件全部经压缩后装入一module模块(图4)。第一,这个模块是可换的,整体拿出后清洗(离线清洗);第二,这个模块内包含着所有与药粉接触的零部件包括标准件;第三,这个模块是密闭的,密闭等级可由用户根据自身的需要进行选择,最高等级的密封泄漏可以1μg/m³以下。并且GEA Courtoy公司将该模块与出片系统至筛片、金属检测等辅机全部组合在一起,形成一个完整的系统密闭。在ECM与外部之间仅存在4个接口:①药粉入口、②空气入口、③片子出口、④吸尘口。

图3 Korsch公司各种带隔离操作器的压片机

图4 Courtoy公司带密闭技术的模块
8 压片机隔离操作器在中国的展望
总的来讲压片机隔离操作器的设计应充分考虑压片产品对人体的伤害程度,以及隔离操作器的密闭等级,另外,应考虑到所设计的隔离操作器的工厂室内空间的要求,维护的方便,以及除尘、金属检测、筛片等辅助设备的整体考虑。这些参数亦会影响整个项目的成本和施工的进度,也应尽早在设计过程中加以确定。
当前我国压片机隔离器技术的发展还处于萌芽阶段,目前只有很少的药厂采用带隔离器技术的压片机,而压片机国内的制造厂商对压片机隔离器技术的研发还处于初级阶段,尚未设计生产出产品。在净化、泄漏测试、人机工程和进入的灵活性研制时会遇到不少困难。
从欧美等制药强国的经验来看,传统开放的无菌室已经不适应越来越高的无菌需求,政府时有毒有害药物生产的控制日益提高,对操作人员的保护,EHS环境、职业健康安全管理体系,势必会推动压片机隔离器技术的大力发展,新版GMP的实施也将大大促进和加快国内压片机隔离器技术的发展。
[1] 药品生产质量管理规范(2010)(年修订)[S].北京:中华人民共和国卫生部.
[2] www.Pharmpro.com/Articles/2009/0.1.
[3] 韩前健,密闭技术在现代固体制剂生产中的定义和探讨[J].机电信息,2012(8):13-18.
[4] Assessing the particulate containment performance pharmaceutical Equipment(ISPE,2010).
