两个厂家的烟酸片的溶出度比较
2013-10-20江苏省泰州市食品药品检验所225300黄勇钱忠义
江苏省泰州市食品药品检验所(225300)黄勇 钱忠义
固体制剂口服给药后,药物的吸收取决于药物在制剂中的释放、生理条件下药物的溶出度或溶解作用及药物在胃肠道的生物膜通透性。上述步骤中前两步具有决定性作用,因此药物的体外溶出度可以预测体内行为。因药物释放度是评价药物制剂质量的内在指标,是制剂质量控制的重要手段,在缓、控和迟释制剂的前期开发中有着非常重要的意义[1]。
人体对药物的吸收部位主要是消化道。体内环境正常者,胃肠道内存在有正常量和正常pH的胃酸和肠液;体内环境非正常或体质虚弱者,胃酸和肠液的量及pH会有差异。人体消化器官内的液体pH范围为:胃1.2~7.6,十二指肠3.1~6.7,小肠5.2~6.0。50 岁以上的人群,胃酸和肠液均有变化。因此,笔者使用4种pH值的溶出介质模拟人体的不同部位的体液:0.1mol/L盐酸液,pH4乙酸盐缓冲液,pH6.8磷酸盐缓冲液,水(《中国药典》2010年版二部品种项下的溶出介质)900ml。采用转篮法,转速100r/min。
1 仪器与试药
UV分光光度计(日本岛津),Mettler AG-135电子天平(梅特勒-托利多)。烟酸对照品(中国药品生物制品检定所,批号:100434-201102),试剂均为分析纯。
2 测定法
2.1 溶出量的测定方法 采用《中国药典》2010年版二部烟酸片溶出度项下的方法,采用紫外分光光度法,在262nm波长处测定吸光度。
2.2 对照品溶液 精密称取烟酸对照品适量,分别加溶出介质溶解并稀释成浓度为11μg/L的对照品溶液。
2.3 供试品溶液 上海信谊药厂有限公司3个批次的样品(批号:100101、110701、120501)和南京白敬宇制药有限责任公司1个批号供试品(批号:120301),照溶出度测定法(《中国药典》2010年版二部附录X C第一法),分别以0.1mol/L盐酸液、pH4乙酸盐缓冲液、pH6.8磷酸盐缓冲液和水900ml为溶出介质,转速100r/min,依法操作,分别于5,10,15,25,30min时取溶液5ml(及时补充相应体积溶出介质),滤过,取续滤液5ml,用溶出介质稀释成11μg/L的溶液,即得供试品溶液。
2.4 测定 照《中国药典》2010年版二部附录ⅣA测定[2],在262nm波长处有最大吸收,计算溶出量。取上海信谊药厂有限公司3个批号的溶出度的平均值和南京白敬宇制药有限责任公司1个批号的样品绘制溶出曲线,见附图1~4。
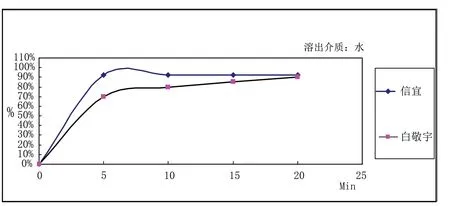
附图1 两个厂家烟酸片在水中的溶出曲线
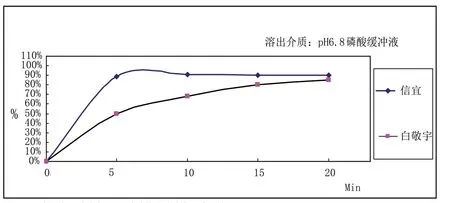
附图2 两个厂家烟酸片在pH6.8磷酸盐缓冲液中的溶出曲线
由附图1、附图2、附图3和附图4可见,两个厂家的样品的溶出曲线有明显的差异。上海信谊药厂有限公司的烟酸片在4种介质中的溶出曲线大体上一致,溶出都比较快,5min时,4种介质中烟酸的溶出量均能达到80%以上;南京白敬宇的烟酸片在4种介质中溶出曲线有差异,且溶出相对缓慢,尤其是在0.1mol/L盐酸液中溶出速率最低,15min时,4种介质中烟酸的溶出量也达到80%。这说明上海信宜的烟酸片和南京白敬宇的处方工艺有较大差异[3]。纯化水不是合适的溶出介质。不同地区的水的硬度和pH值均有差异,且水没有缓冲能力,即不适合模拟人体环境,也不适合在不同地区的实验室重现试验结果。0.1mol/L盐酸液对两个厂家的烟酸片有较强的分辨力,且能充分模拟胃酸。USP34也采用0.1mol/L盐酸液作为烟酸片的溶出介质。因此,建议将标准的溶出介质修改为0.1mol/L盐酸液。
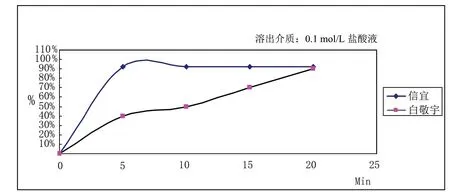
附图3 两个厂家烟酸片在0.1mol/L盐酸液中的溶出曲线
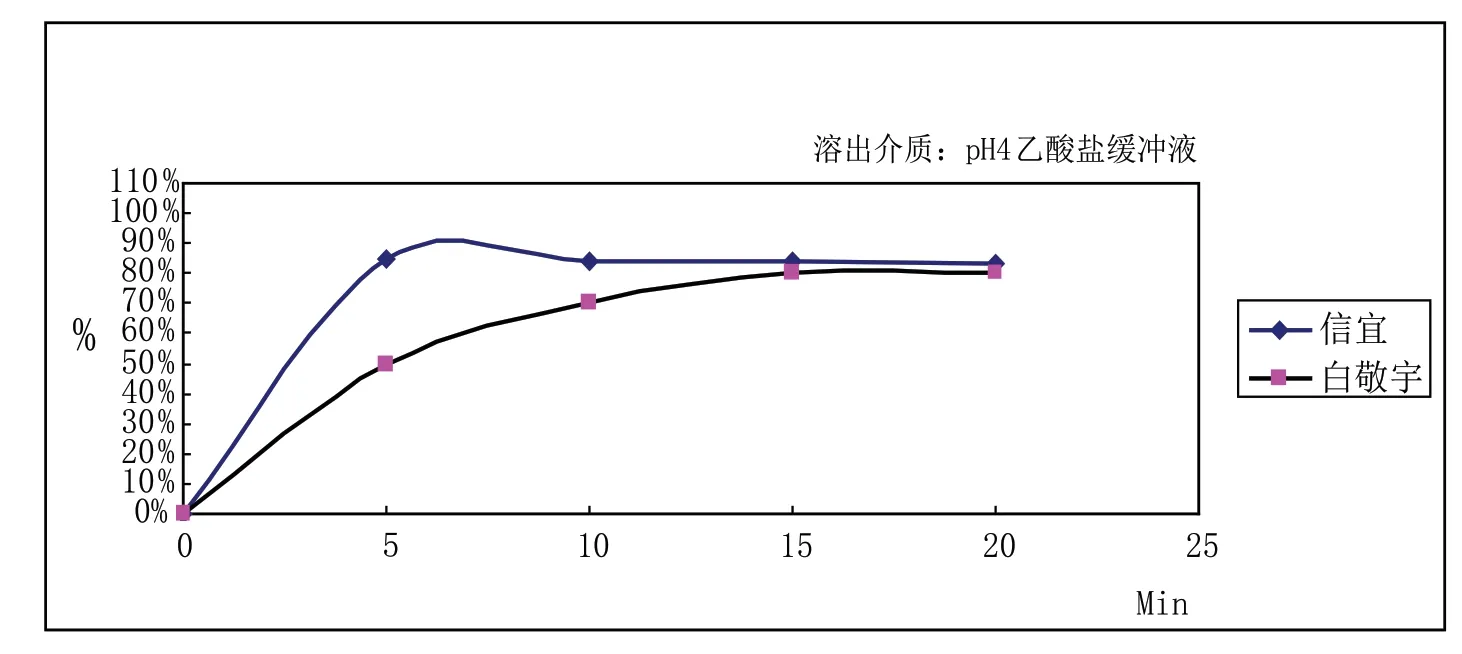
附图4 两个厂家烟酸片在pH4乙酸盐缓冲液中的溶出曲线
