HPLC测定心悦胶囊中人参皂苷Rg1、Re及Rb3的含量
2013-09-26杨颖王宏伟于文静
杨颖,王宏伟,于文静
(吉林省食品药品检验所,吉林 长春 130033)
HPLC测定心悦胶囊中人参皂苷Rg1、Re及Rb3的含量
杨颖*,王宏伟,于文静
(吉林省食品药品检验所,吉林 长春 130033)
目的:研究心悦胶囊中人参皂苷Re、人参皂苷Rg1及人参皂苷Rb3的定量方法。方法:采用高效液相色谱法。色谱柱:Lun C18(250 mm×4.6 mm,5 μm);流动相:乙腈-水梯度洗脱;检测波长为203 nm。结果:线性范围为人参皂苷Rg1在0.098 9~1.978 0μg(r=0.999 1,n=5),人参皂苷Re在0.312 0~5.38 μg(r=0.999 2,n=5),人参皂苷Rb3在0.448~8.96 μg(r=0.999 1,n=5)。平均加样回收率人参皂苷Rg1为97.1%,RSD=2.46%(n=6),人参皂苷Re为97.5%,RSD=1.89%(n=6),人参皂苷Rb3为100.0%,RSD=2.28%(n=6)。结论:本法简便、灵敏、准确,可用于心悦胶囊的质量控制。
人参皂苷Re;人参皂苷Rg1;人参皂苷Rb3;心悦胶囊;高效液相色谱
心悦胶囊是由西洋参茎叶总皂苷制成的单方制剂,具有益气养心,和血之功效。用于冠心病心绞痛属于气阴两虚证者。原标准仅建立了以人参皂苷Rb3为对照,采用高效液相色谱法进行含量测定,不能全面有效地控制该品种的内在质量,故被列为国家中药制剂质量标准提高行动计划品种。西洋参PanaxquinquefoliumL.是五加科人参属植物,为我国传统的名贵药材之一。西洋参茎叶属于其地上部位,现代研究证明,西洋参地上部位含有以人参皂苷为主的多种活性成分[1-2],西洋参茎叶总皂苷即为西洋参茎叶提取物。作者在参考相关文献[3-6]的基础上,建立了以人参皂苷Rg1、人参皂苷Re及人参皂苷Rb3为对照品,采用高效液相色谱法测定本制剂中西洋参茎叶总皂苷的含量,旨在全面、有效控制该产品的内在质量。
1 仪器与试药
Agilent 1100高效液相色谱仪。人参皂苷Rg1对照品(批号:110703-201027)、人参皂苷Re对照品(批号:110754-200822)、人参皂苷Rb3对照品(批号:111686-200501),中国食品药品检定研究院,供含量测定用;乙腈为色谱纯,水为纯化水,其他试剂均为分析纯。心悦胶囊(吉林省集安益盛药业股份有限公司,规格:0.3 g/粒,批号:100624,100717,100718,100819,100820,090510)。
2 方法与结果
2.1 色谱条件
色谱柱:Lun C18(250 mm×4.6 mm,5 μm);以乙腈为流动相A,水为流动相B,按表1进行梯度洗脱;柱温35 ℃,检测波长为203 nm,进样量5 μL,理论板数按人参皂苷Re计算应不低于6 000。

表1 流动相梯度洗脱表
2.2 对照品溶液的制备
取人参皂苷Rg1对照品、人参皂苷Re对照品及人参皂苷Rb3对照品适量,精密称定,加甲醇制成每1 mL含人参皂苷Rg1对照品0.1 mg、人参皂苷Re对照品及人参皂苷Rb3对照品各0.4 mg的混合溶液,摇匀,即得。
2.3 供试品溶液的制备
取装量差异项下的本品内容物,研细,取约1.5 g,精密称定,置100 mL量瓶中,加甲醇适量使溶解并稀释至刻度,摇匀,滤过,取续滤液,即得。
2.4 测定方法
分别精密吸取对照品溶液与供试品溶液各10 μL,注入液相色谱仪,测定,即得。HPLC图见图1。
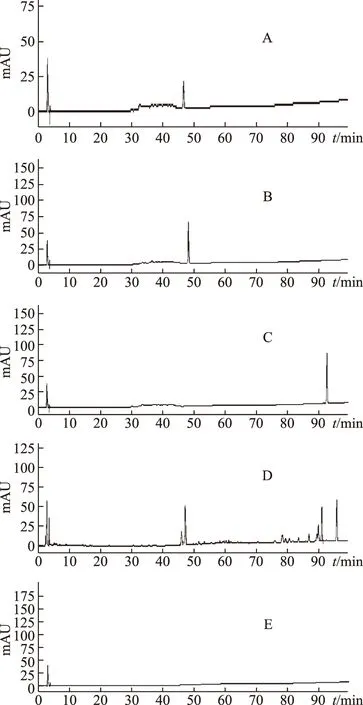
A.人参皂苷Rg1对照品 B.人参皂苷Re对照品 C.人参皂苷Rb3对照品 D.供试品 E.阴性对照品图1 心悦胶囊及对照品HPLC图
2.5 线性关系考察
分别精密吸取人参皂苷Rg1对照品(批号:110703-201027)浓度为0.102 7 mg·mL-1、人参皂苷Re对照品(批号:110754-200822)浓度为0.351 3 mg·mL-1、人参皂苷Rb3对照品(批号:111686-200501)浓度为0.448 mg·mL-1的溶液,分别注入液相色谱仪,按拟定色谱条件测定,以对照品的进样量(μg)为横坐标,色谱峰面积为纵坐标绘制标准曲线。人参皂苷Rg1回归方程为:Y=319.51X+14.726,r=0.999 1,结果表明,人参皂苷Rg1在0.098 9~1.978 0 μg线性关系良好;人参皂苷Re回归方程为Y=308.56X+27.87,r=0.999 2,结果表明,人参皂苷Re在0.312 0~5.38 μg线性关系良好;人参皂苷Rb3回归方程为Y=249.41X+34.559,r=0.999 1,结果表明,人参皂苷Rb3在0.448~8.96 μg线性关系良好。
2.6 精密度试验
精密吸取上述供试品溶液10 μL,注入液相色谱仪,重复6次,测定其色谱峰面积,人参皂苷Rg1平均值为250.00,RSD=2.51%;人参皂苷Re平均值为788.99,RSD=0.95%;人参皂苷Rb3平均值为1 101.81,RSD=1.16%。结果表明所用仪器具良好的精密性。
2.7重复性试验
取本品(批号:100624),倾出内容物,混匀,按供试品溶液制备方法制备,独立配制6份供试品溶液进行测定,计算含量,人参皂苷Rg1的RSD=1.01%;人参皂苷Re的RSD=0.53%;人参皂苷Rb3的RSD=0.78%。结果表明本法重现性较好,精密度较高。
2.8 回收率试验
精密量取同法测定已知含量的供试品(批号:100624)6份,每份0.75 g,分别精密量取人参皂苷Rg1(批号:110703-201027)浓度为0.844 mg·mL-1的对照品溶液5 mL,加入样品中,按拟订标准的方法提取、测定,计算回收率,结果见表2。
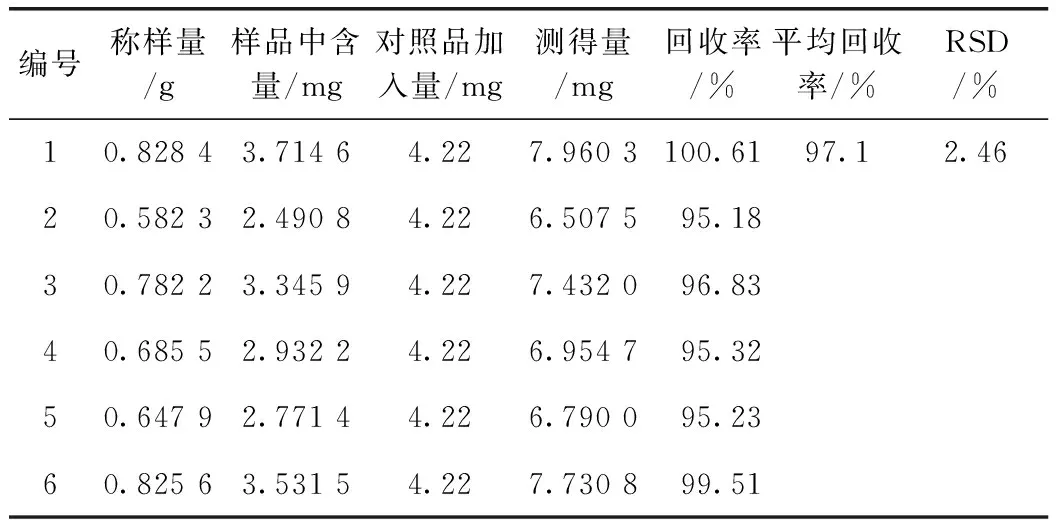
表2 人参皂苷Rg1回收率试验
注:人参皂苷Rg1对照品加入量均为4.22 mg
精密量取同法测定已知含量的供试品(批号:100624)6份,每份0.75 g,分别精密量取人参皂苷Re对照品(批号:110754-200822)浓度为1.242 mg·mL-1的对照品溶液10 mL,加入样品中,按拟订标准的方法提取、测定,计算回收率,结果见表3。
精密量取同法测定已知含量的供试品(批号:100624)6份,每份0.75 g,分别精密量取、人参皂苷Rb3对照品(批号:111686-200501)浓度为21.78 mg·mL-1的对照品溶液10 mL,加入样品中,按拟订标准的方法提取、测定,计算回收率,结果见表4。
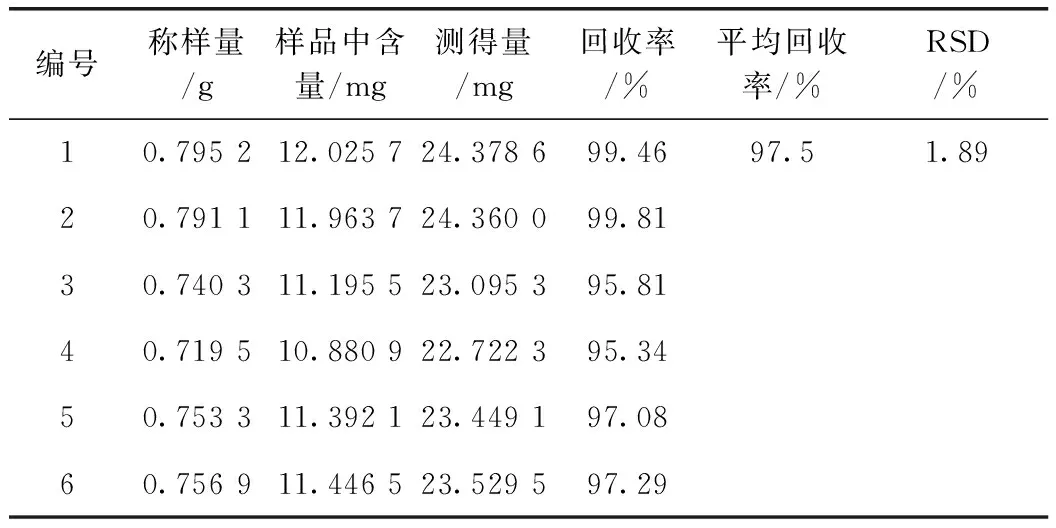
表3 人参皂苷Re回收率试验
注:人参皂苷Re对照品加入量均为12.42 mg
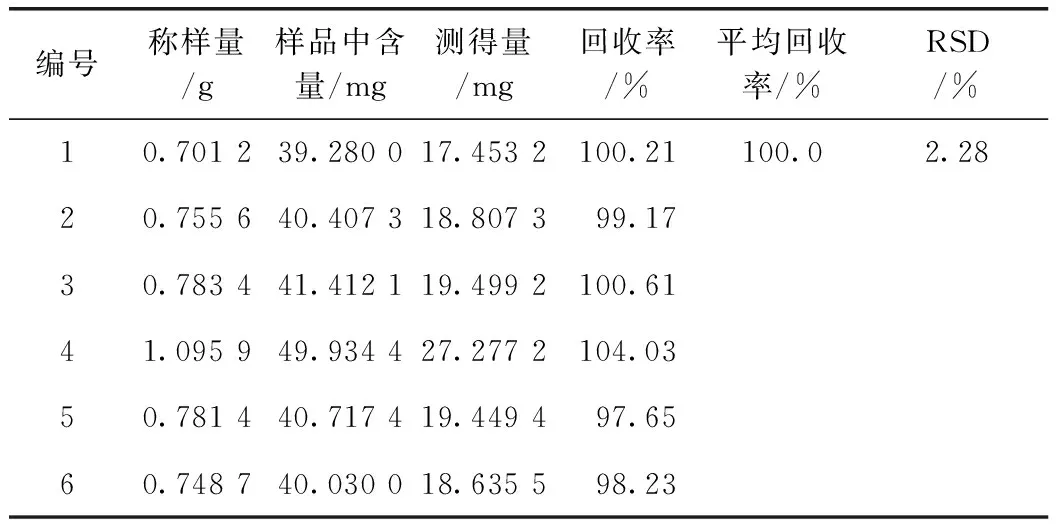
表4 人参皂苷Rb3回收率试验
注:人参皂苷Rb3对照品加入量均为21.78 mg
2.9 稳定性试验
对同一份供试品溶液(批号:100624),按正文色谱条件,每隔8 h进样1次,每次进样10 μL,记录峰面积,计算人参皂苷Rg1的RSD=1.54%,人参皂苷Re的RSD=1.50%,人参皂苷Rb3的RSD=0.56%,结果表明48 h内供试品溶液中人参皂苷Rg1、人参皂苷Re及人参皂苷Rb3含量基本稳定。
2.10 空白试验
为进一步考察实验设计的合理性,取不含西洋参茎叶总皂苷的阴性对照样品适量,按正文含量测定方法进行测定。结果阴性样品色谱中在与人参皂苷Rg1、人参皂苷Re及人参皂苷Rb3峰相应的保留时间位置处无干扰峰检出(见图1),从而证明本法是合理可行的。
2.11 样品含量测定
照上述方法测定6批样品,结果见表4。
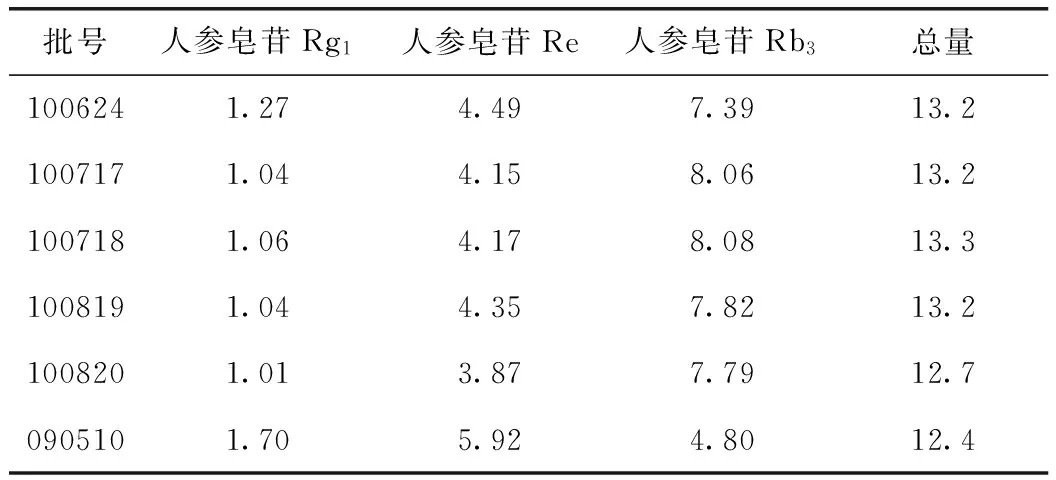
表4 6批心悦胶囊样品中人参皂苷Rg1、Re、Rb3含量测定 mg/粒
根据6批样品含量测定结果,并考虑到实际生产中的波动,含量限度暂定本品每粒含西洋参茎叶总皂苷以人参皂苷Rg1、人参皂苷Re及人参皂苷Rb3总量计,不得少于5.5 mg。
3 讨论
3.1 测定波长的选择
取人参皂苷Rg1、Re、Rb3的甲醇溶液,经UV-2550紫外分光光度计,在190~400 nm扫描,参考《中国药典》2010年版一部西洋参及人参含量测定项下波长,故选择203 nm为实验测定波长。
3.2 色谱柱的选择
曾分别采用Agilent HC C18(250 mm×4.6 mm,5 μm)、Diamonsil(2) C18(250 mm×4.6 mm,5 μm)、Luna C18(250 mm×4.6 mm,5 μm)3个不同的C18色谱柱进行试验,结果显示均可得到良好的分离。故规定本法的理论板数按人参皂苷Re峰计不得低于6 000。
3.3 提取方法与提取时间考察
分别对4种提取方法进行了考察。
(1)按原标准方法提取,取装量差异项下的本品内容物,研细,取约3 g,精密称定,加甲醇50 mL使溶解,滤过,残渣加甲醇洗涤3次,每次20 mL,合并滤液及洗涤液,蒸干,残渣加流动相使溶解,并定量转移至100 mL量瓶中,加流动相稀释至刻度,摇匀,滤过,取续滤液,即得。
(2)取装量差异项下的本品内容物,研细,取约1.5 g,精密称定,置100 mL量瓶中,加甲醇适量使溶解并稀释至刻度,摇匀,滤过,取续滤液,即得。
(3)取装量差异项下的本品内容物,研细,取约1.5 g,精密称定,置100 mL量瓶中,加流动相适量超声处理30 min,放冷;加流动相稀释至刻度,摇匀,滤过,取续滤液,即得。
(4)取装量差异项下的本品内容物,研细,取约1.5 g,精密称定,置100 mL量瓶中,加甲醇适量超声处理30 min,放冷;加甲醇稀释至刻度,摇匀,滤过,取续滤液,即得。
结果(1)、(2)、(4)相差不大,(3)因溶解时极易产生泡沫,溶解效果不佳,不易定容,无法进行测定。考虑到实验方便和节省时间,故选择方法(2)。
实验建立的方法简便、准确,重现性较好,为心悦胶囊质量标准提高提供了参考依据。
[1] Wang W, Zhao Y Q, Rayburn ER,et al.In vitro anti-cancer activity and structure-activity relationships of natural products isolated from fruits ofPanaxginseng[J].Cancer Chemotherapy and Pharmacology,2007,59(5):589-601.
[2] 翟鹏贵,赵珺彦,祝铃栋,等.西洋参制剂抗疲劳作用的实验研究[J].浙江中医药大学学报,2007,(6):761-762 .
[3] 黄新生.高效液相色谱法测定人参茎叶浸膏及人参根中的人参皂苷含量[J].中国中药杂志,2001,26(3):29-31.
[4] 许传莲.RP-HPLC法测定西洋参茎叶中6种人参皂苷的含量[J].吉林农业大学学报,2002,(3):53-55.
[5] 国家药典委员会.中国药典[S].一部.北京:中国医药科技出版社,2010:8.
[6] 李俨,李敬华.人参消渴胶囊中人参皂苷Rg1和人参皂苷Re的含量测定[J].中国药业,2011,20(2):48-49.
TheDeterminationofGinsenosideRg1,GinsenosideReandGinsenosideRb3inXinyueCapsulesByHPLC
YANG Ying*,WANG Hong-wei,YU Wen-jing
(JilinInstituteforFoodandDrugControl,Changchun130033,China)
Objective:An assay method was developed for the determination of Ginsenoside Rg1、Ginsenoside Re and Ginsenoside Rb3in Xinyue Capsules by HPLC.Methods:The analysis was performed on Lun C18(250 mm×4.6 mm,5 μm)column.Acetonitrile-water gradient elution,detector wavelength 203 nm;Results:Ginsenoside Rg1linear range is 0.098 9-1.798 0 μg;relevant coefficientr=0.999 1(n=5),Ginsenoside Re linear range is 0.312 0-5.38 μg;relevant coefficientr=0.999 2(n=5),Ginsenoside Rg1avevage recovery is 97.1%,RSD=2.46%(n=6).Ginsenoside Re avevage recovery is 97.5%,RSD=1.89%(n=6),Ginsenoside Rb3linear range is 0.448-8.96 μg;relevant coefficientr=0.999 1(n=5),Ginsenoside Rb3avevage recovery is 100.0%,RSD=2.28%(n=6).Conclusion:The method is simple,rapid and accurate,it is suitable for the quality control of strychnine.
Ginsenoside Rg1;Ginsenoside Re;Ginsenoside Rb3;Xinyue Capsules;HPLC
2013-01-18)
*
杨颖,E-mail:kangroo@xinhuanet.com
