脊柱多发性骨髓瘤的MR诊断价值
2013-09-14杨晓萍刘光耀王跃军
杨晓萍,张 茜,刘光耀,王跃军
多发性骨髓瘤(multiple myeloma,MM)是原发性恶性血浆B细胞在骨髓中无节制的增殖,伴异常的单克隆免疫球蛋白生成为特征的浆细胞恶性肿瘤[1],常破坏骨组织,引起多发溶骨性病变,以脊柱、肋骨、颅骨、骨盆较为常见[2-3]。本文总结分析43例脊柱MM的MRI表现,旨在加强对该疾病的认识,提高脊柱MM的诊断准确率。
1 资料与方法
1.1 一般资料 选择兰州军区兰州总医院2006年12月—2012年12月收治的有MRI资料的43例脊柱 MM,男 25 例,女 19 例;年龄(55.6 ±13.1)岁。均经骨髓穿刺活检证实。主要临床表现为全身骨痛、贫血、乏力、发热。
1.2 MR检查方法 使用西门子公司生产的1.5T Avanto、3.0T Verio MR扫描机进行脊柱MR扫描,按临床要求分节段脊柱扫描,包括矢状位自旋回波(SE)序列T1加权和快速自旋回波(FSE)序列矢状位、轴位FSE T2WI及T2WI-FS;20例行全脊柱扫描,通过自动移床技术一次完成大范围全景式脊柱矢状位成像。矢状位扫描层厚3~4 mm、间隔0.4 mm或无间隔,轴位标定感兴趣椎体层面逐层进行扫描,11例行增强扫描及DWI成像。选取Gd-DTPA 10~15 ml团注增强扫描,注射后扫描启动时间40 s~2 min,矢、冠、轴3个方位脂肪抑制增强扫描;选取b值为800 s/mm2的DWI矢状位扫描,矩阵256×128,激励2或3次。
2 结果
2.1 临床分期与MRI分型 临床分期以骨髓穿刺细胞数确定:每m2瘤细胞数<0.6×1012为临床Ⅰ期,(0.6 ~1.2) ×1012为临床Ⅱ期,>1.2 ×1012为临床Ⅲ期。参考Stabler等[4]分型标准将MM MRI表现分为正常型、弥漫型、局灶型、混合型、“椒盐”型。本组MRI正常型、局灶型、“椒盐”型以临床Ⅰ期常见,弥漫型、混合型以临床Ⅱ、Ⅲ期常见,见表1。

表1 43例脊柱多发性骨髓瘤的临床分期与MRI分型(例)
2.2 MR扫视受累椎体分布区域 43例脊柱MM MRI扫视到964个椎体,452个椎体受累(椎体附件同时受累算一个椎体,仅附件受累也归类于椎体受累),其中颈椎61个椎体受累,占13.5%;胸椎257个椎体受累,占56.8%;腰骶椎134个椎体受累,占29.7%。出现病理性骨折111个,占受累椎体的24.6%。
2.3 MRI表现 正常型6例,16个椎体骨折,占14.4%;弥漫型10 例,38 个椎体骨折,占 34.2%;局灶型7例,22个椎体骨折,占19.8%;混合型14例,20个椎体骨折,占18.0%;“椒盐”型6例,15个椎体骨折,占13.5%。正常型6例中,患者均有不同程度的骨质疏松及脂肪斑块沉积,表现为T1WI、T2WI均为不规则形高信号,T2WI信号更高,与皮下脂肪信号一致,此6例MR扫描后均被诊断为骨质疏松、骨质增生及骨质陈旧性或新鲜压缩骨折,最后通过骨髓穿刺确诊,见图1。弥漫型10例,表现为椎体T1WI信号普遍减低,信号相对较均匀,个别椎体见少许小斑点状T2WI为高信号,T1WI为略高信号,信号略不均匀,但程度不及“椒盐征”明显,见图2。局灶型7例,表现为正常椎体内或附件区散在圆形、类圆形或不规则形异常信号灶,大小相等或不等,病灶T1WI中央信号略低,周围信号略高,T2WI中央表现等信号,周围呈低信号,病灶境界均显示不清晰,见图3。混合型14例,表现为椎体T1WI呈弥漫性低信号背景下伴有椎体内或附件区多发局灶性更低信号灶,T2WI呈不均匀高信号,见图4。“椒盐”型6例,T1WI呈弥漫性斑点状高或低的混合信号,T2WI呈弥漫性斑点状低或等的混合信号,正常骨髓中可见到众多细小颗粒状病灶,见图5。
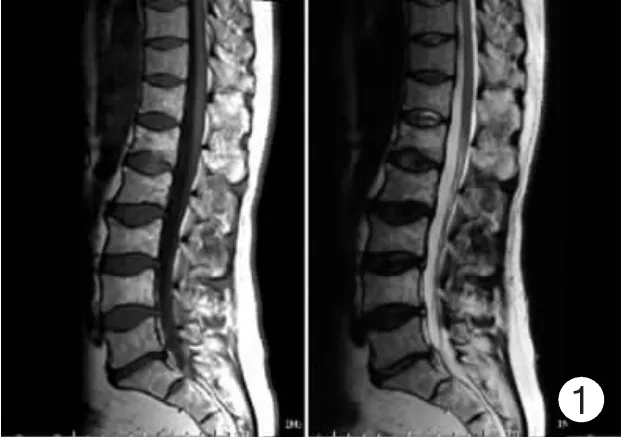
图1 正常型脊柱MM MRI表现
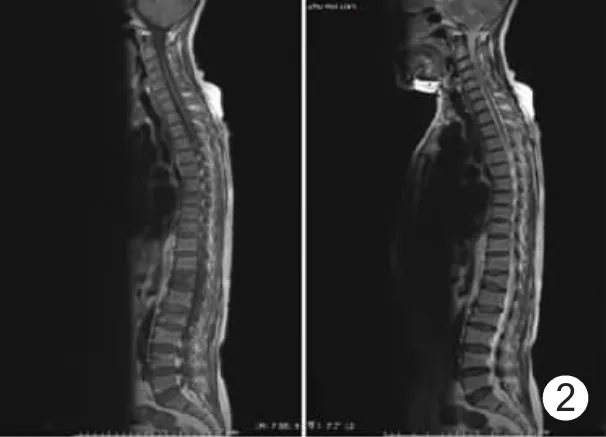
图2 弥漫型脊柱MM MRI表现

图3 局灶型脊柱MM MRI表现

图4 混合型脊柱MM MRI表现
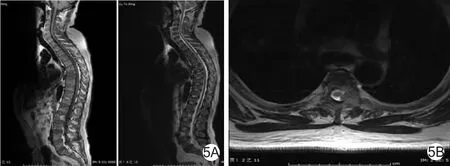
图5 “椒盐”型脊柱MM MRI表现
3 讨论
3.1 脊柱MM MRI分型的病理学分析 正常骨髓含有较多的脂肪成分,MRI常表现为中等T2、短T1信号,MRI对骨髓的改变(分布、成分、数量)很敏感。MM在T1WI上显示较好,多表现为高信号背景下不同信号强度的低信号;在T2WI序列上未经治疗的病变表现为高信号,而对治疗有反应时则表现为信号不同程度的减低;T2WI脂肪抑制序列由于脂肪信号被抑制,病灶高信号较T2WI更明显。
1996年Stabler等[4]将MM的MRI表现通过与细胞学对照分为5种类型,正常型:该型影像检查仅表现骨质疏松、压缩骨折改变,这与骨髓瘤分泌破骨细胞活动因子,该类因子抑制骨细胞的胶原合成,激活破骨细胞,引起骨量减少,造成骨质疏松,骨质破坏及压缩性骨折有关,这种骨折不以局灶性肿块为前提,而是由于骨质溶解吸收引起,表现为良性压缩性骨折,但骨髓穿刺仍可查到骨髓瘤细胞。弥漫型:是骨髓内正常的脂肪细胞被病理性的浆细胞普遍替代而减少,表现为全段脊柱的正常黄骨髓信号消失。局灶型:骨髓内正常的脂肪细胞被病理性的浆细胞替代,浆细胞聚集形成瘤结节,表现为区域性病变,单个或多个椎骨的大小、数目不等,形态不规则的长T1长T2软组织块。混合型:是局灶型和弥漫型的混合病理改变。“椒盐”型:骨髓中弥漫不均匀的小颗粒瘤细胞小灶与周围脂肪细胞的部分红骨髓相互混杂,形成T1WI高低不一的点状或小颗粒状混杂信号。
3.2 脊柱MM与转移瘤的MRI鉴别诊断 脊柱MM与转移瘤的MRI表现相似,以下分析可资鉴别:①病变分布的区别:脊柱MM常表现为多椎体连续受累,椎体受侵分布比例与转移瘤无明显差别[5],但呈跳跃性分布以转移瘤椎体常见,如果同一病例多个椎体MR表现不同,多考虑转移瘤[6],考虑与原发肿瘤的多次播散有关。由转移瘤的血供特点分析,甲状腺癌易转移到颈椎,肺癌易转移到胸椎,前列腺癌及子宫附件肿瘤易转移到腰骶椎等,脊柱转移部位与椎体供血有关。而MM脊柱浸润与椎体血供间并无明显相关性。②病灶MRI信号特点:MRI表现正常型MM,是通过临床表现确诊的。其他类型的MM,如弥漫型MM,表现受累椎体信号混杂,病灶境界不清[7]。而转移瘤表现为病变部分或完全取代了正常椎体松质骨应有的短T1高信号,在正常椎体信号的衬托下,椎体转移瘤境界清晰,表现为长T1信号[8]。局灶型MM椎体常呈圆形及类圆形受累,在T2WI上表现病灶周围低信号环绕的中央等信号影,压脂像显示较清晰[9]。而转移瘤表现为病灶周围骨小梁的破坏,破坏区域含水量丰富,在T2WI上转移灶周围常有条状高信号环包绕,即“晕征”[10]。“晕征”的出现高度提示转移瘤,可与MM进行鉴别。③椎体形态与附件破坏:脊柱MM椎体变形的发生率较低,转移瘤椎体变形的发生率较高。MM和椎体转移瘤均可累及附件,而MM的发生率较转移瘤低。④椎旁软组织影:MM和转移瘤椎体破坏所形成的软组织肿块的形态差异不明显,但有研究者认为,MM形成的软组织肿块表现“围管征”,即包绕椎管,填塞硬膜外间隙,硬膜囊狭窄,附件形态完整性基本保持,而转移瘤常以破坏椎体为中心向周围形成软组织肿块[11]。
3.3 MRI分型与临床分期的关系 临床Ⅰ期的MM,其骨髓浸润较轻,MRI表现为正常型及“椒盐”型;MRI显示累及范围小的局灶型MM,也多属于临床Ⅰ期;Ⅱ、Ⅲ期的MM,弥漫型等其他类型更多见,并发病理性骨折的MM多发生在临床Ⅱ、Ⅲ期,且多为MRI弥漫型病例。由此笔者认为,MM的临床分期与MRI表现分型之间可能存在某种程度的联系,根据MM MRI表现类型有助于临床分期和预后判断。临床分期又反映MM病程和肿瘤负荷,与治疗及预后有一定相关性,可用来判断疗效。
3.4 MRI诊断MM的优势 ①全脊柱MRI成像技术能够良好地显示脊柱全貌,多序列、多方位成像及无放射损害,对引起骨髓转变、浸润、取代、丢失、及水肿或缺血的病变比较敏感;图像空间、密度分辨率高,能够真实再现骨髓受侵情况。可以明确脊柱MM的浸润范围、病变大小、形态、邻近结构的变化、软组织改变及脊髓情况等,有利于准确了解病情。是目前影像学评价脊柱MM的首选手段[12-13]。②骨髓穿刺仅显示的是局部穿刺区域的骨髓情况,其结果有时不能真正反映病变情况,尤其是局灶型病例。MRI可以提示病变部位,有效地指导临床选择病理活检穿刺部位,避免盲目穿刺。
[1]Waheed S,Shaughnessy J D,Van Rhee F,et al.International staging system and metaphase cytogenetic abnormalities in the era of gene expression profiling data in multiple myeloma treated with total therapy 2 and 3 protocols[J].Cancer,2011,117(5):1001-1009.
[2]武忠弼.病理学[M].北京:人民卫生出版社,1993:355-356.
[3]马方宇,刘竞 .多发性骨髓瘤的治疗进展[J].中国医药指南,2013,11(8):460-461.
[4]Stabler A,Baur A,Bartl R,et al.Contrast enhancement and quantitative signal in MR imaging of mutiple myeloma:Assessment of focal and diffuse growth pattern in marrow correlated with biopsies and survival rates[J].AJR Am J Roentgenol,1996,167(4):1029.
[5]陈兵,罗飞,张滔,等.脊柱多发性骨髓瘤影像学对比分析[J].中国中西医结合影像学杂志,2012,10(2):155-157.
[6]邵建文,刘斌.脊柱转移瘤的MRI影像学诊断分析[J].牡丹江医学院学报,2013,34(1):66-67.
[7]曹成,杨惠林,胡海,等.脊柱多发性骨髓瘤影像学诊断的临床意义[J].中华核医学与分子影像杂志,2012,1(2):151.
[8]窦怀洲,赵兴举,王琛.脊柱转移瘤外科治疗的临床分析[J].中华肿瘤防治杂志,2008,15(11):858-860.
[9]姜亮,袁伟,刘晓光 ,等.脊柱多发性骨髓瘤的诊断与治疗——附36例报告[J].中国脊柱脊髓杂志,2011,21(7):540-544.
[10]王中伟.DR、CT、MRI及核素扫描在脊柱转移瘤诊断中的价值及优势[J].中国医药指南,2012,10(34):258-259.
[11]同志勤,陈银霞,刘振堂,等.脊柱多发性骨髓瘤与转移瘤的MRI鉴别诊断[J].中华放射学杂志,2004,38(2):175-177.
[12]Baur Melnyk A,Buhmann S,Becker C,et al.Wholebody MRI versus whole-body MDCT for staging of multiple myeloma[J].American Journal of Roentgenology,2008,190(4):1097-1104.
[13]Shortt C P,Gleeson T G,Breen K A,et al.Whole-Body MRI Versus PET in Assessment of Multiple Myeloma Disease Activity[J].American Journal of Roentgenology,2009,192(4):980-986.
