胰腺癌术后肠内营养护理的应用
2013-09-14王广胜
王广胜
湖北省宜昌市中心人民医院普外科,湖北宜昌 443000
胰腺癌患者常伴有不同程度的营养不良和免疫功能下降,术后死亡率及感染率较高[1]。营养支持重要的护理内容,正确有效的饮食护理可以增加患者营养,改善胃癌患者术后的机体营养状态,促进机体功能恢复,减少术后并发症[2]。研究表明,肠内营养比胃肠外营养更为安全,应用肠内营养支持可以及时预防并纠正营养不良的发生,并且可以更有效地减少并发症的发生[3]。本研究对20例胰腺癌术后患者早期采用肠内营养,并加强护理,取得了较好的效果,现报道如下:
1 资料与方法
1.1 一般资料
选取2011年1月~2012年8月宜昌中心人民医院(以下简称我院)40例胰腺癌患者,所有病例均经临床、影像学和病理检查确诊,无肝肾功能异常,无糖尿病患者,近期内为接受或免疫制剂及激素治疗。排除近期患有功能性胃肠病、甲状腺功能减退、结缔组织病、术后发生严重合并症及认知功能障碍者。其中,男24例,女16例;年龄42~70岁,平均(55.9±2.5)岁;病理类型:高分化腺癌16例,中分化腺癌13例,导管细胞癌11例。将所有患者根据术后营养方式的不同分为观察组和对照组,每组各20例。两组患者在年龄、性别、病理类型等方面比较差异无统计学意义(P>0.05),具有可比性。
1.2 方法
1.2.1 营养方式 两组手术方法相同,但术后营养方式不同。但两组患者能量供应按146.3 kJ/kg 计算,非蛋白热量/氮为564.3 kJ/kg[5]。①对照组:采用肠外营养,建立静脉通道,将一定量的葡萄糖、电解质、氨基酸、维生素脂肪乳剂通过微量泵从周围静脉或深静脉匀速输入到患者的体内。其余均混匀在3 L 聚乙烯袋中进行滴注(抗生素单独滴注)。②观察组:采用肠内营养支持,由我院营养科按患者情况进行匀浆膳的配置,其中包括鸡蛋、牛奶、米粉、奶粉、香菇、白糖、红枣、油、盐等,早期将匀浆膳通过鼻胃十二指肠管注入。其中每天为维持氮平衡,增强患者的免疫功能,满足机体的需要,应给的蛋白质>2 g/kg[4]。过多的蛋白质可增加肾脏的负担,出现氮质潴留,并可能导致腹泻,因此,在肠内营养时,蛋白质的供给控制在总热量的20%。初次胃肠道输入者,从1000 kcal/d 开始,2~3 d 后逐渐增加至人体需要量[6]。
1.2.2 肠内营养的护理 ①由于是鼻插管的不适感,使患者不易接受,甚至产生抵触情绪,因此,在鼻饲前护理人员将肠内营养高的意义,方法和医患如何配合都向患者和家属详细的进行说明,取得患者的配合[7]。②鼻饲前首先吸净咽喉部的分泌物,取右侧卧位,使用前端带有侧孔的5~6 F软质硅胶胃管,胃管的下端用液状石蜡润滑胃管,右手持胃管用拇、食指夹持胃管由一侧鼻孔缓缓插入胃管,插入到胃部,胃管长度以耳垂-鼻尖-剑突间距离为准[8]。插入时无阻力,则快速向下插入所需长度。插管操作一定要轻柔,切忌暴力推进,以免损伤黏膜。当胃管的插入深度达到标记时,取左侧卧位,可用抽吸胃液法或用听诊器在胃部听气过水声等方法确定胃管在胃内[9]。以贴胶将胃管妥善固定后可开始缓慢注入患者所需营养液。③鼻饲期间环境应保持整洁、安静、无强光刺激,认真精细的护理患者,鼻饲前30 min 不宜翻身或进行其他操作。固定胃管用的胶布宽度以1.5~2.0 mm 为宜,胶布要保持干燥,注意检查胶布处皮肤是否出现损伤,更换时须先以温水沾湿以防损伤患者皮肤[10]。每次鼻饲前后用2~3 mL 的温开水冲洗营养管,严格掌握如真的温度和浓度,温度为38~40℃,以防止引起患者腹泻或腹痛。每次鼻饲前先抽吸患者胃内容物[11]。④鼻饲结束后将胃管末端的盖子盖好,以纱布包裹好,待下次鼻饲时打开。做好口腔护理,每周更换鼻饲管。在输注营养液的过程中,护士应严密观察患者胃肠耐受情况,注意有无呕吐、腹胀、腹泻、明显胃潴留现象,并观察患者大便的颜色、性状及量。若明显腹胀、胃潴留、反复呼吸暂停,应停止鼻饲,采用静脉高营养积极预防感染,严格遵守无菌操作规程。并注意观察营养液有无污染,及时排除低蛋白血症引起的腹泻。加强巡视,预防少量的营养液反流可引起呼吸暂停甚至窒息,及时发现,及时处理。准确记录24 h出入量,严密监测患者的水、电解质、血糖变化。
1.3 评价指标
比较两组患者术后7 d 时的胃肠功能情况(反流、腹泻、腹胀、便秘等)、营养学指标变化、免疫功能情况,并发症(吸入性肺炎、消化道出血、感染等)的发生率及术后3个月的生活质量。①营养学指标:包括血浆白蛋白、血浆前白蛋白和血红蛋白。采集患者清晨空腹肘静脉血2 mL,放入-40℃冰箱保存,统一进行检测。检测仪器为日本生产的日立7170A 自动生化分析仪。②免疫功能:检测患者术前、术后7 d 免疫功能主要检测患者伤后7 d 的CD4+、CD4+/CD8+、IgM、IgG 的变化。采用由美国贝克曼公司生产的用于IMMAGE 800 仪器,测试方法为免疫比浊法。③生活质量:采用生活质量综合评定问卷(GQOLI-74)进行调查两组患者出院前的生活质量。共包括四个维度,躯体功能、心理功能、社会功能、物质生活状态,前三个维度有5个因子,最后一个维度有4个因子,每个项目评分采用5级(1~5级)。
1.4 统计学方法
采用SPSS 16.0 统计软件,计量资料采用均数±标准差(±s)表示,组间比较采用t检验,计数资料采用百分率表示,组间对比采用χ2检验。以P<0.05 为差异有统计学意义。
2 结果
2.1 两组术后7 d 胃肠功能及并发症比较
观察组术后7 d 的胃肠功能显著优于对照组(χ2=3.89,P<0.05),并发症显著少于对照组,差异有统计学意义(χ2=3.85,P<0.05)。见表1。
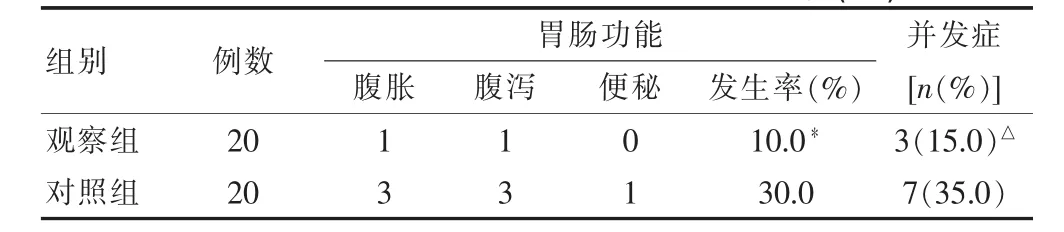
表2 两组术后7 d时胃肠功能及并发症比较(例)
2.2 两组患者术后7 d 时的营养学指标变化
营养支持7 d 时的血浆白蛋白、血浆前白蛋白和血红蛋白,观察组均显著优于对照组,差异有统计学意义(P<0.05)。见表2。
表2 两组患者营养相关生化指标分析(±s)
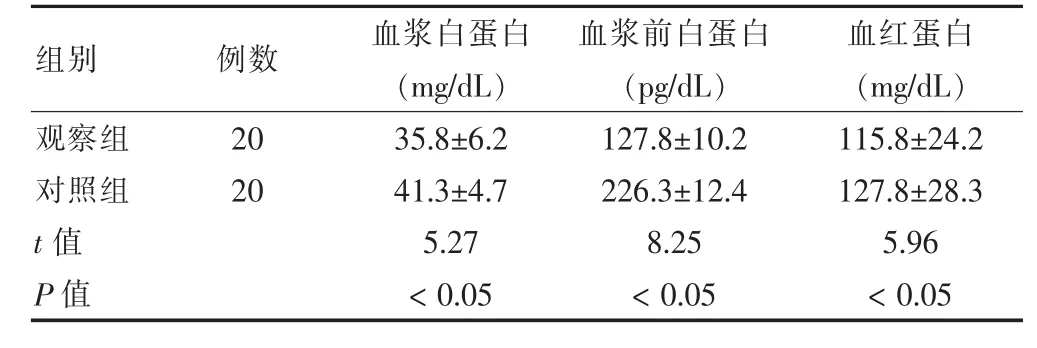
表2 两组患者营养相关生化指标分析(±s)
组别例数 血浆白蛋白(mg/dL)血浆前白蛋白(pg/dL)血红蛋白(mg/dL)观察组对照组20 20 t 值 P 值35.8±6.2 41.3±4.7 5.27<0.05 127.8±10.2 226.3±12.4 8.25<0.05 115.8±24.2 127.8±28.3 5.96<0.05
2.3 两组患者术后7d 时的免疫功能学指标比较
营养支持 7 d 的 CD4+、CD4+/CD8+、IgA、IgG, 观察组均显著高于对照组,差异有统计学意义(P<0.05)。见表3。
表3 两组患者免疫功能比较(±s)
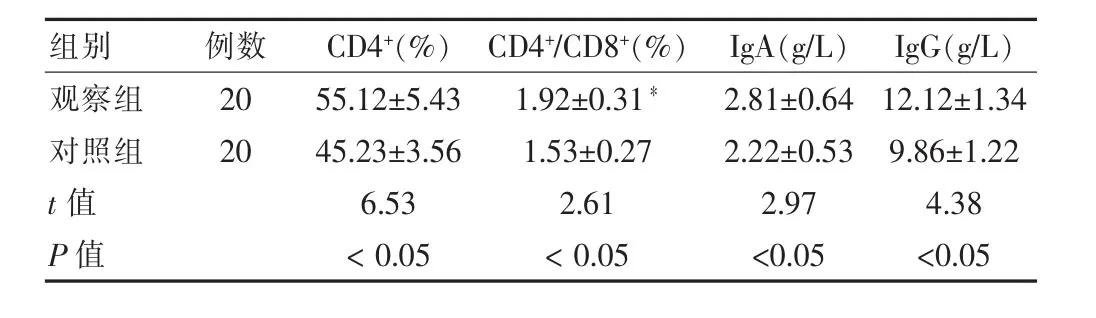
表3 两组患者免疫功能比较(±s)
组别例数 CD4+(%) CD4+/CD8+(%) IgA(g/L) IgG(g/L)观察组对照组20 20 t 值 P 值55.12±5.43 45.23±3.56 6.53<0.05 1.92±0.31*1.53±0.27 2.61<0.05 2.81±0.64 2.22±0.53 2.97<0.05 12.12±1.34 9.86±1.22 4.38<0.05
2.4 两组术后3个月的生活质量比较
观察组术后3个月时在躯体功能、心理功能、社会功能、物质生活状态方面的生活质量评分显著高于对照组,差异有统计学意义(P<0.05)。见表4。
3 讨论
手术是治疗胰腺癌的重要方法,但手术使胃的结构发生了变化,正常生理功能受到了影响,出现胃纳不佳,餐后饱胀,消化吸收功能紊乱等症状,容易发生蛋白质-能量营养不良[12]。营养是维持生命、保持健康的物质基础,在很大程度上饮食对机体的功能和状态有着重要的影响。营养支持作为其中的一个重要部分,对其转归具有十分重要的意义。因此,必须采用必要的护理手段改善患者的饮食状况,增加营养,以减少并发症的发生,提高机体免疫能力。胃肠外营养是常用的营养支持方式,但往往不能满足患者的营养需求,患者一旦营养不良住院期间就更容易并发肺炎及其他部位的感染,甚至胃肠道出血。肠内营养在近年来发展迅速,能有效改善患者的营养状态,食物可促进胃肠道激素增多,促进肠道屏障功能恢复且维持全身脏器功能,减轻应激状态下肠黏膜萎缩、降低肠道通透性、改善黏膜的免疫功能[3],还可防止菌群失调,降低肠道内膜屏障功能的损害和细菌内毒素的易位,预防由细菌或内毒素吸收而导致肠源性感染。还能刺激消化液和胃肠道激素的分泌,促进肠蠕动,增加内脏血液循环[13]。此外,食物中的葡萄糖还能促进巨噬细胞和单核细胞、T 淋巴细胞的增生和分化,增加机体防御能力。
表4 两组术后3个月的生活质量比较(分,±s)
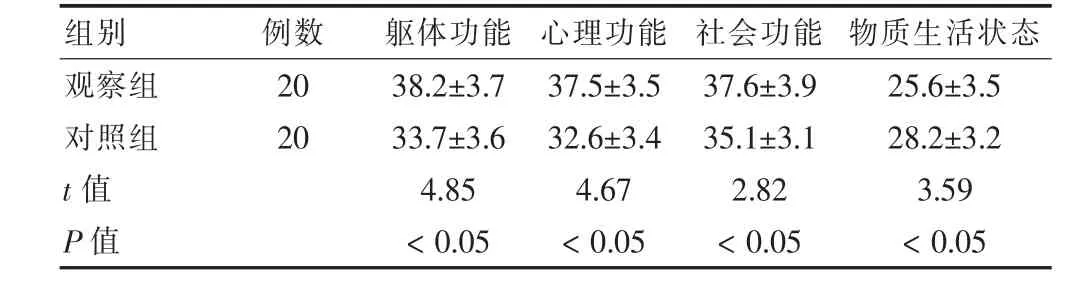
表4 两组术后3个月的生活质量比较(分,±s)
组别例数 躯体功能 心理功能 社会功能 物质生活状态观察组对照组20 20 t 值 P 值38.2±3.7 33.7±3.6 4.85<0.05 37.5±3.5 32.6±3.4 4.67<0.05 37.6±3.9 35.1±3.1 2.82<0.05 25.6±3.5 28.2±3.2 3.59<0.05
本研究结果显示,采用早期肠内应用的观察组术后7 d的胃肠功能显著优于对照组,并发症显著少于对照组(P<0.05);营养支持7 d 时的血浆白蛋白、血浆前白蛋白和血红蛋白,观察组均显著优于对照组(P<0.05);营养支持7 d 的CD4+、CD4+/CD8+、IgA、IgG, 观察组均显著高于对照组 (P<0.05);这提示肠内应用能够较好的改善胰腺癌患者术后的胃肠功能,增加营养,提高患者的免疫功能。结果还显示,观察组术后3个月时在躯体功能、心理功能、社会功能、物质生活状态方面的生活质量评分显著高于对照组(P<0.05)。
综上所述,对胰腺癌患者术后早期采用肠内应用可改善患者的体液免疫情况和营养学指标,增加抵抗力,减少并发症的发生。同时患者营养素平衡全面,安全价廉,合理方便,有利于提高术后生活质量。
[1]林丽华,杨观德,吴家园.肠内营养对胰腺癌患者术后营养支持的探讨[J].中国实用医药,2009,4(15):19-20.
[2]Komunm S,Nelwon KA,Wahh D,et al.Gastrointestinal symptom-samong inpatients with advance cancer [J].Am J Hosp pattiar Care,2002,9(5):351-355.
[3]李庆林,李宝平,贾仙.早期肠内营养对胃癌胰腺癌术后免疫功能的影响[J].山东医药,2007,47(30):96-98.
[4]Hadden JW.Immunode ciencv and cancer:prospects for correction[J].Int Immu opharmac,2003,12(3):1061-1071.
[5]赵亮,于永福,李慧.肠内营养支持治疗在肺癌化疗病人中的临床应用[J].肠外与肠内营养,2011,18(5):281-283.
[6]邵燕.食管癌术后早期肠内营养支持的护理[J].齐齐哈尔医学院学报,2005,26(1):111.
[7]郑家驹.肠内营养的实施与进展[J].临床内科杂志,2005,22(2):13.
[8]王庆喜.早期肠内营养在胃癌、胰腺癌术后的应用及护理[J].当代护士:专科版,2009,12(5):59-60.
[9]马玲,朱丹.早期肠内营养在急性重度胰腺炎中的应用及护理[J].护理学杂志,2005,20(4):81-82.
[10]李爱霞,张叶锋,张转玲.胰腺癌术后早期肠内营养治疗的护理体会[J].当代医学,2011,17(1):120-121.
[11]杨勇,全志伟,沈定丰,等.术后早期肠内免疫营养对老年胰腺癌、胃癌患者免疫的影响[J].胰腺病学,2008,2(3):155-158.
[12]囝瑞君.急性重症胰腺炎早期肠内营养的应用[J].中国医药导报,20l0,7(31):164-165.
[12]苏惠芳.庞旭峰,李舰.胰腺癌术后肠内营养护理[J].实用医药杂志,2010,27(8):719-720.
[13]许文华.对重症急性胰腺炎患者髓内营养护理研究[J].中国医药导报,2011,8(11):101-102.
