混合碱滴定分析
2013-09-03杨文静黎学明李武林牛丽丹
杨文静, 黎学明, 李武林, 牛丽丹
(重庆大学化学化工学院,重庆400044)
0 引言
混合碱一般是由碳酸钠、碳酸氢钠以及氢氧化钠的一种或几种组成。混合碱滴定分析是分析化学实验课的重要组成部分,而目前广泛使用的滴定方法是酚酞+甲基橙双指示剂法,其测定结果准确度及重现性较差[1-2]。为解决上述问题,众多改进和替代方法早已报道,如使用混合指示剂法[3-5]、利用碳酸钠和碳酸氢钠在氯化钠水溶液中溶解度不同的分离法[6]、碳酸钡沉淀分离法[7-8]、电位滴定法[9]、等离子体原子反射光谱法[10-11]等,但这些方法均比较耗时,且操作者不易掌握。废渣中混有一部分有色杂质,使滴定分析结果的可靠性不高。本文通过对双指示剂法测定混合碱中指示剂进行优化,能够较准确地判断滴定终点,滴定结果的准确性及重现性均比较好[12-15]。
1 混合碱测定原理
混合碱滴定通常采用标准HCl溶液为滴定剂来计算产品纯度,其滴定总反应式为:
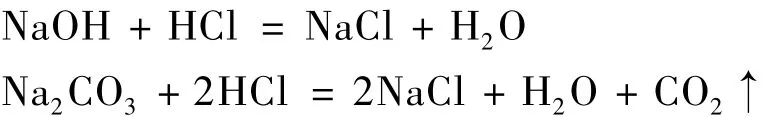
第一化学计量点时的滴定反应式为:

溶液中NaOH全部中和;Na2CO3只被滴定到NaHCO3,即只中和了一半。第二化学计量点时的滴定反应式为:

第一步生成的NaHCO3被进一步中和为CO2。
碳酸钠为多元弱碱,其 Kb1=1.79×10-4,Kb2=2.38 ×10-8,Kb1/Kb2≈104,基本满足被强酸准确滴定以及分布滴定的条件(CKb≥10-8。Kb1/Kb2≥104)。
根据其水解常数,通过计算可以得到如图1所示的碳酸钠分布系数曲线。

图1 碳酸盐分布曲线
从图1可以看出,第一化学计量点时,pH约为8.31,由于CO2-3的Kb1/Kb2的值略小于104,使滴定的第一个突跃不明显,当用酚酞作指示剂时,酚酞从红色到无色的变化不是很敏锐,终点误差较大。第二化学计量点时,pH约为3.88,溶液容易生成H2CO3过饱和溶液,影响第二化学计量点的准确判断。使得结果的准确度及重现性较差[16]。
2 实验
2.1 指示剂的选择
根据文献报道的结果,选取酚酞、甲酚红-百里酚蓝作为第一化学计量点指示剂,甲基橙作为第二化学计量点指示剂,比较不同指示剂时滴定的准确度。
2.2 混合碱液
(1)标准混合碱溶液配置。称取 2.674 9 g Na2CO3和1.987 5 g NaOH 于100 mL小烧杯中,用少量蒸馏水溶解并定量转移到1 000 mL容量瓶,稀释到相应刻度,并摇匀。
(2)称取4 g重庆某化工厂提供的碱样,加热溶于100 ml小烧杯中并定量转移到1 000 ml容量瓶,稀释到相应刻度,并摇匀。
2.3 滴定分析
用25.00 mL移液管移取25.00 mL溶液于250 mL锥形瓶中,分别加入上述指示剂,以HCl标准溶液(0.095 2 mol/L)滴定,平行测定3次。
3 结果讨论
3.1 第一化学计量点指示剂比较
由表1可以看出,使用酚酞作为第一化学计量点指示剂,由于其是从红色变到无色,颜色变化不是很敏锐,滴定剂盐酸用量很容易过等当点。如果使用甲酚红-百里酚蓝指示剂,其接近化学等当点时颜色是由紫色变为玫瑰红色,变化敏锐,其滴定剂用量较少。通过理论计算可以得知,当混合碱溶液达到第一化学等当点时,盐酸用量约为19.68 mL。可见,采用酚酞作为指示剂的结果偏大,而使用甲酚红-百里酚蓝作为指示剂的滴定结果更为合理。

表1 混合碱滴定第一化学计量点消耗盐酸量
3.2 第二化学计量点准确性比较
采用甲基橙作为第二化学计量点指示剂,对混合碱样进行分析,并通过BaCl2法对第二化学计量点盐酸用量进行了比较,结果如表2所示。

表2 混合碱滴定第二化学计量点消耗盐酸量
从表2中可以看出,采用双指示剂法滴定的结果与BaCl2法得到的结果非常接近,说明采用甲基橙作为第二化学计量点指示剂还是比较准确。下述分析混合碱样时采用甲酚红-百里酚蓝作为第一化学计量点指示剂,甲基橙作为第二化学计量点指示剂。
3.3 混合碱样的分析
重庆某化工厂提供的样品呈黑色,溶于水中后形成的溶液略显黄色,采用传统的双指示剂法滴定结果重现性也不好。采用上述建立的方法对未知碱样进行分析,并采用电位滴定法对结果进行了比较,结果如表3所示。
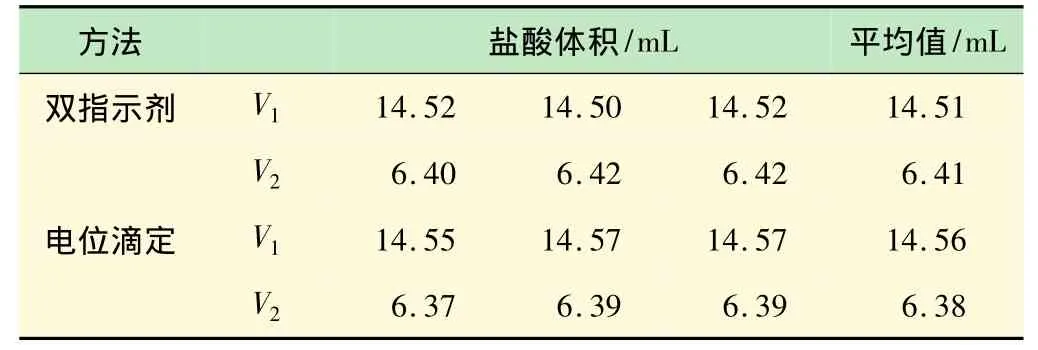
表3 未知碱样滴定分析结果
从滴定结果来看,双指示剂法滴定结果与电位滴定结果非常接近,可以作为该化工厂碱样的化学分析检测方法。
3.4 注意事项
(1)混合碱滴定快到终点时有可能生成H2CO3饱和溶液,pH为3.9。为了防止终点提前,需在接近终点时剧烈振荡溶液或加热以驱除CO2,本文采用的是加热溶液。
(2)本文采用双指示剂法测定混合碱的含量时,使用了甲酚红-百里酚蓝(由紫色至玫瑰红)、甲基橙(由黄色至橙色),颜色变化明显,消除了主观因素,分析结果准确度较高,溶液中含少量有色杂质也不会影响滴定结果。
4 结语
混合碱含量的测定时使用甲酚红-百里酚蓝+甲基橙双指示剂进行滴定,通过消耗的盐酸的体积计算混合碱中的组分与含量,整个操作简洁实用,测定结果较为准确,有较大推广价值。
[1] 刘晓辉,于文清,双指示剂法测定混合碱误差的主要原因[J].承德民族师专学报,2009,29(2):46-47.
[2] 杜 金.双指示剂法测定混合碱样的含量[J].辽宁化工,2010,39(8):888-900.
[3] 吴 镇.碱塔中混合碱含量的测定[J].江苏氯碱,2010(2):15-16.
[4] 金显春.关于“基础化学实验”中“混合碱”测定的教学探索[J].科教文汇(中旬刊),2009(35):197.
[5] 邓艳丽,杨诗佳.混合碱分析方法的改进[J].河南科技学院学报(自然科学版),2012,40(4):67-70.
[6] 宋 耘,李景鸽.碳酸氢钠产品中碳酸钠碳酸氢钠和水分的测定[J].纯碱工业,1989(4):10-14.
[7] 刘 煜.氯化钡法测定混合碱[J].辽宁师专学报(自然科学版),2001,3(3):30-32.
[8] 彭国丽;刘家春.氯化钡法测定混合碱的改进[J].金陵科技学院学报,2006,22(4):12-15.
[9] 李春晖,林培喜.自动电位滴定法用于混合碱的测定[J].茂名学院学报,2005,15(3):16-18.
[10] 段旭川.酸碱滴定法与电感耦合等离子体原子发射光谱法联合测定混合碱中碳酸钠和碳酸氢钠[J].冶金分析,2009,29(9):36-39.
[11] 段旭川.气态进样-电感耦合等离子体原子发射光谱法测定固体混合碱中的碳酸钠和碳酸氢钠[J].冶金分析,2009,29(2):45-48.
[12] 王晓艳.混合碱中碳酸氢钠的含量测定[J].化学工程与装备,2010(1):164-165.
[13] 杨晓瑛,杨青林.初探混合碱测定中指示剂的选择[J].吉林电力技术,1995(6):25-27.
[14] 沈巧莲.双指示剂法测定混合碱实验条件的优化[J].金华职业技术学院学报,2007,7(2):78-80.
[15] 张启伟.混合碱滴定分析中指示剂的选择[J].浙江师大学报(自然科学版),1996,19(1):89-91.
[16] 阎俊英.返滴定法确定混合碱第一计量点的探讨[J].商丘师范学院学报,2001,17(6):85-87.
