难治性高血压诊断治疗中国专家共识
2013-08-10孙宁玲霍勇王继光李南方陶军李勇严晓伟蒋雄京李学旺
孙宁玲 霍勇 王继光 李南方 陶军 李勇 严晓伟 蒋雄京 李学旺
难治性高血压(resistant hypertension,RH)是高血压治疗中的一个难点。随着人口老龄化以及肥胖、睡眠呼吸暂停低通气综合征、慢性肾脏病等疾病的增多,难治性高血压成为越来越常见的临床问题。血压控制不良会导致心、脑、肾等靶器官损害,从而促进临床心血管事件的发生,积极有效地使血压达标是高血压治疗的重要环节。影响血压难以达标的因素较多,包括患者的不良生活方式、患者的依从性差、药物治疗的不足或不规范以及继发性高血压等多方面。有效的诊断以及合理的药物治疗是控制难治性高血压的重要手段,近年介入性治疗方法的引进也为难治性高血压提供了治疗机遇。本共识旨在归纳难治性高血压的临床特点、诊断评估方法以及最佳血压控制的治疗策略。通过总结目前对难治性高血压的认识,呼吁广大临床医生关注并正确地诊治难治性高血压,从而进一步规范和提高我国的高血压防治水平。
一、难治性高血压的定义
在改善生活方式的基础上,应用了合理可耐受的足量3种或3 种以上降压药物(包括利尿剂)一个月以上血压仍未达标,或服用4 种或4 种以上降压药物血压才能有效控制,称为难治性高血压[1-3]。
二、难治性高血压的流行病学及患病率
目前难治性高血压患病率并不十分清楚,我国还没有准确的流行病学数据,但可以参考近年来几个临床试验中血压未达标的比例。ASCOT(Anglo-Scandinavian Cardiac Outcomes Trial-Blood Pressure Lowering Arm)试验结束时,血压未达标患者的比例为47%[糖尿病患者血压≥130/80 mm Hg(1 mm Hg = 0.133 kPa)],非糖尿病患者≥140/90 mm Hg)[4];ACCOMPLISH (Avoiding Cardiovascular Events through Combination Therapy in Patients Living with Systolic Hypertension)试验结束时,血压未达标患者的比例为26%(不论是否患有糖尿病,血压≥140/90 mm Hg)[5]。两个试验入选的都是具有高心血管病风险的高血压患者,这些患者中难治性高血压的比例可能较高。据2008 年美国心脏协会(AHA)关于难治性高血压诊断、评估和治疗的科学声明中所述:小样本研究显示,难治性高血压的患病率在普通门诊中约为5%[1]。参考近几年的临床试验结果,结合来自经常就诊的高血压患者的数据以及高血压研究中心的现有数据,推算难治性高血压病的患病率约为5% ~30%[6]。
三、难治性高血压的病因及病理生理学机制
难治性高血压的病因及病理生理学机制是多方面的。有基本病因,也有中枢及局部的神经体液机制等。高盐摄入、肥胖、颈动脉压力反射功能减退是高血压患者血压难以控制的基本原因。在此基础上,循环和组织中的肾素-血管紧张素-醛固酮系统(RAAS)的激活以及中枢或局部组织(特别是肾脏)交感神经活性的过度增高会启动炎症因子、氧化应激过程并促发动脉硬化和动脉粥样硬化的发生和进展,加重了血管结构和功能的异常,从而使增高的血压难以获得控制。研究显示,交感神经以及RAAS 的活性增强及持续存在是难治性高血压的重要发病机制之一[7]。临床和实验数据也表明,多重因素共同影响交感神经及RAAS 的激活,如胰岛素抵抗、内皮细胞功能障碍、间歇性低氧血症、体内容量负荷过高、醛固酮等作用于中枢神经系统以及动脉化学感受器和压力感受器的功能失调等。
肾脏在难治性高血压的发病过程中具有重要作用。其中,肾脏局部交感神经过度激活是难治性高血压的发病基础以及重要的病理生理学机制之一。肾交感神经由传入纤维和传出纤维组成。肾交感神经传入纤维的过度激活可以增强中枢交感神经系统的活性,使全身交感神经活性亢进,肾上腺素释放增加,从而引起肾脏、心脏和血管等靶器官的结构和功能改变,从而导致高血压的维持和进展。肾交感神经传出纤维的过度兴奋则可产生和分泌过多的去甲肾上腺素,使肾血管收缩,肾血流量减少,进而激活肾脏和全身RAAS系统;还使入球小动脉收缩强于出球小动脉,进而出现肾小球滤过率减少、水钠重吸收增多;同时,受刺激的颗粒细胞释放肾素,也进一步激活RAAS 系统。上述病理生理过程加剧了血压水平升高,参与难治性高血压的维持与进展[8-10]。
四、难治性高血压的诊断方法
(一)血压测量作为主要诊断手段[11]
1. 基本诊断方法:诊室血压测量:坐位、非同日测量3次以上血压,血压未达标时建议需同时测量双侧上臂血压,当两侧血压相差20 mm Hg 以上时,建议增加双侧下肢血压的测量。
2. 常规诊断方法:在诊室血压测量的基础上,建议进行连续家庭血压测量和24 小时动态血压测量(ABPM),以便排除白大衣效应、了解血压的特殊形态等(如杓型、非杓型、超杓型、晨峰现象和清晨高血压)。
(1)家庭自测血压
建议新诊断的高血压患者连续2 周、血压波动明显的患者连续3 ~7 d,早晚2 次(早在晨起服药前测定,晚在晨起服药后至少12 h 或睡前测定)进行家庭自测血压,每次测量3 遍,计算最接近的2 次血压的平均值。
家庭自测血压≥135/85 mm Hg 可诊断为高血压。
家庭自测血压表选择:建议采用上臂式肱动脉全自动血压表,自动血压表均应是通过欧盟、英国、美国认证的血压表。建议患者把全自动血压表带到诊室,以便检查患者的测量技术及仪器的准确性(与水银血压计对比)。
不适宜进行家庭自测血压的人群:情绪障碍和焦虑患者。
(2)24 小时动态血压测量
目的:了解全天血压的波动以及增高的程度,排除假性高血压。
高血压的诊断标准:全天(24 h)≥130/80 mm Hg,白昼≥135/85 mm Hg,夜间≥120/70 mm Hg[10],全天24 h 监测的有效次数达85%以上为有效检测。
不适宜人群:肥胖者臂围>40 cm,严重失眠,长期夜班者。
(二)鉴别影响血压控制不良的原因,进一步排除假性难治性高血压
1. 血压测量方法不正确:是假性难治性高血压的常见原因。例如,患者背部没有支撑可使舒张压升高,双腿交叉可使收缩压升高。
2. 治疗依从性:分析患者是否持续按医嘱服药。
3. 是否服用影响血压的药物(甘草、非甾体类抗炎药物、口服避孕药物、类固醇药物、环孢素、促红细胞生成素、麻黄素等)。
4. 生活方式因素:是否存在高盐摄入、过度焦虑、大量吸烟、重度肥胖、慢性疼痛等。
5. 是否存在高血压药物治疗不充分(药物用量不足或未使用利尿剂或联合方案不正确)。
6. 寻找继发性高血压的线索。
五、难治性高血压中继发性高血压的鉴别
近年随着对高血压病因认识的深入和临床诊断技术的提高,继发性高血压的检出率明显增高,继发性高血压往往具有血压水平较高、多种降压药物治疗血压仍然难以控制以及通过针对病因的治疗可以使血压得到明显控制甚至恢复至正常的临床特点。因此,鉴别出继发性高血压并加以相应的治疗是控制难治性高血压的关键环节之一。对所有难治性高血压均应该警惕继发性高血压的可能性,需要注意从病史、症状、体征及常规实验室检查中排查继发性高血压。
1. 难治性高血压中常见的继发性高血压的种类
(1)睡眠呼吸暂停综合征;(2)原发性醛固酮增多症;(3)肾实质性高血压;(4)肾血管性高血压;(5)嗜铬细胞瘤。
同时,应警惕精神心理因素所导致的难以控制的高血压。
2. 常用于继发性高血压鉴别的基本检查内容包括:血常规、尿常规、血电解质、血肌酐、血糖、血脂、24 h 尿钠、钾,以及颈动脉超声、超声心动图、肾脏超声和眼底检查等,记录身高、体重、计算体重指数(BMI)、按照MDRD 公式计算估算的肾小球滤过率(eGFR)等。
3. 对怀疑有继发性高血压的患者,进一步进行相应的专科检查,避免漏诊、误诊的同时,也要避免过度检查。
主要检查内容包括:肾动脉超声和CT;肾上腺CT;血浆醛固酮/肾素及其比值的测定;醛固酮抑制或激发试验;血、尿儿茶酚胺测定以及131碘-MIBG闪烁扫描示踪;皮质醇节律和地塞米松抑制试验;睡眠呼吸监测;必要时对患者进行精神心理评估。
专科检查方法的选择应基于高血压患者特殊的临床表现和相应的实验室检查提供的基本线索,围绕着疑似病因进行相应的专科检查,避免盲目地进行继发性高血压的病因筛查。针对病因明确的继发性高血压,应有的放矢地进行相应的药物、器具和手术治疗以提高降压治疗的有效性和治愈率。病因的诊断对于继发性高血压患者治疗策略的选择和预后的判断具有十分重要的意义。
六、难治性高血压的治疗
(一)矫治不良生活方式
这些措施主要包括:减轻体重[12-13];适度酒精摄入,建议大多数男性每日不超过2 杯(红酒300 ml 以内,啤酒600 ml 左右),女性或较低体重的人减半[14];限盐,建议食盐量<6 g/d[15-17];高纤维、低脂饮食[18];增加体力活动,每天进行50%最大耗氧量强度的有氧运动至少30 min,且每周尽量多的天数进行体力活动[19-20]。同时注意心理调节,减轻精神压力,保持心理平衡。
(二)药物治疗
1. 药物治疗原则
在纠正不良生活方式的同时还要注意降压药物的合理使用。药物选用的原则包括:停用干扰血压的药物;正确地使用利尿剂。同时注意合理的联合用药(包括单片固定复方制剂),以达到最大降压效果和最小不良反应。在药物治疗中应尽量应用长效制剂,以有效控制夜间血压、晨峰血压以及清晨高血压,提供24 h 的持续降压效果;另外,必须遵循个体化原则,根据患者具体情况和耐受性,选择适合患者的降压药物。
2. 药物治疗方法
需要联合≥3 种不同降压机制的药物,应选择长效或固定复方制剂以减少给药次数和片数。酌情将全天用药一次或分成早、晚服用,以控制全天血压。避免使用影响降压效果的药物或减至最低剂量。见表1。

表1 影响降压效果的药物
3. 治疗药物的选择
对于高肾素及高交感活性(以心率及血浆肾素活性作为基本判断标准)的患者以RAS 阻断剂(RASI)[血管紧张素Ⅱ受体拮抗剂(ARB)或血管紧张素转换酶抑制剂(ACEI)]和β 阻滞剂治疗为主。对于容量增高(高盐饮食、老年北方人群或以24 h 尿钠排泄作为基本判断指标)及循环RAS 低下的患者,以钙拮抗剂(CCB)和利尿剂为主;其中,对于摄盐量大的患者,在强调严格限盐的同时适当增加噻嗪类利尿剂的用量。对于eGFR≤30 ml·min-1·1.73 m-2的患者应采用襻利尿剂,非透析的肾功能不全的患者由于RAS 抑制剂的使用或剂量受限,应增加CCB 的剂量,甚至将二氢吡啶类与非二氢吡啶类CCB 合用。对于肥胖患者应增加RASI 的剂量[21]。以收缩压升高为主或老年患者应增加CCB 剂量。
通常的三药联合方案推荐RASI + CCB + 噻嗪类利尿剂。血压仍不能达标时可以考虑加用螺内酯(需要评估肾功能和潜在高血钾的风险),或联合β 阻滞剂、α-β 阻滞剂或α阻滞剂。血压仍不能达标时,可乐定、利血平等中枢神经抑制药物可作为联合方案的第五种降压药物的选择。
4. 降压药物使用的原则
(1)难治性高血压的基本药物治疗应以RASI(ARB 或ACEI)联合CCB 再联合噻嗪类利尿剂的三联治疗方案为主[1-2]。因为此种联合方案存在机制上的合理性,符合一般高血压患者的治疗。在此基础上如血压仍不能达标,可依据患者的临床特点联合其他的降压药物(包括β 阻滞剂、α-β受体阻滞剂或α 阻滞剂以及醛固酮拮抗剂等)。药物治疗流程图见图1。
(2)在三联的治疗方案中,药物剂量应为常规或双倍的可耐受剂量。
(3)在多药联合治疗的方案中,建议寻求疗效叠加、不良反应少、依从性高的方案,可由有经验的专科医师协助选择。
5. 治疗依从性评估
药物调整阶段每2 ~4 周随诊一次,通过与患者和家属交谈了解服药种类、数量、频率和时间,并根据每次处方的药量和患者取药的频率计算服药依从性。耐心听取患者对用药方案的意见并予以针对性的调整是提高治疗依从性的有效方法。服用β 阻滞剂者通过测定心率、服用α 阻滞剂者测定立位时血压变化、服用利尿剂者观察血尿酸、血钾的变化等均有助于判断服药的依从性情况。
6. 药物疗效以及安全性评估
除诊室血压外,需结合家庭自测血压和ABPM 评估降压疗效。根据患者服药频率和时间确定自测血压的次数和时间。对于血压波动性大的患者,应嘱咐患者在每次服药前、清晨、午间、傍晚、睡前测量血压并记录结果,并携带就诊。对于诊室血压与家庭自测血压不符、血压波动明显、需要了解夜间血压情况和全天血压平稳情况时,推荐进行24 ~48 h ABPM。
了解患者的任何不适,尤其是体位性头晕、黑矇;询问患者对治疗药物的耐受情况和不良反应。肾功能受损且应用RASI、醛固酮拮抗剂、合并襻利尿剂治疗的患者,必须定期测定血钾和血肌酐,并计算eGFR。
(三)有创介入治疗
由于难治性高血压患者心血管风险明显增加,控制血压是治疗的重要环节和目标。RH 患者在进行规范合理的强化治疗干预后,仍有部分患者的血压控制不满意。近年以肾动脉交感神经消融术(renal denervation,RDN)为代表的介入性治疗逐渐引起人们的关注,有望成为药物治疗控制不良的难治性高血压患者的一种新治疗方法。
由于肾交感神经过度激活是高血压的发病和维持的重要病理生理基础,并且肾交感神经纤维进出肾脏绝大部分经肾动脉主干外膜,这一解剖特点决定了RDN 可选择性消融大部分肾交感神经纤维。通过插入肾动脉的射频导管释放能量,透过肾动脉的内、中膜,选择性毁坏外膜的部分肾交感神经纤维,从而达到降低肾交感神经活性的目的[22]。
近年发表的几项小样本前瞻性研究(Symplicity HTN-1、Symplicity HTN-2 等[23-25])表明,难治性高血压患者进行RDN 术后,多数患者近中期对治疗有反应(定义为术后诊室收缩压降低≥10 mm Hg),而无明显的手术并发症,术后降压药物使用的数量有所减少(但一些患者仍需要多种降压药物控制血压)。该方法对于胰岛素抵抗、呼吸睡眠暂停综合征、室性心律失常、慢性肾脏病等存在交感神经过度激活的疾病可能也有一定的疗效,但是仍需要更大规模的有针对性的研究以及更长期的随访来确定其有效性和安全性。对于临床上明确判断为真性难治性高血压患者、无法耐受多种降压药物联合治疗或治疗依从性很差的高血压患者,在知情同意下可考虑行RDN,实施方法以及入选标准详见2012 ESH RDN Position Paper[6]。
七、临床建议
1. 难治性高血压患者的血压水平,需采用诊室血压测量结合家庭自测血压和24 小时动态血压检测的方法共同确定。在此基础上,对于已采用3 种以上最佳剂量、最合理配比的联合治疗方案(包括利尿剂)治疗至少>1个月后血压仍然在目标水平以上方可确定为难治性高血压。

图1 难治性高血压药物治疗选择流程图
2. 难治性高血压患者应评估降压药物治疗的合理性、依从性,应筛查、鉴别产生血压控制不良的原发因素和继发因素,以鉴别出真性难治性高血压。对于糖尿病、心力衰竭、冠心病、卒中、慢性肾脏病等多个器官受损以及多种疾病并存的难治性高血压患者需综合干预多种危险因素以及更积极地控制血压。
3. 在药物控制血压的同时,需坚持限盐、有氧运动、戒烟、降低体重为主的强化生活方式性治疗。
4. 采用优化的药物联合方案(CCB +RASI+利尿剂)以及最佳的、可耐受的治疗剂量。在此基础上如血压仍不能控制在靶目标水平,可根据患者的个体临床情况加用醛固酮拮抗剂(肾功能允许的情况下)或β 阻滞剂、αβ 阻滞剂或α 阻滞剂以及中枢神经系统拮抗药物。
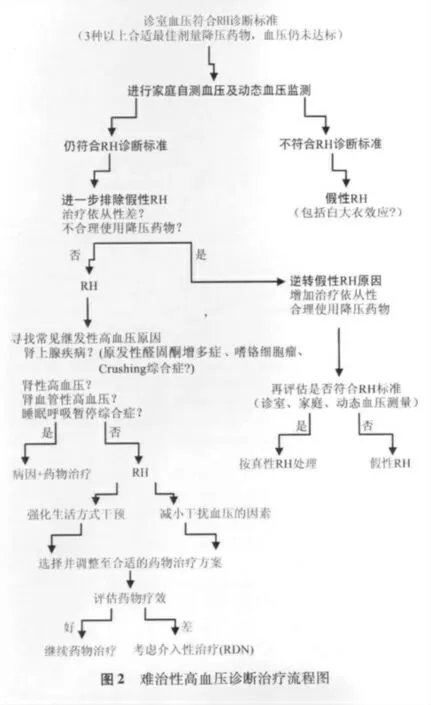
5. 经高血压专业医师的指导或在其诊断治疗下,确定为药物控制不良的难治性高血压,或不能耐受4 种以上药物治疗(治疗依从性很差)且存在心血管高风险的难治性高血压,在患者充分知情同意的基础上可考虑严格按照RDN 入选标准进行RDN 治疗。但鉴于RDN 还处于研究阶段以及我国还缺乏长期随访的结果,因此需谨慎、慎重、严格遵循操作规程、有序地开展RDN 治疗。难治性高血压诊断治疗流程见图2。
结束语:RH 是一种导致心脑血管疾病进展的高血压现象,明确的诊断和有效的治疗至关重要。但需要仔细地甄别病因,其中药物治疗剂量不足及不合理、用药时间不合适以及生活方式不良、治疗依从性差等均是重要的原因,继发性高血压也会导致血压难以控制。动态血压监测及家庭血压测量对于明确RH 患者的血压水平至关重要,因此需作为重要的诊断手段。严格的生活方式干预可改善血压,而合理、最佳、可耐受剂量的多种药物联合治疗(包括利尿剂)是控制血压的关键,其中,利尿剂、螺内酯、α-β 受体阻滞剂以及中枢神经拮抗剂的应用是不容忽视的。对于药物控制无效的真性难治性高血压患者,介入性RDN 技术可能是一种有效的治疗方法;但是,因其还处于研究阶段,需严格选择适应症、按操作规程慎重、有序地开展,也提倡进行有计划的前瞻性研究。
共识顾问:刘力生 王海燕 高润霖
共识专家:(按姓氏拼音排序)
陈鲁元 陈纪言 陈韵岱 高平进
葛均波 霍 勇 蒋雄京 李虹伟
李南方 李学旺 李 勇 卢成志
牟建军 谌贻璞 孙宁玲 陶 军
王继光 王建安 王伟民 王 文
王 玉 吴海英 吴兆苏 谢良地
严晓伟 曾春雨 张抒扬 张宇清
赵连友 祝之明
共识秘书:喜杨 马为
[1] Calhoun DA,Jones D,Textor S,et al. Resistant hypertension:diagnosis,evaluation,and treatment. A scientific statement from the American Heart Association Professional Education Committee of the Council for High Blood Pressure Research. Hypertension,2008,51:1403-1419.
[2] 中国高血压防治指南修订委员会. 中国高血压防治指南2010. 中华高血压杂志,2011,19:701-743.
[3] Chobanian AV,Bakris GL,Black HR,et al. Joint National Committee on Prevention,Detection,Evaluation,and Treatment of High Blood Pressure. National Heart,Lung,and Blood Institute;National Heart,Lung,and Blood Institute;National High Blood Pressure Education Program Coordinating Committee.Seventh report of the Joint National Committee on prevention,detection,evaluation,and treatment of high blood pressure.Hypertension,2003,42:1206-1252.
[4] Dahlf B,Sever PS,Poulter NR,et al. ASCOT Investigators.Prevention of cardiovascular events with an antihypertensive regimen of amlodipine adding perindopril as required versus atenolol adding bendroflumethiazide as required,in the Anglo-Scandinavian Cardiac Outcomes Trial-Blood Pressure Lowering Arm (ASCOT-BPLA):a multicentre randomised controlled trial.Lancet,2005,366:895-906.
[5] Jamerson K,Weber MA,Bakris GL,et al. ACCOMPLISH Trial Investigators. Benazepril plus amlodipine or hydrochlorothiazide for hypertension in high-risk patients. N Engl J Med,2008,359:2417-2428.
[6] Schmieder RE,Redon J,Grassi G,et al. ESH position paper:renal denervation-an interventional therapy of resistant hypertension. J Hypertens,2012,30:837-841.
[7] Tsioufis C,Kordalis A,Flessas D,et al. Pathophysiology of resistant hypertension:the role of sympathetic nervous system.Int J Hypertens,2011,ID:642416.
[8] Barajas L,Liu L,Powers K. Anatomy of the renal innervation:intrarenal aspects and ganglia of origin. Can J Physiol Pharmacol,1992,70:735-749.
[9] Hering D,Mahfoud F,Walton AS,et al. Renal denervation in moderate to severe CKD. J Am Soc Nephrol,2012,23:1250-1257.
[10] Laurent S,Schlaich M,Esler M. New drugs,procedures,and devices for hypertension. Lancet,2012,380:591-600.
[11] 中国血压测量工作组.中国血压测量指南. 中华高血压杂志,2011,19:1101-1115.
[12] Aucott L,Poobalan A,Smith WC,et al. Effects of weight loss in overweight/obese individuals and long-term hyper-tension outcomes:a systematic review. Hypertension,2005,45:1035-1041.
[13] Neter JE,Stam BE,Kok FJ,et al. Influence of weight reduction on blood pressure:a meta-analysis of randomized controlled trials. Hypertension,2003,42:878-884.
[14] Chobanian AV,Bakris GL,Black HR,et al. National Heart,Lung, and Blood Institute Joint National Committee on Prevention,Detection,Evaluation,and Treatment of High Blood Pressure;National High Blood Pressure Education Program Coordi-nating Committee. The Seventh Report of the Joint National Committee on Prevention,Detection,Evaluation,and Treatment of High Blood Pressure:the JNC 7 report. JAMA,2003,289:2560-2572.
[15] He FJ,Markandu ND,MacGregor GA. Modest salt reduction lowers blood pressure in isolated systolic hypertension and combined hyper-tension. Hypertension,2005,46:66-70.
[16] Vollmer WM,Sacks FM,Ard J,et al. DASH-Sodium Trial Collaborative Research Group. Effects of diet and sodium intake on blood pressure:subgroup analysis of the DASH-sodium trial.Ann Intern Med,2001,135:1019-1028.
[17] Singer DR,Markandu ND,Sugden AL,et al.Sodium restriction in hypertensive patients treated with a converting enzyme inhibitor and a thiazide. Hypertension,1991,17:798-803.
[18] Appel LJ,Moore TJ,Obarzanek E,et al. A clinical trial of the effects of dietary patterns on blood pressure. DASH Collaborative Research Group. N Engl J Med,1997,336:1117-1124.
[19] Kokkinos PF,Narayan P,Colleran JA,et al. Effects of regular exercise on blood pressure and left ventricular hypertrophy in African-American men with severe hypertension. N Engl J Med,1995,333:1462-1467.
[20] Whelton SP,Chin A,Xin X,et al. Effect of aerobic exercise on blood pressure:a meta-analysis of randomized,controlled trials.Ann Intern Med,2002,136:493-503.
[21] Jordan J,Yumuk V,Schlaich M,et al. Joint statement of the European Association for the Study of Obesity and the European Society of Hypertension:obesity and difficult to treat arterial hypertension. J Hypertens,2012,30:1047-1055.
[22] DiBona GF, Esler M. Translational medicine: the antihypertensive effect of renal denervation. Am J Physiol Regul Integr Comp Physiol,2010,298:R245-R253.
[23] Krum H,Schlaich M,Whitbourn R,et al. Catheter-based renal sympathetic denervation for resistant hypertension:a multicentre safety and proof-of-principle cohort study. Lancet,2009,373:1275-1281.
[24] Simplicity HTN-1 Investigators 2011. Catheter-based renal sympathetic denervation for resistant hypertension:durability of blood pressure reduction out to 24 months. Hypertension,2011,57:911-917.
[25] Simplicity HTN-2 Investigators,Esler MD,Krum H,et al. Renal sympathetic denervation in patients with treatment-resistant hypertension (The Symplicity HTN-2 Trial):a randomised controlled trial. Lancet,2010,376:1903-1909.
