更昔洛韦在单壁碳纳米管修饰电极上的电化学行为
2013-07-03常竹马啸华
常竹,马啸华
(商丘师范学院 化学化工学院,河南 商丘 476000)
更昔洛韦(ganciclovir)是一种广谱抗病毒药[1],其化学名称为9-(1,3-二羟基-2-丙氧甲基)鸟嘌呤.更昔洛韦可适用于免疫缺陷患者(包括艾滋病患者)并发巨细胞病毒视网膜炎的诱导期和维持期治疗.亦可用于接受器官移植的患者预防巨细胞病毒感染及用于巨细胞病毒血清试验阳性的艾滋病患者预防发生巨细胞病毒疾病.是目前临床治疗疱疹病毒感染的首选药物之一.因此对其测定方法的研究在临床应用和探讨其生理机制方面具有重要的实际意义.目前更昔洛韦的分析方法主要有紫外分光光度[2,3]、高效液相色谱法[4,5]等、非水滴定法等.
近年来基于更昔洛韦的电化学活性而建立起来的电化学分析法已有较多报道[6-8].高作宁等研究了更昔洛韦在SDBS 胶束中的电化学行为[9].然而,关于更昔洛韦的电化学氧化的报道较少,仅有在碳糊电极上利用其电化学氧化测定的报道[10].
碳纳米管是一种良好的电极修饰材料[11,12],由于碳纳米管具有独特的电子效应和强吸附性质等,已成为电化学领域的研究热点[13].本文旨在利用碳纳米管对更昔洛韦的吸附性能,研究更昔洛韦在单壁碳纳米管修饰电极上的电化学行为.研究表明此修饰电极对更昔洛韦的氧化具有明显的电催化作用,峰电流显著增大,灵敏度明显提高.并且该电极制备简单,具有良好的重现性和稳定性,可用于药剂中更昔洛韦的测定.
1 实验部分
1.1 仪器与试剂
LK98BII 电化学工作站(天津兰力科公司),电化学实验用三电极系统:单壁碳纳米管修饰玻碳电极为工作电极,饱和甘汞电极(SCE)为参比电极,铂丝为对电极;KS-300D 型超声仪(宁波科生仪器厂);PHS-3C 型数字酸度计(杭州东星仪器设备厂).
单壁碳纳米管(SWNT,中科院成都有机化学研究所);更昔洛韦(天津药业集团新郑股份有限公司081106),注射用更昔洛韦(海南中化联合制药工业有限公司,批号090801);N,N-二甲基甲酰胺(DMF,上海实验试剂有限公司);其它试剂均为分析纯;所有试剂均未经纯化.试验用水为二次蒸馏水.支持电解质:0.04MB-R(磷酸+冰乙酸+硼酸)缓冲液(pH=4.00).
1.2 单壁碳纳米管修饰电极的制备
将直径为3 mm 玻碳电极依次用0.3 μm 和0.05 μmAl2O3粉末在抛光布上抛光,使成镜面,然后分别用乙醇和蒸馏水超声清洗,自然晾干待用.称取SWNT 5 mg,加入到10 ml的DMF 试剂中,经超声振荡搅拌,SWNT分散于DMF 中,形成黑色的悬浊液.取此黑色悬浮液适量滴加在处理好的玻碳电极表面,置于红外灯下,待溶剂完全挥发后即可使用.
1.3 实验方法
取含一定量的更昔洛韦的10 ml 0.04MB-R(pH=4.00)缓冲溶液于电解池中,采用三电极系统,在0.5 ~1.5 V 范围内进行循环伏安扫描,记录更昔洛韦的氧化峰电流.
2 结果与讨论
2.1 更昔洛韦的电化学行为
在0.04MB-R(pH=4.00)缓冲溶液中,更昔洛韦在SWNT 修饰惦记上的循环伏安曲线见图1.由曲线b 可知,在空白溶液中SWNT 修饰电极没有电化学响应,加入1.0×10-5M更昔洛韦后,产生了1个峰(曲线c).在1.08 V处的氧化峰与裸玻碳电极相比,其电位正移了约30 mV,峰电流增加了近15倍,其原因可能是更昔洛韦能在SWNT 表面吸附,并且SWNT 具有促进电极反应的电子交换催化特性,从而产生灵敏的氧化还原电流.
更昔洛韦在SWNT 修饰电极上在1.08 V处产生一个氧化峰,反向扫描时,没有出现相应的还原峰,表明更昔洛韦在修饰电极上的电化学过程是一个不可逆过程.根据文献报到,更昔洛韦的氧化位点是C-8位,即在1.08 V处的氧化峰是把C 上的H 氧化成—OH所致[6].
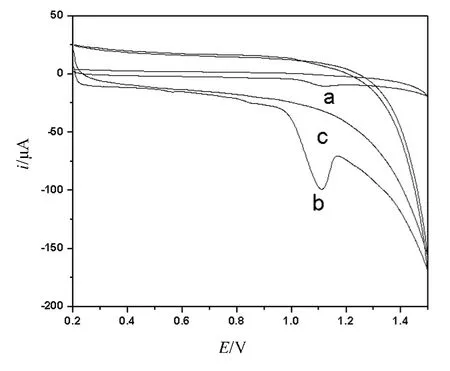
图1 更昔洛韦在不同电极上的循环伏安图
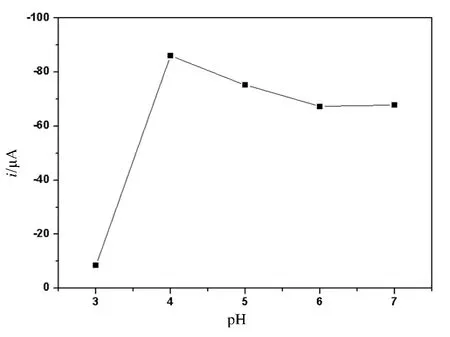
图2 pH 对更昔洛韦氧化峰电流的影响
2.2 实验条件优化
2.2.1 支持电解质的选择
考察了1.0×10-5M更昔洛韦在0.1MHAc-NaAc (pH=3.5 ~5.6)、0.1MNa2HPO4-NaH2PO4(pH=4.8 ~8.1)、0.04MB-R (pH=4.0 ~8.0)、0.1M酒石酸-酒石酸钠(pH=3.5 ~5.6)缓冲溶液中的氧化峰电流,结果发现更昔洛韦在这几种缓冲溶液中都有氧化峰,但是氧化峰的位置、峰形、峰电流有所不同.其中在0.04 MB-R 缓冲溶液中更昔洛韦的氧化峰形较好,峰电流较高,背景电流较低,故选用0.04MB-R 缓冲溶液作为支持电解质进行电化学测定.
2.2.2 pH 值的选择
配制了pH 为3.0 ~7.0的一系列0.04MB-R 缓冲溶液,利用循环伏安法研究了氧化峰电流和峰电位与pH的关系.研究发现,随着pH 值的增加,氧化峰电位负移,表明其在SWNT 修饰电极上的氧化反应过程中有质子参与.氧化峰电流随pH 值的增大先增大后减小,如图2所示.当pH 为4.0 时峰电流最大,故选择pH 值为4.0的缓冲溶液作为分析体系.
2.2.3 修饰剂用量的影响
SWNT-DMF分散在电极表面的用量会影响更昔洛韦的氧化峰电流.实验研究了更昔洛韦的氧化峰电流与SWNT-DMF分散液用量的关系.当用量少于10 μL 时,峰电流随用量的增加而显著增大,这是因为用量增多,富集效率随之提高,导致峰电流增大.当分散液的用量超过10 μL 之后,峰电流逐渐降低.这是因为碳纳米管具有优异的导电性能,而DMF 是电的不良导体,能阻碍更昔洛韦与电极之间的电子交换,所以分散液用量增加,峰电流反而降低.故本实验修饰剂用量选用10 μL.
2.2.4 扫描速度的选择
用循环伏安法研究了氧化峰电流与扫描速度的关系,如图3所示.在0.005 ~0.50 V/s 之间,氧化峰电流随扫描速度的增加而线性增加,线性方程为ip(μA)=-7.78-1345 v(V/s)(r=-0.9978),表明更昔洛韦在SWNT 修饰电极上的氧化过程受吸附控制.当扫描速度过高时,充电电流过大,影响测定的准确性.为了获得较大的峰电流,本实验选择扫描速度为0.5 V/s.
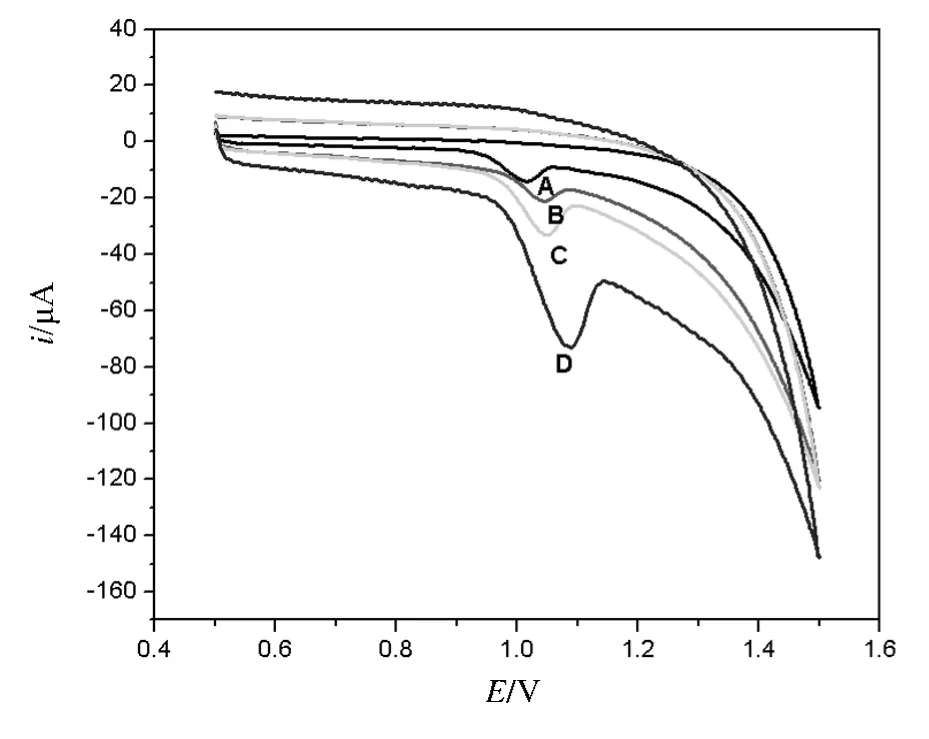
图3 不同扫描速度下更昔洛韦(1.22×10 -4 M)在碳纳米管修饰电极上的循环伏安图
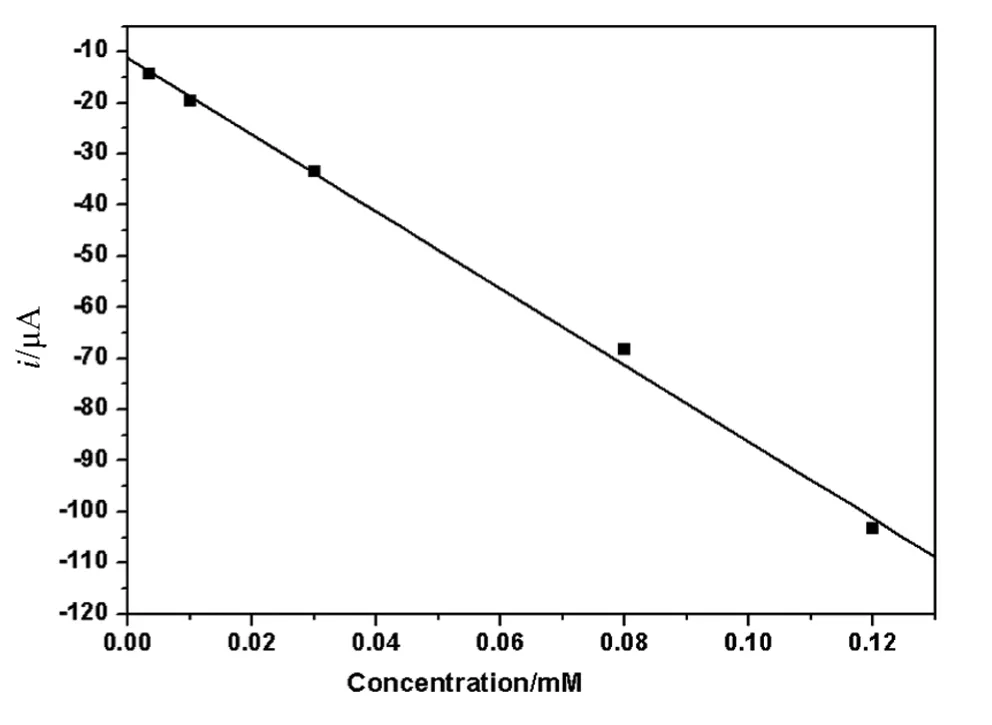
图4 更昔洛韦在碳纳米管修饰电极上的氧化峰电流与浓度线性关系
2.3 线性范围和检出限
在上述优化的实验条件下,考察了更昔洛韦氧化峰电流大小与其浓度的关系(图4).结果表明,更昔洛韦的氧化峰电流与其浓度在3.5×10-7~1.2×10-5M范围内呈良好的线性关系,线性回归方程为ip(μA)=-11.28 – 750.44 c(mM),(r=-0.9988),检测限为1.8×10-8M.当浓度高于1.2×10-5M时,氧化峰电流随浓度增加而几乎不变,进一步说明更昔洛韦在修饰电极表面发生了吸附.
2.4 修饰电极的稳定性与重现性
同一支玻碳电极以同样的方式分别修饰SWNT 5次,然后浸入到同一份更昔洛韦溶液中,5次测定的峰电流相对标准偏差(RSD)为3.9%.同一支SWNT 修饰电极在5份同样的更昔洛韦溶液中测定,5次测定的峰电流相对标准偏差为3.3%.同一支玻碳电极修饰SWNT 24 h 后再测定同样浓度且新鲜配制的更昔洛韦溶液,峰电流下降了8.3 %.以上实验结果说明SWNT修饰电极具有很好的稳定性与重现性.
2.5 干扰实验
在此体系中研究了一些常见的金属离子和有机化合物对更昔洛韦测定的影响.结果发现当更昔洛韦浓度为1.0×10-5mol/L 时,50倍的抗坏血酸、尿酸、尿素、葡萄糖、酒石酸、柠檬酸、Zn2+、Cu2+、Cd2+、Fe3+,100倍的K+、Na+、Ca2+、Mg2+、Al3+、NH4+、Cl-、Ac-、NO3-、SO42-等的存在几乎不干扰更昔洛韦的测定(相对误差<5%),表明SWNT 修饰电极测定更昔洛韦的抗干扰能力较强.
3 结 论
本文采用循环伏安法研究了更昔洛韦在碳纳米管修饰电极上的伏安行为,同时对更昔洛韦的电极反应进行了初步探讨.结果表明,碳纳米管修饰电极对更昔洛韦有较好的响应,其灵敏度优于使用玻碳电极直接测定,具有良好的重现性,可用于低浓度的检测.
[1]姜宏,李保院,韩业坤,等.更昔洛韦的临床应用进展[J].齐鲁药事,2006,25(3):166-168.
[2]王增寿,朱光辉,林光勇.更昔洛韦凝胶剂的制备及质量控制[J].广东药学,2002,12(4):24-25.
[3]陈华士,林志秀.HPLC 测定注射用更昔洛韦的含量[J].广东药学,2005,15(1):10-12.
[4]吴畏,何凤慈.更昔洛韦分散片的研制及体外溶出特征[J].中国药房,2005,16(12):910-912.
[5]李志勤.RP-HPLC 法测定血清中更昔洛韦浓度[J].中国药师,2005,8(8):675-676.
[6]BENGI u,BURCU d,SIBEL a o.Electrochemical studies of ganciclovir at glassy carbon electrodes and its direct determination in serum and pharmaceutics by square wave and differential pulse vohammetry[J].Analytica Chimica Acta,2005,537:307-313.
[7]GAO z n,PENG j,HAN x x.Electrochemical behaviors of ascorbic acid and uric acid in the presence of micelles and their selective determination application[J].Polish J Chem.,2007,81:441-454.
[8]PENG j,GAO z n.Micelles influence on electrochemical behaviors of catechol and hydroquinone and their simultaneous determination[J].Anal and Bioanal Chem.,2006,384(7-8):1525-1532.
[9]犹卫,高作宁.更昔洛韦在SDBS 胶束中的电化学行为及其电化学测定方法[J].宁夏大学学报,2009,30(1):55-57.
[10]李春哲,王桂芬,王爽,林晓华.更昔洛韦的电化学测定[J].化学研究与应用,2008,20(4):442-445.
[11]Nugent JM,SanthanamK SV,RubioA,et a1.Fast electron transfer kinetics on multiwalled carbon nanotube microbandle electrodes[J].Nano Let.,2001,1(2):87-91.
[12]Zhang b,IJang j,Xu c l,et a1.Electric double-layer capacitors using carbon nanotube electrodes and organic electrolyte[J].Matter Lett.,2001.,51(6):539-542.
[13]王宗花,刘军,颜流水.碳纳米管修饰电极的孔性界面对电分离多巴胺和抗坏血酸的影响[J].高等学校化学学报,2003,24(2):236-240.
