电化学发光免疫分析仪残余试剂的再利用
2013-05-24梁大立李介华蓝永乐邱瑞霞黄延峰
梁大立 李介华 蓝永乐 邱瑞霞 黄延峰
暨南大学医学院附属清远医院 清远市人民医院检验中心,广东清远 511500
电化学发光免疫分析 (electrochemiluminescence immunoassay,ECLIA)是电化学发光和免疫测定相结合的新一代标记免疫测定技术。因标志物为非放射性物质,而且实现自动化,具有快速、简便、灵敏、特异等特点,己广泛应用于各种激素、肿瘤标志物、药物及其他微量生物活性物质的测定[1],但配套试剂均需进口,测定成本高,为独立包装、固定测试数、条码自动记录,使瓶中残余试剂不能再利用而造成浪费。为充分利用医学资源,在保证检验质量的前提下,笔者对罗氏E170电化学发光免疫分析仪残余试剂混合再利用的可行性进行研究,现报道如下:
1 仪器与试药
1.1 仪器
瑞士罗氏公司E170全自动电化学发光免疫分析仪。
1.2 试药
定标物为罗氏原装配套,PCT质控物为罗氏公司提供,批号为168843、168845;CA72-4质控物为美国伯乐公司提供,批号为54551、54553。新试剂为罗氏E170原装配套试剂;混合试剂为罗氏E170同一项目、同一批号的试剂,经仪器扫描条码为0测试,将瓶中残余试剂每3~4瓶混合为1瓶。所有试剂均在有效期内使用。
2 方法与结果
2.1 方法
2.1.1 手工输入条码信息 将罗氏三联装试剂白色瓶上的15位数字信息,输入到相应的试剂位空白栏。
2.1.2 定标与质控 按要求保养仪器,对E170分析仪所检验项目进行定标及常规质控,定标通过及室内质控在控方可进行以下实验。
2.1.3 混合试剂精密度试验 根据《体外诊断试剂分析性能评估指导原则》进行,取高、低2个浓度的质控物,每天做2批次的测试,每批次测试时,对同一样品作双份测定,共做20 d。得80个测试结果,计算批内及批间精密度。
2.1.4 混合试剂准确性测试 两种试剂分别检测PCT、CA72-4高、低浓度质控物各20次,检查分析结果是否在允许范围内,并进行结果比较。
2.1.5 标本测定 用新试剂和混合试剂对80例血清样本进行PCT、CA72-4测定,对结果进行比较及相关性分析。
2.1.6 回收试验 分别在1000μL正常血清内加入PCT、CA72-4低值、高值质控血清100μL,制成2个待测标本进行回收试验,每样本用混合试剂重复检测3次,取平均值,计算回收率。回收率为90%~110%,结果为可接受[2]。
2.1.7 稳定性试验 每天用罗氏与伯乐低值、高值质控物作为监控品,对混合试剂进行3周监控。
2.2 统计学方法
本研究所有数据采用SPSS 12.0软件进行统计分析,计量资料以()表示,进行 t检验,以P<0.05为差异有统计学意义。
2.3 结果
2.3.1 混合试剂精密度检测结果 混合试剂检测质控物PCT、CA72-4批内、批间CV均 <5%,符合卫生部临床检验中心的要求(< 10%)(表 1)。
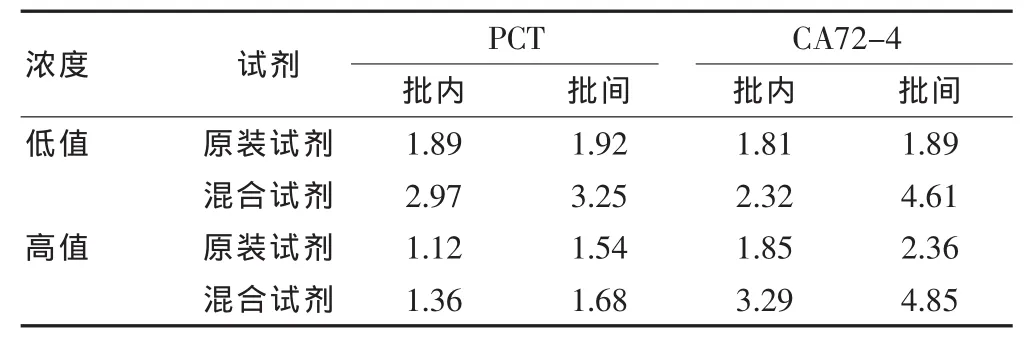
表1 原装与混合试剂检测质控血清PCT、CA72-4批内、批间CV的比较(%)
2.3.2 混合试剂准确性检测结果 混合试剂测得PCT、CA72-4低、高浓度质控物各20次结果与靶值结果比较,PCT、CA72-4其20次结果均在质控允许范围内,经单样本t检验,两项目各浓度测定值差异无统计学意义(P>0.05)(表 2)。
表2 混合试剂准确性检测结果

表2 混合试剂准确性检测结果
?
2.3.3 原装试剂与混合试剂检测血清样本结果 原装新试剂与混合试剂检测80例血清样本的PCT、CA72-4的结果相关系数(r)分别为0.998、0.997,两种试剂测定结果经配对样本t检验,差异无统计学意义(P均 >0.05)(表3)。
表3 80例标本原装试剂与混合试剂检测血清PCT、CA72-4结果

表3 80例标本原装试剂与混合试剂检测血清PCT、CA72-4结果
?
2.3.4 混合试剂回收试验结果 PCT、CA72-4的低值回收率分别是96.3%、101.5%,PCT、CA72-4的高值回收率分别是96.8%、105.9%。
2.3.5 混合试剂稳定检测结果 低、高值质控品21次检测结果有均在允许范围之内,未出现失控,经单样本t检验,两项目各浓度测定值差异无统计学意义(P>0.05)(表4)。
3 讨论
罗氏E170电化学发光免疫分析仪克服了放射免疫分析试剂有效期短和辐射污染、酶联免疫吸附试验易受温度、酸碱度变化的影响,以及化学发光免疫分析技术中发光分子只能利用一次的缺点,分析过程可通过电场精确控制,因此具有特异性好、灵敏度高、线性测定范围宽、操作的自动化程度高等优点[3],国内外均有文献对其综合性能进行了分析并给予较高评价[4-6]。
表4 混合试剂准确性检测结果

表4 混合试剂准确性检测结果
?
罗氏E170电化学发光试剂为专用试剂,每套试剂条码记录为100个测试,当检测了100个样本后,仪器即默认该套试剂为“零”个测试,试剂瓶内虽有残余试剂,但仪器不会再进行检测。经2年多实践观察,每套试剂残余量约为25%,与文献报道的每套试剂有20%~30%的试剂剩余量相近,因此弃之不用,造成较大浪费[7]。
本研究结果显示,对混合的残余试剂进行21 d监控,PCT、CA72-4两项目高、低水平质控物测定结果均在控,两项目各浓度差异无统计学意义,说明混合试剂3周内有较好的稳定性;混合试剂检测质控物PCT、CA72-4两项目的精密度、准确性、回收率等实验性能指标均符合相关实验要求,新试剂与混合试剂检测患者血清样本的PCT、CA72-4的结果相关性良好,且测定结果差异无统计学意义,说明混合试剂性能稳定,检测质量可靠。实践工作中应注意每盒试剂的稳定期,罗氏E170试剂盒开封后2~8℃可稳定12周,放在E170免疫分析仪上4周,如置20~25℃约为20 h。因此,检测完毕后,试剂尽快放入4℃冰箱保存,盖紧试剂瓶,防止试剂水分蒸发,造成变质。同一项目、同一批号的混合残余试剂在一定时间内检测结果可靠,残余试剂在4周内尽快再利用[8]。残余试剂混合再利用检测前应先进行定标,检测时设置高、低水平质控在检测前、中、后进行严密监控,在定标曲线合格和质控都在控的情况下测定结果方为有效。实践证明E170试剂盒的残余试剂混合再利用,操作简便可行、稳定性好、测定结果可靠,能节约1/4检测成本,减少医学资源浪费。
[1]吕世静.临床免疫学检验[M].2版.北京:中国医药科技出版社,2010:122.
[2]张葵.定量检测系统方法学性能验证实验的基本方法[J].临床检验杂志,2009,27(5):321-323.
[3]叶应妩,王毓三,申子瑜,等.全国临床检验操作规程[M].3版.南京:东南大学出版社,2006:575.
[4]Bieglmayer C,Chan DW,Sokoll L,et al.Multicentre performance evaluation of the E170 module for modular analytics[J].Clin Chem Lab Med,2004,42(10):186-202.
[5]谭浩.电化学发光免疫分析系统E170的应用评价[J].实用预防医学,2011,18(3):527-528.
[6]张学平,陈晓萍,张萍,等.利用空的试剂盒节约试剂的方法[J].实用医技杂志,2008,15(24):3202-3203.
[7]潘永康,何炯.Roche E170电化学发光仪开源节流三法[J].检验医学与临床,2008,24(5):1531.
[8]李炎梅,莫思健,梁太英,等.ACCESS化学发光仪残余试剂的回收方法及临床应用[J].中国临床新医学,2012,5(11):1012-1014.
