掺铁钨酸铋的制备及光催化降解罗丹明B的研究
2013-05-22王春英江桐桐秦晓海
王春英, 江桐桐, 周 丹, 刘 俊, 秦晓海
(江西理工大学资源与环境工程学院,江西 赣州341000)
自1990年Verwey等[1]最先发现在半导体中掺杂不同价态的金属离子可改变材料的催化性能后,人们对金属离子掺杂半导体光催化剂的研究也越来越多.目前研究最广的是金属离子掺杂TiO2,但由于TiO2带隙宽度为3.2 eV,且仅在紫外光照射下响应,对太阳能的利用率很低[2-3].而钨酸铋(Bi2WO6)作为其中一种具有可见光活性的新型半导体光催化剂[4],近年来得到了广泛的关注.文中通过水热合成掺铁Bi2WO6,讨论其在可见光辐射下降解有机染料罗丹明B的最佳条件及其降解机理.
1 实验
(1)实验试剂:硝酸铋 Bi(NO3)3·5H2O,钨酸钠Na2WO4·2H2O,氢氧化钠 NaOH,硝酸铁 Fe(NO3)3·9H2O,硝酸HNO3,罗丹明B,无水乙醇,以上试剂均为分析纯.
(2)实验仪器:UV-2100 Spectrophotometer(尤尼柯上海仪器有限公司),PHS-3C型pH计 (上海精密科学仪器有限公司),800型离心沉淀器(上海手术器械十厂),卤钨灯(500W,江苏连云港悦然照明有限公司),自组装光催化反应装置.
(3)催化剂制备与表征.催化剂的制备:首先,以 2∶1 的摩尔比将 Bi(NO3)3·5H2O 和 Na2WO4·2H2O分别溶解于稀HNO3和NaOH溶液中;其次,取一定量的 Fe(NO3)3·9H2O 溶液到 20 mL的 Bi(NO3)3·5H2O溶液中,并将20 mL Na2WO4·2H2O溶液逐滴加入到Bi(NO3)3·5H2O和Fe(NO3)3的混合溶液中,整个过程始终保持磁力搅拌,滴定完成后继续磁力搅拌10min,超声30 min后,调节前驱体溶液的pH值;然后,将前躯体溶液转移到有聚四氟乙烯内衬的不锈钢水热釜(50mL)中密封,并于140℃水热反应20 h;最后,将离心分离得到的固体样品在120℃干燥4 h后备用.不同掺铁量、不同水热合成溶液pH的钨酸铋催化剂得以制备.催化剂的制备实验过程中反应控制条件:制备pH分别为1.2、4、7、10;掺铁量 0%、0.1%、0.5%、1%、5%、10%(均为摩尔比).
催化剂的表征:通过场发射扫描电子显微镜(TMP,XL30W,荷兰飞利浦)分析合成材料的形貌;采用X射线射仪(XRD,型号为SMART APEXⅡ,德国布鲁克AXS公司)分析样品物相;制备材料的吸光性能通过紫外-可见光漫反射仪(UV-vis,型号为UV-2550,日本岛津公司)测定.
(4)光催化实验.将制备好的光催化剂加到100mL浓度为10mg/L的罗丹明B溶液中,并充分搅拌.为确保罗丹明B在催化剂上达到吸附-脱附平衡,光照之前避光搅拌30min.开灯后,每隔一定的时间取反应溶液5mL,用离心机离去悬浮液中的催化剂,采用分光光度计于554 nm处测上清液的吸光度.罗丹明B的降解率R按照(1)式计算:

根据一级动力学关系式计算罗丹明B的光催化降解速率[5]:

式(2)中:t为反应时间;C为反应t时刻溶液中罗丹明B浓度;C0为罗丹明B的初始浓度;k为反应速率常数.
光催化实验的反应控制变量条件:催化剂的投加量 0.01 g、0.05 g、0.1 g、0.2 g、0.4 g; 反应溶液的初始 pH 值 2.93、6.87、9.21、11.12.
2 实验结果与讨论
(1)催化剂表征结果.图1是制备pH=10,未掺铁和掺铁量为0.5%水热合成的Bi2WO6催化剂的XRD图谱.由图1可知,在制备pH=10下,未掺铁和掺铁量为0.5%条件下合成催化剂的各衍射峰位置与Bi2WO6标准卡片(图1下部)吻合,说明所合成的催化剂为钨铋矿结构的Bi2WO6.但是在掺铁Bi2WO6的衍射图中并没有发现Fe元素的衍射峰,可能的是由于Fe的掺杂量较少的缘故.

在140℃、pH=10条件下,水热合成的未掺铁和掺铁0.5%Bi2WO6催化剂粉末的扫描电镜(SEM)结果如图2所示,两种样品均主要呈片层状或球状结构,两种样品片层尺寸差别不大,粒径尺寸为20~25μm,即掺铁后催化剂形貌没有发生明显变化.

图3是制备pH=10,掺铁量为0.5%的Bi2WO6催化剂的紫外-可见漫反射光谱图.最大吸收波长λ0通过切线法确定,λ0≈460 nm.将其代入方程式(3)计算光催化剂的禁带宽度:

式(3)中:λ0为最大吸收波长;Eg为禁带宽度.经过计算,得出制备pH=10,掺铁量为0.5%的Bi2WO6的禁带宽度约为2.70 eV,相对于纯的Bi2WO6(Eg=2.76)[6],禁带宽度下降,最大吸收波长红移,铁的掺杂拓宽了在可见光区的吸收范围.催化剂为浅黄色,与其在460 nm左右吸收波段相吻合.
(2)水热合成pH对罗丹明B光催化降解的影响.不同制备pH下的催化剂对罗丹明B光降解率随时间的变化关系如图4.
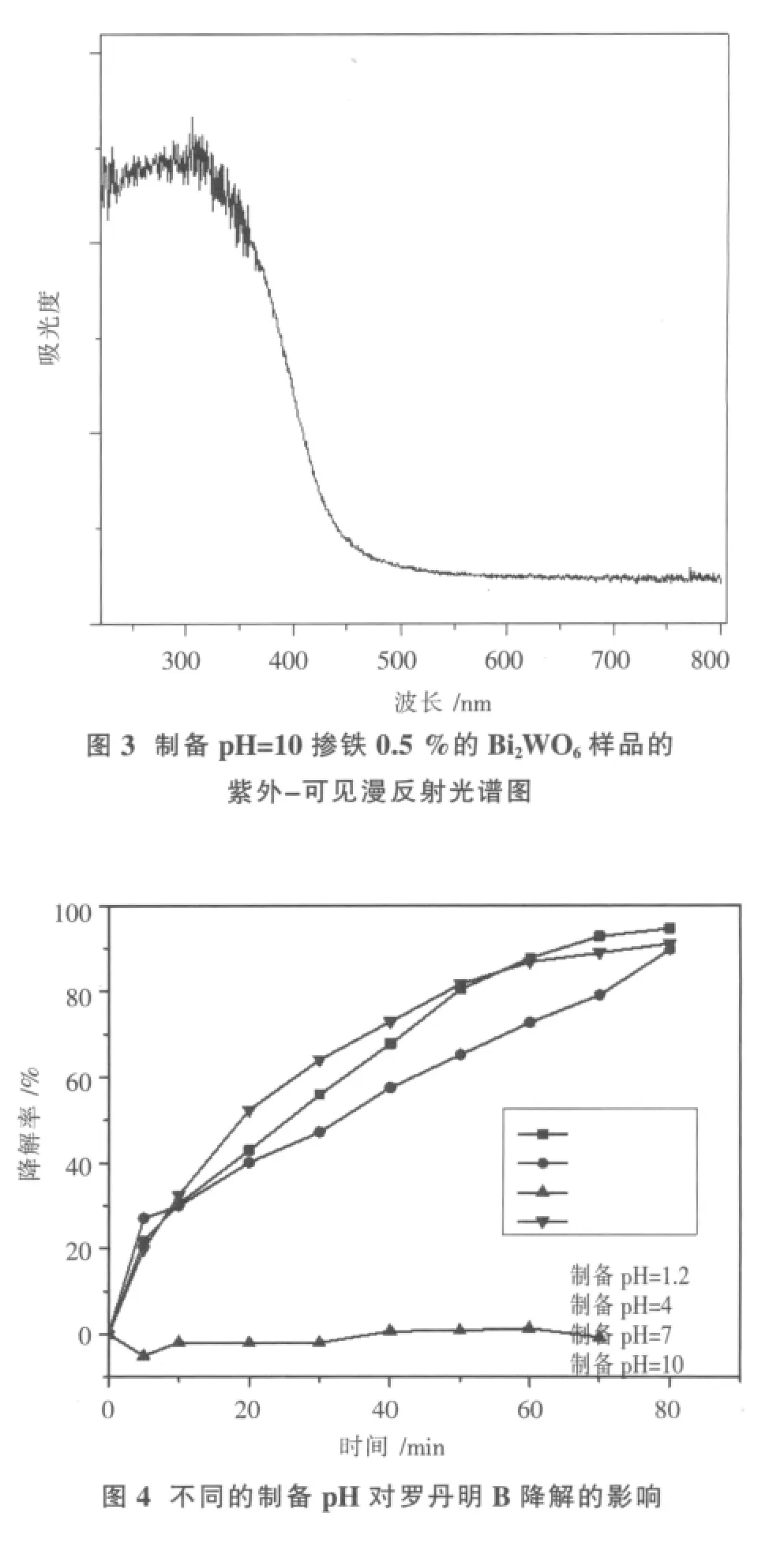
从图4中可以看出:在酸性或者碱性条件下,水热合成的掺铁Bi2WO6对罗丹明B均具有良好的降解活性,吸附30 min,光照80 min后,罗丹明B降解率可达到90%;在中性(pH=7)条件下制备的掺铁Bi2WO6对罗丹明B几乎没有降解作用.
比表面积和结晶度等因素会影响催化剂的光催化活性.较大的比表面积能够提高催化剂的吸附能力,有利于降解反应的进行。在前期研究中发现,Bi2WO6催化剂的比表面积随pH增大而减小,则在pH=1.2时Bi2WO6具有较大的比表面积[6],故在水热合成pH=1.2时的Bi2WO6表现出较好的催化活性.另外,Bi2WO6催化剂的结晶度在pH值为4~10范围是随pH增大而增强[7].据报道,高结晶度可以减少电子-空穴对的复合率[8-9],从而促进光催化反应的进行.在水热合成pH=4~10范围内,结晶度可能是影响Bi2WO6光催化降解罗丹明B的主要因素,故pH=10为水热合成掺铁Bi2WO6催化剂同样具有较好的光催化活性.考虑到pH=10的掺铁Bi2WO6光催化降解罗丹明B较pH=1.2反应过程更符合一级反应动力学方程,故在文中后续实验中均选择水热合成pH=10条件下合成的掺铁Bi2WO6为催化剂进行光催化降解罗丹明B的反应.
(3)不同掺铁量合成催化剂对罗丹明B光催化降解的影响.金属离子的掺杂会在半导体光催化剂晶格中引入缺陷位置或者改变结晶度,从而在半导体光催化剂的带隙能级中引入缺陷能级或杂质能级从而拓宽半导体光催化剂对太阳光的光谱响应范围,提高对太阳光能的利用率[10].水热合成pH=10的不同掺铁量的Bi2WO6催化剂对罗丹明B光降解率随时间的变化关系如图5.
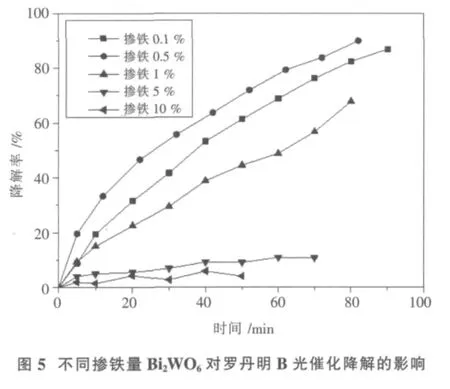
由图5可知:在掺铁量为0.5%时的Bi2WO6催化剂对罗丹明B表现出较好的降解性能,光照80 min后,罗丹明B降解率可达到90%;随着掺铁量从0.5%到10%的增加,催化活性相应的降低.说明金属离子的掺杂存在一个最佳掺杂量,而掺铁Bi2WO6的最佳掺杂量为0.5%.
(4)催化剂用量对罗丹明B光催化降解的影响.水热合成pH=10,掺铁量为0.5%的Bi2WO6催化剂不同用量与罗丹明B光降解率随时间的变化关系如图6.

从图6知:整体上,掺铁Bi2WO6对罗丹明B光降解速率随催化剂的投加量的增加而加快;但降解速率并不是一直随催化剂量的增加而提高;当催化剂的用量从2 g/L到4 g/L时,催化活性没有显著提高;催化剂用量为2 g/L时,光照80min后,罗丹明B降解率可达到90%.
产生上面的结果可能是由于:催化剂用量较小的情况下,溶液中的光催化活性点位随着催化剂用量的增加而增多,从而吸收更多的光子,使降解率增大;当催化剂加入量继续增加,溶液浊度提高,造成光散射,催化剂接受的光量子数减少,使得生成的电子-空穴对数目减少[11],光催化活性点位相应降低.并且催化剂用量由2 g/L增至4 g/L,罗丹明B降解率增加不明显.因此,选择催化剂的最佳投加浓度为2 g/L.
(5)反应溶液pH值对罗丹明B光催化降解的影响.不同光催化反应溶液pH下,水热合成pH=10,掺铁量为0.5%Bi2WO6对罗丹明B光降解速率随时间的变化如图7.

溶液在碱性范围内,催化剂对罗丹明B几乎没有降解能力,在酸性范围内催化剂的降解性能一般,而在中性条件下催化剂对罗丹明B表现出较好的降解能力,光照80min后,罗丹明B降解率可达到90%,说明中性条件下,罗丹明B更易被催化降解.
在强酸或强碱性环境下,掺铁Bi2WO6催化剂对罗丹明B的降解效果不佳.分析其原因,可能是由于酸性环境下Bi2WO6不稳定,易水解成H2WO4和Bi2O3[12],从而使催化剂有效的比表面积和活性点位降低,影响了其光催化活性.另外,强碱性溶液中存在的大量OH-,使催化剂表面带负电荷,同时罗丹明B上的羟基发生离解,大多以负离子存在,由于同电相斥,从而阻碍了光催化降解反应的进行.
(6)罗丹明B的光催化降解动力学.水热合成pH、掺铁量、反应溶液pH为降解的最佳值时,掺铁0.5%Bi2WO6光催化降降罗丹明B光催化降解罗丹明B的一级反应方程曲线如图8.
以光照射前后浓度比值的对数(1n(C0/C))对照射时间t(min)作图,其结果如图8.
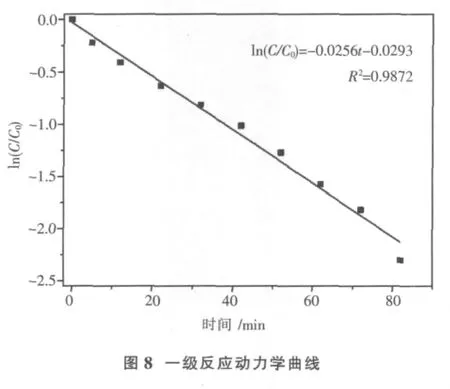
从图8可见,1n(C/C0)与t关线性关系良好,表明罗丹明B光催化降解反应符合一级反应动力学.直线的斜率为表观反应速率常数,故该实验条件下,掺铁Bi2WO6光催化降解罗丹明B的速率常数k=0.0256 min-1,光催化反应的半衰期t1/2为27.1min.
3 掺铁Bi2WO6光催化降解罗丹明B机理研究
以0.1 g水热合成pH=10条件下制备的掺铁量为0.5%Bi2WO6为催化剂对100mL10mg/L的罗丹明B溶液进行光催化降解,避光搅拌30min,开灯光照后,分别在 0min、11min、22min、42min、62min、82 min、102 min、122 min、152 min 取 5 mL 水样进行分析.不同时间点的水样在200~800 nm的紫外-可见吸收波谱见图9.

从图9可知,随着反应时间的进行罗丹明B溶液的吸光度迅速降低,且吸收峰的位置发生了蓝移(554 nm→500 nm),推测其可能的原因有两方面:①由于反应溶液在降解过程中pH发生了变化,pH会影响溶液的最大吸收波峰的波长;②随着反应的进行,罗丹明B在被降解的过程结构发生变化,产生了新的物质.
反应过程中溶液的pH的变化范围为6~8.而通过实验对pH=3~11范围内的罗丹明B初始溶液进行光谱扫描可知:在pH=6~8范围内的罗丹明B的最大吸收峰的波长基本是处在554 nm左右,没有发生位移.故反应溶液pH发生变化不可能导致最大吸收峰的蓝移.有研究表明罗丹明B在降解过程中发生吸收峰的蓝移是由脱乙基反应所致[13-15].刘华俊[13]和尹京花[16]均通过质谱分析证明罗丹明B被降解吸收峰发生蓝移的溶液中有脱乙基产物存在。因此,推测掺铁Bi2WO6对罗丹明B降解反应中以脱乙基反应为主,随着时间的推移,吸收峰值迅速降低,说明这些脱乙基产物生成后进一步被掺铁Bi2WO6光催化降解.
4 实验结论
(1)应用水热合成法,通过调节水热合成溶液的pH值制备掺铁Bi2WO6.在pH=10、掺铁量为0.5%的条件下催化剂对罗丹明B具有最好的光催化活性.
(2)催化剂的投加量以及光降解体系的初始pH值对掺铁Bi2WO6光催化降解罗丹明B具有重要的影响:本次实验中,最优的添加量为2 g/L;而罗丹明B降解的最适的反应溶液pH为中性.
(3)掺铁Bi2WO6光催化降解罗丹明B的最佳反应条件:制备pH=10、掺铁量为0.5%、反应溶液pH=6.86,反应80 min后,罗丹明B的去除率可达90%,且反应符合一级动力方程.
(4)通过对不同降解时段溶液的紫外-可见吸收波普全扫描分析,推测掺铁Bi2WO6对罗丹明B的降解以脱乙基反应为主.
[1]Ileperuma O A,Tennakone K,Dissanayake W D D P.Photocatalyticbehaviourofmetaldoped titanium dioxide:studieson the photochemicalsynthesis of ammonia on Mg/TiO2catalyst systems[J].Appl.Cata.,1990,62(1):L1-L5.
[2]Lin L,Lin W J,Xie L,et al.Photocatalytic properties of phosphordoped titania nanopartides[J].Appl.Catal.B.,2007(75):52.
[3]Hagfeldt A,Gratzel M.Light-induced reactions in nanocrystallines systems[J].Chem.Rev.,1995(95):49.
[4]Zhang C,Zhu Y F.Synthesis of square Bi2WO6nanoplates as high-activity visible-light-driven photocatalysts[J].Chem.Mater.,2005,17(13):3537-3545.
[5]余长林,杨 凯,Yu Jimmy C,等.水热合成Bi2WO6/ZnO异质结型光催化剂及其光催化性能[J].无机材料学报,2011,26(11):1-6.
[6]王淑兰,梁英教.物理化学[M].北京:冶金工业出版社,2008.
[7]Wang C Y,Zhang H,Li F,et.al.Degradation and mineralization of bisphenol A by mesoporous Bi2WO6under simulated solar light irradiation[J].Environ.Sci.Technol,2010,44(17):6843-6848.
[8]Ikeda S,Sugiyama N,Murakami S,et al.Quantitative analysis of defective sites in titanium (IV)oxide photocatalyst powders[J].Chem.Phys.,2003,5(4):778-783.
[9]Ohtani B,Bowman R M,Colombo Jr,et al.Femtosecond diffuse reflectance spec-troscopy of aqueous Titanium (IV)Oxide suspension:Correlation of electron-hole recombination kinetics with photocatalytic activity[J].Chem.Lett.,1998,27(7):579-580.
[10]张国强.金属掺杂TiO2以及钨酸铋的制备、表征及其光催化性能研究[D].济南:山东大学,2010.
[11]邓 沁,肖新颜,廖东亮,等.TiO2薄膜光催化降解甲基橙反应动力学研究[J].精细化工,2003,20(12):721-723.
[12]Fu H,Pan C,Yao W,et al.Visible-light-induced degradation of Rhodamine B by nanosized Bi2WO6[J].J.Phys.Chem.B.,2005,109(47):22432-22439.
[13]刘华俊,彭天右,彭正合,等.Dy/WO3光催化降解罗丹明B的反应机理[J].武汉大学学报:理学版,2007,53:129-130.
[14]付宏刚,王建强,任志宇,等.Fe3+-TiO2/SiO2薄膜催化剂的结构对其光催化性能的影响[J].高等学校化学学报,2003,24(9):1671-1676.
[15]Shiragami T,Fukami S,Waka Y J,et al.Semiconductor photocatalysis:Effect of light intensity on nano scade CdS-catalyzed photolysis of organic subst-rates[J].J.Phys.Chem.,1993,97(49):12882-12887.
[16]尹京花,赵莲花,崔胜云,等.掺铁二氧化钛光催化氧化罗丹明B溶液的反应机理初探[J].延边大学学报:自然科学版,2005,31(2):115-117.
