钯催化的有机卤化物的1,2-加成反应研究进展
2013-05-22陈程吴良葛晨叶仕春贾义霞高建荣
陈程 吴良 葛晨 叶仕春 贾义霞 高建荣
(浙江工业大学化学工程与材料学院,浙江 杭州 310032)
0 前言
传统有机合成中,Grignard反应[1]一直是构建碳-碳键的一类重要方法。反应中涉及的格氏试剂对水氧敏感,活泼不易制备同时无法引入敏感性基团,使该方法的应用存在一定局限性。上世纪70年代发展的Nozaki-Hiyama-Kishi(NHK)反应[2],通过卤代烃与二氯化铬现场生成有机铬试剂,然后对醛发生亲核加成,有效地避免了格氏反应中活泼有机金属试剂的制备过程,简化了操作的同时提高了底物官能团的适应性。然而,反应中使用的高毒性铬盐对环境造成很大压力,并且反应局限于醛类底物,限制了该反应的进一步发展。因此,发展高效、绿色的卤代烃对碳-杂原子重键的1,2-加成反应具有重要的科学意义。
近年来,在过渡金属催化研究领域,通过卤代烃与钯催化剂发生氧化加成获得的有机钯中间体,可作为亲电组分与一系列亲核性有机金属试剂发生Kumada-Corriu、Negishi、Stille、Suzuki 及Hiyama等偶联反应[2]。而有机钯中间体与亲电试剂反应的研究很少,主要是因为有机钯中间体的极性较小,亲核性不强。尽管如此,该类反应研究依然得到了一定的发展,本文以亲电试剂类型进行分类对研究进展进行总结。
1 以醛酮为亲电试剂
1999年,Yamamoto小组在醋酸钯催化下,以醇类为还原剂,实现了邻溴芳醛[3](酮[4])与炔的环合反应,以较高的收率获得了一系列茚醇产物。反应中,芳基溴化物与零价钯进行氧化加成后对炔烃进行插入反应,获得烯基钯中间体1,通过1对羰基的亲核加成,以及随后与醇的质子交换以及还原消除反应,最终获得目标产物并完成催化循环(Eq.1)。

2000年,Gai等人[5]将反应拓展到联烯底物,以环钯络合物2为催化剂,实现了烯基钯中间体对醛酮的分子内亲核加成反应,高收率的获得了一系列环戊醇化合物(Eq.2)。

同年,Yamamoto小组[6]报道了钯催化下芳基溴化物对酮的分子内直接亲核加成反应,发展了合成苯并环戊醇类化合物的新方法(Eq.3)。值得一提的是,醛类底物3的反应得到复杂的混合物,而邻位无取代的酮类底物4则不发生反应。

2010年,Kundig小组[7]在 Pd/PtBu3催化体系下,以正丁醇为还原剂,实现了分子内溴苯对酰胺酮的亲核加成反应,高收率的获得了重要的药物及生物活性中间体3-羟基-2-吲哚酮类化合物(Eq.4)。

2011年,Shibasaki小组[8]通过手性配体(R)-DifluroPhos的引入,实现了分子内芳基三氟甲磺酸酯对酰胺酮的分子内不对称亲核加成反应,合成了一系列手性3-羟基-2-吲哚酮类化合物,ee值最高达99%(Eq.5)。首次实现了钯催化下芳基(类)卤化物对羰基的不对称亲核加成反应。值得一提的是,当酰胺氮上有取代基时,相应反应产物的ee值非常低。

2 以羧酸衍生物为亲电试剂
相比于醛酮,羧酸衍生物的亲电性较弱。2007 年,Sole 小组[9]在甲苯中以 Pd(PPh3)4为催化剂,三乙胺作碱,在回流条件下实现了芳基碘化物对酯基的分子内亲核取代反应,较高收率的获得了一系列苯并环己酮类产物(Eq.6)。反应中,碱起很关键的作用。当采用碳酸铯作碱时,反应获得脱卤产物;而以苯酚钾作碱时,底物中酯基倾向于发生烯醇互变,抑制了亲核取代反应,更有利于发生酯基α-芳基化反应。随后,该小组成功地将该反应拓展至相应的酰胺底物[10](Eq.7)中。

Cacchi等人[11]在N,N-二甲基甲酰胺溶剂中,以氯化锂为添加剂,实现了钯催化的芳基碘化物对乙酸酐的亲核取代反应。该反应对一系列官能化的碘苯均能适用,从而为合成含敏感性基团的取代苯乙酮提供了一种直接有效的方法(Eq.8)。当芳基碘化物中含有中性、弱吸电子性以及弱供电子性基团时,反应均可高收率地获得相应的取代苯乙酮产物,而当含有强供电子基团时,收率中等。

3 以碳氮重键化合物为亲电试剂
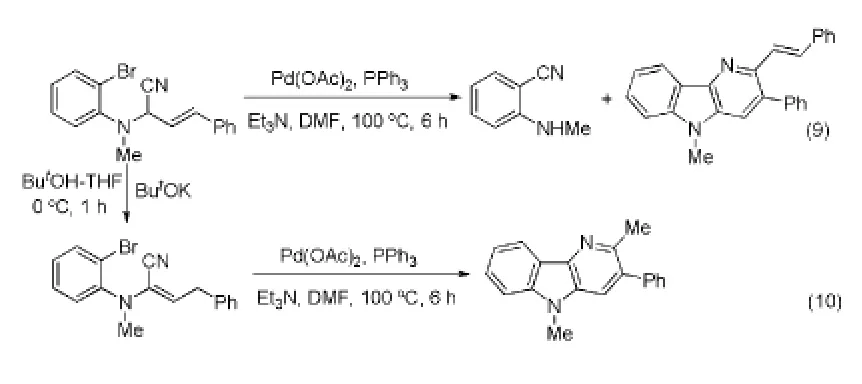
1994年,Yang等人[12]在N,N-二甲基甲酰胺溶剂中,在Pd(OAc)2/PPh3催化体系下,以三乙胺作碱,实现了芳基溴化物对烯丙基腈的亲核加成反应,在获得亚胺中间体后继续发生环合反应,最终得到Υ-咔啉产物以及邻腈基苯甲胺副产物(Eq.9)。随后作者在0℃条件下,以叔丁醇钾为碱,将烯丙基腈底物转化为相应的烯基腈底物,在上述催化体系中成功实现区域选择性的环化反应,以88%的收率获得相应的咔啉产物(Eq.10)。
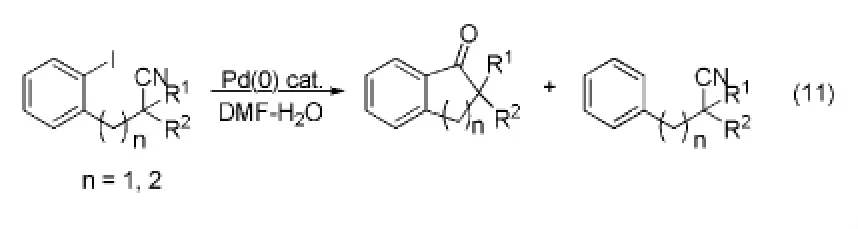
2002年,Larock[13]小组以ω-2-碘芳基烷基腈为底物,在钯催化下实现了芳基碘对腈基的直接亲核加成反应,体系中水的存在使加成产物亚胺即刻水解成相应的目标产物,为苯并环酮类化合物的合成提供了新方法(Eq.11)。
同年,该小组[14]以邻碘苯腈为底物,在钯催化下和炔发生环和反应,高收率的获得了一系列茚酮产物(Eq.12)。该反应中邻碘苯腈在钯催化下首先与炔发生插入反应,获得烯基钯中间体,随后对腈基实现分子内亲核加成,得到相应的亚胺中间体5,最后水解获得目标产物。当该反应拓展至邻碘苯乙腈底物时,可以获得β-萘胺类化合物(Eq.13)。

此外,通过添加正丁基氯化铵,上述反应底物可以从炔烃拓展至桥环烯烃[15],高收率的获得相应的二氢茚酮产物(Eq.14)。

2011年,李金恒课题组[16]通过钯催化下叔胺和芳基碘的氧化偶联反应合成了一系列烷基芳酮化合物(Eq.15)。该反应首次利用叔胺作酰基源,发展了合成取代烷基芳基酮类化合物的新方法。
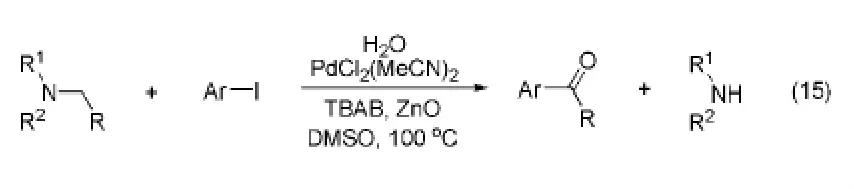
2012年,Ley小组[17]在钯催化下,以(R)-DifluroPhos为手性配体,实现了分子内芳基甲磺酸酯对酰胺亚胺的分子内不对称亲核加成反应,合成了一系列手性3-胺基吲哚酮(Eq.16)。反应中,底物中亚胺芳基上的取代基对产物的ee值有很大影响,当芳基上含吸电子基团或中性基团时,反应获得很高的ee值,而含供电子基团时,产物ee值仅中等。尽管如此,该反应为手性3-胺基吲哚酮的合成打开了新的思路。

4 以二氧化碳为亲电试剂
Martin小组[18]通过配体调控以及还原剂的筛选,实现了钯催化下芳基溴化物对二氧化碳的分子间亲核加成反应,较高收率的获得了一系列芳基甲酸(Eq.17),提供了一种简单、直接的制备芳基甲酸的新办法。

5 结论
综上所述,钯催化下卤代烃对碳-杂原子重键化合物的1,2-加成反应不但可以有效避免活泼有机金属试剂的制备,简化合成,提高底物官能团的适应性,而且通过采用合适的还原剂(如醇、有机胺等)可以有效减少废弃物的产生和排放,符合绿色化学的发展要求,具有良好的发展和应用前景。尽管目前该类研究仍属于一个新兴领域,但相信其在有机合成中会有越来越重要的应用。
[1]Grignard V.Some new organometallic combinations of magnesium and their application to the synthesis of alcohols and hydrocarbons[J].C.R.Acad.Sci.,1900,1322-1324.
[2]Li,Jack J.有机人名反应及机理[M].上海:华东理工大学出版社,2003,9.
[3]Gevorgyan V,Quan L G,Yamamoto Y.Synthesis of indenols and indanones via catalytic cyclic vinylpalladation of aromatic aldehydes[J].Tetrahedron Lett.,1999,40:4089-4092.
[4]Quan L G,Gevorgyan V,Yamamoto Y.Intramolecular nucleophilic addition of vinylpalladiums to aryl ketones[J].J.Am.Chem.Soc.,1999,121:3545-3546.
[5]Gai X J,Grigg R,Collard S.Palladium catalyzed intramolecular nucleophilic addition of allylic species,generated from allene,to aryl aldehydes and ketones[J].Chem.Commun.,2000,1765-1766.
[6]Quan L G,Lamrani M,Yamamoto Y.Intramolecular nucleophilic addition of aryl bromides to ketones catalyzed by palladium[J].J.Am.Chem.Soc.,2000,122:4827-4828.
[7]Jia Y X,Katayev D,Kundig E P.Synthesis of 3-hydroxyoxindoles by Pd-catalysed intramolecular nucleophilic addition of aryl halides to α-ketoamides[J].Chem.Commun.,2010,130-132.
[8]Yin L,Kanai M,Shibasaki M.A facile pathway to enantiomerically enriched 3-hydroxy-2-oxindoles:asymmetric intramolecular arylation of α-keto amides catalyzed by a palladium-difluorphos complex[J].Angew.Chem.,2011,123:7762-7765.
[9]Sole D,Serrano O.Palladium-catalyzed intramolecular nucleophilic substitution at the alkoxycarbonyl group[J].Angew.Chem.,Int.Ed.,2007,46:7270-7272.
[10]Sole D,Serrano O.Intramolecular Pd(0)-catalyzed reactions of β-(2-Iodoanilino)carboxamides:enolate arylation and nucleophilic substitution at the carboxamide group[J].J.Org.Chem.,2008,73:9372-9378.
[11]Cacchi S,Fabrizi G,Gavazza,F.Palladium-catalyzed reaction of aryl iodides with acetic anhydride.a carbon monoxide-free synthesis of acetophenones [J].Org.Lett.,2003,5:289-291.
[12]Yang C C,Sun P J,Fang J M.Palladium-catalysed regioselective cyclisation of unsaturated bromoanili noalkenenitriles[J].J.Chem.Soc.Chem.Comm.,1994,2629-2630.
[13]Pletnev A A,Larock R C.Carbopalladation of nitriles:synthesis of benzocyclic ketones and cyclopentenones via Pdcatalyzed cyclization of ω-(2-Iodoaryl)alkanenitriles and related compounds[J].J.Org.Chem.,2002,67:9428-9438.
[14]Larock R C,Tian Q P,Pletnev A A.Carbocycle synthesis via carbopalladation of nitriles[J].J.Am.Chem.Soc.,1999,121:3238-3239.
[15]Pletnev A A,Tian Q P,Larock R C.Carbopalladation of nitriles:synthesis of 2,3-diarylindenones and polycyclic aromatic ketones by the Pd-catalyzed annulation of alkynes and bicyclic alkenes by 2-iodoarenenitriles[J].J.Org.Chem.,2002,67:9276-9287.
[16]Liu Y,Yao B,Li J H,et al.Palladium-catalyzed oxidative coupling of trialkylamines with aryl iodides leading to alkyl aryl ketones[J].Org.Lett.,2011,13:2184-2187.
[17]Tolstoy P,Lee S X Y,Ley S V,et al.Synthesis of enantiomerically enriched 3-amino-2-oxindoles through a palladium-mediated asymmetric intramolecular arylation of α-ketimino amides[J].Org.Lett.,2012,14:4810-4813.
[18]Correa A,Martin R.Palladium-catalyzed direct carboxyla tion of aryl bromides with carbon dioxide[J].J.Am.Chem.Soc.,2009,131:15974-15975.
