近红外光谱法快速测定白芍中芍药苷含量
2013-05-17李小庆雷敬卫
白 雁,李小庆,雷敬卫
河南中医学院,郑州450046
白芍为毛茛科植物芍药Paeonia lactiflora Pall的干燥根,为我国临床常用传统中药,有养血柔肝、缓中止痛、敛阴收汗的功能[1],芍药苷(paeoniflorin,PF)是白芍的主要有效成分之一[2]。《中国药典》2010版已对白芍的质量控制做出明确的规定,在含量测定项中以芍药苷为指标,利用高效液相色谱法对其进行含量测定,但该法需对药材进行分离提取,耗时耗试剂,不适合中药的快速检测。近红外分析技术是一种二次分析技术,其光谱信息来源于有机物中含氢基团 X-H(X=C、O、N、S、P)振动的倍频和合频吸收,因此其谱带宽,组分之间谱带重叠现象严重,不能用于直接分析,而是综合多学科(光谱学、化学计量学和计算机等)知识的现代分析技术,具有快速、无损、可同时进行多项测定等优点。因此,本研究尝试用近红外建立芍药苷含量测定的新方法,对白芍中芍药苷进行快速分析,以满足中药现代化的需求。
1 仪器与材料
美国Thermo Nicolet 6700型傅立叶变换近红外光谱仪(漫反射积分球附件、OMNIC光谱采集软件和TQ8.0分析软件);Waters2695高效液相色谱仪(PDA2998紫外检测器);METTLER TOLEDO AL204万分之一分析天平(梅特勒-托利多仪器上海有限公司);HS-6150型超声波清洗器(500W,40 kHz,昆山市超声仪器有限公司);FW-200型高速药材粉碎机(北京中兴伟业仪器有限公司);CS101-2D电热鼓风干燥箱(上海实验仪器厂有限公司);乙腈、甲醇为色谱纯,水为市售纯净水。芍药苷对照品(批号:1107036-201035,供含量测定用)由河南省药检所提供;106份白芍样品由河南省宛西制药股份有限公司提供。
2 实验方法
2.1 近红外光谱数据的采集
将106份白芍样品粉碎过65目药典筛,每份样品取约8 g,混合均匀后放人石英样品杯中,摊平,然后以空气为参比,扣除背景,采集光谱图。采样方式:积分球漫反射;采集光谱范围:4000 cm-1~12000 cm-1;分辨率:8 cm-1;扫描次数:32次;温度:(25±2)℃;相对湿度:45% ~50%。每份样品扫描3次,求平均值作为样品的NIR光谱。
2.2 芍药苷含量的HPLC测定
参照2010版《中国药典》中白芍项下芍药苷含量测定中HPLC进行测定。色谱柱为Diamonsil C18(200 mm × 4.6 mm,5 μm),以乙腈-0.1% 磷酸溶液(14∶86)为流动相,检测波长230 nm,柱温25℃,流速1.0 mL/min,进样体积10μL,以保留时间定性,峰面积定量,外标法计算。每份样品平行做2次,以其平均值作为HPLC分析值。
2.3 芍药苷定量分析模型的建立
依据芍药苷的含量分布,从106份白芍样品中选择20个作为验证集,其余作为校正集,将验证集和校正集的NIR光谱与HPLC分析值相关联,输入到TQ8.0软件中,选择不同的光谱预处理方法,建模谱段以及主因字数建立定量校正模型,所建模型用相关系数(R2)和内部交叉验证均方差(RMSECV)来评价,R2越接近于1,RMSECV越小,表明模型结构越合理,其预测能力可通过预测均方差(RMSEP)来衡量,RMSEP越小,表明模型的预测性能和推广能力越强[3]。
3 结果与讨论
3.1 白芍样品NIR图谱的采集
106份白芍样品的近红外光谱叠加图见图1。
3.2 白芍样品的芍药苷含量测定
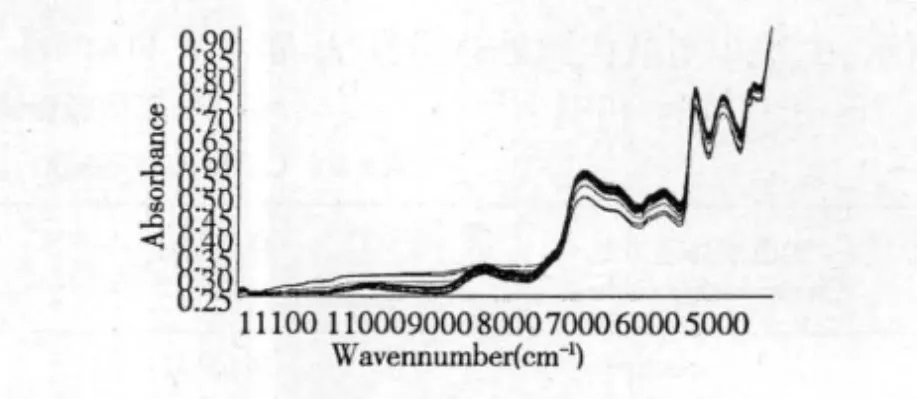
图1 106份白芍样品的近红外光谱叠加图Fig.1 NIRS spectra of106 Paeoniae Radix Alba samples
按2.3项下的方法对106份白芍样品中芍药苷含量进行了测定,其含量范围为1.32% ~3.49%,并以此值作为建立近红外模型的真实值。
3.3 白芍中芍药苷定量校正模型的建立
3.3.1 校正集和验证集的选择
运用TQ8.0定量分析软件中PLS法建立模型。根据白芍样品中芍药苷含量分布情况,从106份白芍样品中选择86个样品作为校正集,20个样品作为验证集。为使校正集样品更具代表性,验证集样品的芍药苷含量应在校正集含量范围之内[4],见表1。

表1 校正集与验证集中芍药苷含量分布Table 1 Concentration distribution of paeoniflorin of calibration set and validation set
3.3.2 光谱预处理方法、光谱范围及主因子数的选择
在建立模型前,首先对样品的原始吸收光谱进行预处理。本实验进行的是粉末样品的NIR漫反射采集,由于样品颗粒尺寸、均匀性等的影响,光程无法保持恒定,不利于建模时有效信息的提取,因此本实验用标准正则变换(SNV)和多元散射校正(MSC)来对光谱进行处理,以消除这些因素的干扰。导数处理是净化图谱、消除光谱偏移或漂移的常用方法,可根据需要进行一阶导数(First Derivative)和二阶导数(Second Derivative)处理。但导数处理在消除基线偏移的同时,也放大和分离了重叠的信息,放大了噪声信号,因此,在对光谱进行微分处理时,需对光谱进行平滑处理,常用的平滑的处理方法有Savitzky-Golay滤波和Norris Derivative滤波。预处理方法对R2、RMSECV及RMSEP的影响如表2所示,由表2知最优预处理方法为MSC+First De- rivative+SG。

表2 不同预处理方法对校正模型影响Table 2 Calibration results with different preprocessingmethods
手动优选最佳波段,辅以R2、RMSECV及RMSEP作为模型性能的评价指标。通过比较,确定4014.56 ~ 7503.91 cm-1为最佳波段,如表3所示。

表3 不同建模区间对模型性能的影响Table 3 The effect of different spectral regions onmodel performance

图2 主因子数对模型RMSECV的影响Fig.2 The RMSECV value with differentmain factors
本文采用交互验证法考察主因子数对RMSECV的影响(图2),当RMSECV最小时,所选主因子数最佳[5],由图2知最佳主因子数为11,此时 RMSECV=0.33068。
3.3.3 白芍中芍药苷定量模型的建立
采用以上确定的最优条件,即106份白芍样品的近红外光谱经过MSC+FirstDerivative+SG处理后,在 4014.56 ~ 7503.91 cm-1波段范围内,选择前11个主成分建立最优校正模型,NIR预测值与参考值相关图见图3,偏差图见图4。由图知,该模型R2=0.99395,RMSECV 及 RMSEP 分别为 0.33068、0.0756,可以看出NIR预测值与参考值非常接近。
Vol.25 白 雁等:近红外光谱法快速测定白芍中芍药苷含量36 1

图3 芍药苷的NIRS预测值与真实值的相关图Fig.3 Correlation between NIR predicted value and actual value

图4 NIR预测值与真实值偏差图Fig.4 Deviation between NIR predicted value and actual value
3.4 芍药苷定量模型的内部验证
将20份验证集样品的NIR图谱输入定量分析模型,预测其芍药苷含量,并与其HPLC测得值进行比较,结果见表4。

表4 NIR预测值与HPLC测定值的比较Table 4 Comparison of NIR predicted value and actual value
由表4知,最大绝对偏差0.17%,以验证集样品的NIR预测值与HPLC测定值的比值作为预测回收率,所得平均回收率100.07%,结果表明,利用近红外光谱技术测定白芍药材中芍药苷的含量是可行的。
3.5 统计学检验
将20份验证集样品的NIR预测值与HPLC测得值进行配对t检验,结果,t=-1.44,双侧P=0.887 >0.05,按 α =0.05 水准不拒绝H0,差异无统计学意义,即2种方法的分析结果差异无统计学意义,该模型可以准确预测其覆盖范围内的白芍药材中芍药苷含量。
3.6 讨论
NIR定量模型的反复优化过程中,性能指数(Performance Index,PI)即相对残差和是确定最优模型的一个重要参数,最大值是100,越接近100表明所建模型精度越好。在3.2项预处理方法选择中,预处理方法为MSC+ First Derivative时R2=0.99425为最高,预处理方法为MSC+First Derivative+SG时RMSECV和RMSEP为最低,无法确定最优模型。而预处理方法为MSC+First Derivative时模型的PI为86.9低于预处理方法为MSC+First Derivative+SG时的87.3,因此,确定最优的光谱预处理方法为MSC+First Derivative+SG。
本实验将NIRS与PLS相结合,建立了白芍中芍药苷定量校正模型,该模型的R2=0.99395,RMSECV 及 RMSEC 分别为0.33068、0.0563,预测均方差(RMSEP)和平均回收率分别为 0.0756和100.07%。表明该模型准确、可靠,可以准确预测其覆盖范围内的白芍药材中芍药苷含量。但该模型建模所用样本均由一个厂家提供,样品来源略显单一,因此,需要不断增加样品集数量,对模型进行再校正和优化,提高模型的适用性和稳健性,更好的应用于实际当中,以满足中药现代化的需求。
1 Chinese Pharmacopoeia Commission(国家药典委员会).Pharmacopoeia of the People’s Republic of China(中华人民共和国药典).Beijing:China Medical Science Press,2010,Vol I.97.
2 Sun LR(孙丽荣),Cao X(曹雄),Hou FQ(侯凤青),et al.Progressive studies of paeoniflorin.China J Chin Mat Med(中国中药杂志),2008,33:2028-2032.
3 Bai Y(白雁),Li S(李姗),Wang X(王星),et al.Determination of chlorogenic acid of honeysuckle by near-infrared spectroscopy rapidly.Chin J Exp Tradit Med Form(中国实验方剂学杂志),2011,17(5):66-69.
4 Zhang SN(章顺楠),Yang HL(杨海雷),Liu ZQ(刘占强),et al.On-line monitoring the contents of active components in the solution for Fufangdanshen dripping pills by near-infrared spectroscopy.JPharm Anal(药物分析杂志),2009,29:192.
5 Lu WZ(陆婉珍).Modern Near Infrared Spectroscopy Analytical Technology(现代近红外光谱分析技术).Beijing:China Petreochemical Press,2007.44.
