注射用替加环素的被动皮肤过敏性实验研究
2013-05-11黄巍唐灿由凤鸣
黄巍 唐灿 由凤鸣
(1.成都中医药大学 成都市 610074;2.西华大学 成都市 610039)
替加环素是全球首个被批准的用于静脉注射的甘氨酰环素类抗生素[1,2],其结构与四环素类药物相似。替加环素抗菌谱广,对有耐药性的耐甲氧西林金黄色葡萄球菌也有活性,2005年6月美国FDA批准该药应用于成人复杂皮肤及软组织感染和成人复杂的腹内感染,包括阑尾炎、烧伤感染、腹内脓肿、深部软组织感染及溃疡感染。
为了分析注射用替加环素的过敏性,我们采用了大鼠皮肤被动过敏试验(PCA)进行评价。
1 仪器与材料
1.1 仪器
BS600L电子天平(上海友声衡器有限公司);FA1004电子天平(上海良平仪器仪表有限公司);722S可见分光光度计(上海梭光技术有限公司);TDL-80-2B台式离心机(上海安亭科学仪器厂)。
1.2 试药
0.9 %氯化钠注射液(四川科伦药业股份有限公司,批号:M11120411,规格:500 ml);卵白蛋白(美国Sigma公司,批号:A-5252,规格:10 g);注射用替加环素(四川中兴药物有限公司,批号:20111201,规格:50 mg)。伊文思蓝(UNI-CHEM,批号:GD4061465);丙酮(成都市科龙化工试剂厂,批号:20080303,规格:500 ml);弗氏完全佐剂(sigma,批号:F5881,规格:10 ml);弗氏不完全佐剂(sigma,批号:F5506,规格:10 ml)。
1.3 动物
大鼠32只,体重180~220 g,雌性12只,雄性20只,均购于四川省实验动物专委会养殖场,生产许可证号:SCXK(川 )2008-14。
2 方法
2.1 溶液的制备
1)抗血清药物溶液的制备[3-5]:用0.9%氯化钠注射液配制成浓度10 mg/ml的卵白蛋白阳性对照组溶液和1.5 mg/ml、0.5 mg/ml的替加环素高、低剂量组溶液。
2)致敏溶液的制备:分别取4组抗血清,用0.9%氯化钠注射液稀释成1∶2、1∶4、1∶8的溶液。
3)激发溶液的制备:用0.5%伊文思蓝-0.9%氯化钠注射液配制成浓度1 mg/ml的卵白蛋白阳性对照组溶液和1.5 mg/ml、0.5 mg/ml的替加环素高、低剂量组溶液。
2.2 分组和给药方法
1)抗血清制备分组:8只雄性大鼠分别按体重分为阴性对照组(氯化钠注射液)、阳性对照组(卵白蛋白)和替加环素高、低剂量组,每组2只。
2)致敏和激发试验分组:取大鼠24只,雌雄各半,按体重分为阴性对照组、阳性对照组和替加环素高、低剂量组,每组6只。
3)抗血清制备方法:阴性对照组(0.9%氯化钠注射液)、阳性对照组(10 mg/ml卵白蛋白)、替加环素高剂量组(1.5 mg/ml)、替加环素低剂量组(0.5 mg/ml)4组大鼠分别腹腔注射相应药物1 ml/只,同时腹腔注射弗氏(完全/不完全)佐剂0.2 ml/只(首次注射使用弗氏完全佐剂,后两次注射使用弗氏不完全佐剂),隔日注射1次,共3次。末次注射后14 d,大鼠股动脉取血,分别收集4组的血液置于室温下,析出血清,离心(3 000 r/min,15 min)。在无菌条件下,吸出抗血清,各组抗血清分别混匀,-20 ℃冷冻保存。
4)致敏方法:致敏前将每只大鼠背部从头部沿尾部方向划分为3个区域,并用记号笔画一个直径为2 cm的圈作为标记,靠近头部的区域为1∶2稀释度区,中间的区域为1∶4稀释度区,靠近尾部的区域为1∶8稀释度区。各组分别于圈内皮内注射相应稀释度的抗血清0.1 ml。激发方法:致敏24 h后,阴性对照组(0.9%氯化钠注射液)、阳性对照组(1 mg/ml卵白蛋白)、替加环素高剂量组(1.5 mg/ml)、替加环素低剂量组(0.5 mg/ml)4组大鼠,分别尾静脉注射已加入伊文思蓝的相应药物1 ml/只进行激发。
2.3 观察指标
激发30 min后断头处死大鼠,剪取背部皮肤,分别测量皮肤内层3个区域的蓝斑大小,直径大于5 mm者判为阳性,不规则斑点的直径为长径与短径之和的1/2。将各蓝色斑皮片剪下,剪碎,分别加入丙酮-0.9%氯化钠注射液(7∶3)混合液5 ml,浸泡48 h,离心(2 000 r/min,20 min),取上清液测吸光度(波长610 nm)。
2.4 数据处理
采用Fisher精确检验法统计,计量资料采用t检验统计。P<0.05表示具有显著性差异。
3 结果
大鼠背部皮肤3个区域(1∶2稀释度,1∶4稀释度,1∶8稀释度)的蓝斑观察结果见表1。阳性对照各稀释组大鼠蓝斑直径均为阳性(P<0.001)。注射用替加环素高、低剂量各稀释组蓝斑直径均为阴性(P<0.001)。注射用替加环素对大鼠未产生被动皮肤过敏反应。
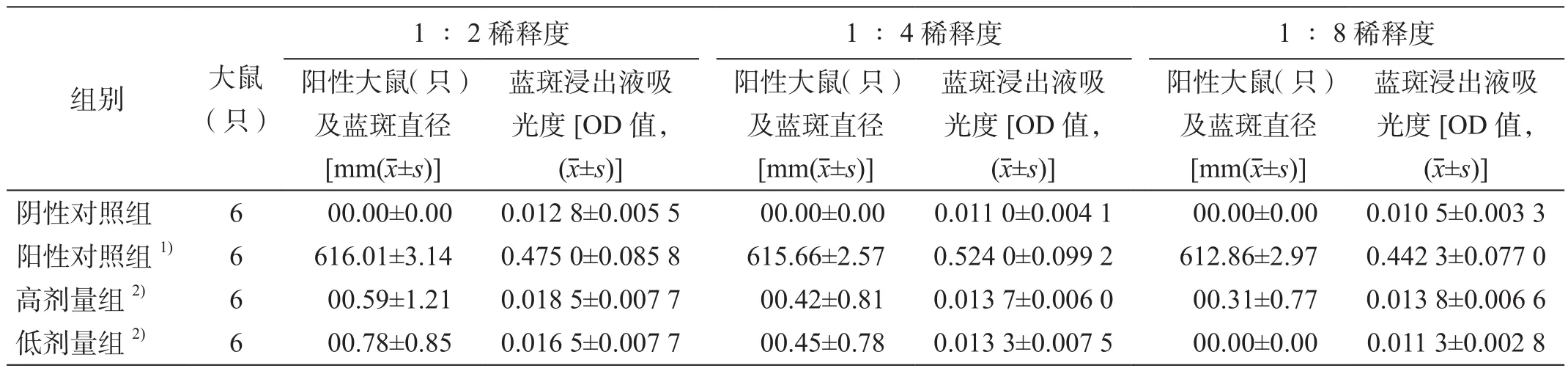
表1 大鼠皮肤蓝斑观察和吸光度测定
4 讨论
按照仿制药的注册申报要求,注射剂应进行临床前的过敏性评价研究。药物的过敏反应中,发生率最高的为Ⅰ型变态反应。豚鼠体内补体非常丰富,能最直观地反映Ⅰ型变态反应,因此豚鼠全身主动过敏试验常用于过敏性实验的评价研究。但是豚鼠对抗生素的敏感性比小鼠高1 000倍,对青霉素类、红霉素类、四环素类等抗生素特别敏感[6],无论给药剂量多大,给药途径如何,均可引起豚鼠发生小肠炎或结肠炎而死亡。我们曾采用豚鼠主动过敏试验评价注射用替加环素的过敏性,但注射用替加环素高、低剂量组豚鼠在致敏期间均有死亡,解剖后发现均有肠胀气现象,导致评价无法进行。
本研究中被动皮肤过敏实验的实验动物采用大鼠,是因为其对大多数实验药物都能够很好地耐受。实验方法为先在弗氏佐剂的强化下制备抗药物的抗血清,然后另选动物在皮内注射抗血清,随后静脉注射药物和染色剂,静脉注射的药物与皮内预先注射的抗血清进行结合,导致皮内染色,比较染色的强弱可以量化药物与抗血清的结合程度,从而反映药物致敏性的强弱。在本研究中阳性组出现了明显的蓝斑,而注射用替加环素高、低剂量组蓝斑的直径及吸光度与阴性组之间的差异在统计学上并无显著性,大鼠被动皮肤过敏实验结果显示:注射替加环素后未呈现明显的致敏性。
[1]卫生部合理用药专家委员会. 中国医师药师临床用药指南[M]. 重庆: 重庆出版社, 2009: 4-6.
[2]陈新谦, 金有豫, 汤光. 新编药物学[M]. 北京: 人民卫生出版社, 2007: 83-86.
[3]蓝继奎, 徐嘉红, 徐晓玉. 被动皮肤过敏试验影响因素初步研究[J]. 中药药理与临床, 2008, 24(2): 108-109.
[4]文洁, 朱建梅, 俞励平. 磷酸川芎嗪注射液血管刺激性、溶血性及过敏性试验研究[J]. 国际医药卫生导报, 2009,15(21): 28-31.
[5]梁新丽, 廖正根, 高秀蛟, 等. 注射用盐酸槐定碱对血管刺激性、溶血、过敏性试验研究[J]. 时珍国医国药, 2007,18(8): 1890-1891.
[6]王彦平. 医学实验动物学[M]. 长春: 吉林大学出版社,2005: 10-12.
