酒石酸掩蔽钨快速测定含钨锡料中锡的方法探索
2013-03-17刘娟
刘 娟
(1.湖南有色金属研究院,湖南长沙 410100;2.复杂铜铅锌共伴生金属资源综合利用湖南省重点实验室,湖南长沙 410100)
我国是世界上锡矿资源丰富的国家,储量居世界之首。主要以钨、铜、铅、锌、锑、钼、铋等伴生矿为主。而其中铜、钨、钼、锑等对锡的测定有严重干扰。锡主要跟钨伴生在一起,用铝片还原-碘酸钾容量法测定锡钨矿中的锡,钨同时被还原成为钨蓝,这对锡的滴定终点有严重干扰[1]。传统的分析方法是,用硝酸溶解试样,在EDTA存在的条件下,以氢氧化铍为载体,用氨水沉淀锡再进行分析[2],或者用辛可宁与锡形成黄色络合物沉淀来分离钨,再进行测定[3]。而这两种方法的操作都比较复杂,前者生成的β-锡酸沉淀颗粒很细,容易造成损失,结果不是很稳定,同时操作流程长。后者辛可宁价格昂贵,造成其分析成本很高,同时分析时间长。
笔者根据锡容易与酒石酸形成稳定络合物这一特性,首先用过氧化钠熔融样品,然后加入酒石酸使钨与酒石酸形成稳定的络合物,再用盐酸酸化,加入适量的还原铁粉,除去试样中可能伴生的铜、砷和锑等干扰元素,过滤分离。继而用铝片还原四价锡为二价锡,最后以淀粉为指示剂,用碘酸钾标准溶液滴定二价锡。该方法具有结果准确、快速、容易操作、成本低等优点,比较符合实际分析检测的要求。
1 实验部分
1.1 主要试剂
1.淀粉指示剂(0.5%)。
2.过氧化钠(化学纯)。
3.盐酸洗液(5%)。
4.铝片,纯度在99.5%以上,折叠成每片大约1.8 g,用锤子轻打压紧。
5.酒石酸、浓盐酸、还原铁粉均为分析纯。
6.锡标准溶液:准确称取1.000 0 g高纯金属锡,于500 mL容量瓶,加入盐酸250 mL使锡自然溶解,冷却至室温后用5%的盐酸洗液稀释至刻度,摇匀备用。
7.碘酸钾标准溶液:称取KOH 0.1 g,KIO30.6 g及KI 3.0 g于300 mL烧杯中,用水溶解,移入1 L容量瓶,稀释至刻度,摇匀。标定:准确吸取锡标准溶液25.00 mL于500 mL锥形瓶中加入40 mL盐酸,100 g/L FeCl3溶液5 mL后按实验方法操作,随同做空白实验。
1.2 实验方法
称取0.1 g试样置于50 mL铁坩埚中,加入2 g过氧化钠,用玻璃棒搅匀并用毛刷将玻璃棒上粘的粉末刷入坩埚,再覆盖2 g过氧化钠,将坩埚放入预先升温到730℃的马弗炉中至坩埚内熔融物呈均匀、透明的桃红色液体。取出稍冷,放入预先盛有50 mL热水的250 mL烧杯中。待剧烈反应后,用盐酸洗液洗出坩埚,加入10 g酒石酸,再加入浓盐酸40 mL,冷却致室温后少量多次地加入还原铁粉至三价铁离子的黄色退去,再放置半小时(若试样出现蓝色则表示酒石酸的加入量不够,可适当补加酒石酸固体至蓝色退去)。用脱脂棉过滤至500 mL锥形瓶中,并用盐酸洗液洗涤烧杯和沉淀3~5次,控制体积150 mL,补加浓盐酸40 mL。加入1.8 g铝片,摇至铝片快作用完时,盖上盛有饱和碳酸氢钠的盖氏漏斗,加热煮沸至铝片完全溶解取下,流水冷却至室温。取下盖氏漏斗,立即加入0.5%淀粉指示剂5 mL,迅速用碘酸钾标准溶液滴定至蓝色为终点,同时进行空白实验。
1.3 锡含量计算方法
锡含量按以下公式计算:
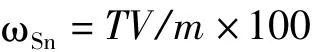
式中T为滴定系数,表示1 mL碘酸钾标准溶液相当于锡量/g·mL-1;V为滴定时消耗碘酸钾标准溶液的体积/mL;m为称样量/g。
2 结果讨论
2.1 掩蔽剂的选择
根据酒石酸,柠檬酸和双氧水都能与锡形成稳定络合物的性质,它们均可以用来做掩蔽剂,但是双氧水自身不稳定,容易分解,因此不采用,实验分别采用酒石酸和柠檬酸做掩蔽剂,发现酒石酸做掩蔽剂的终点更清晰稳定,因此选择了酒石酸做掩蔽剂。
2.2 酒石酸的用量
在整个分析过程中掩蔽剂的加入量十分关键,如果用量不够,钨会络合不完全而在后面铝片还原过程中出现钨蓝,使滴定终点无法判断。用量过多造成浪费,所以该方法对其用量进行方法实验。选取不同含钨量的样品进行实验,结果见表1。
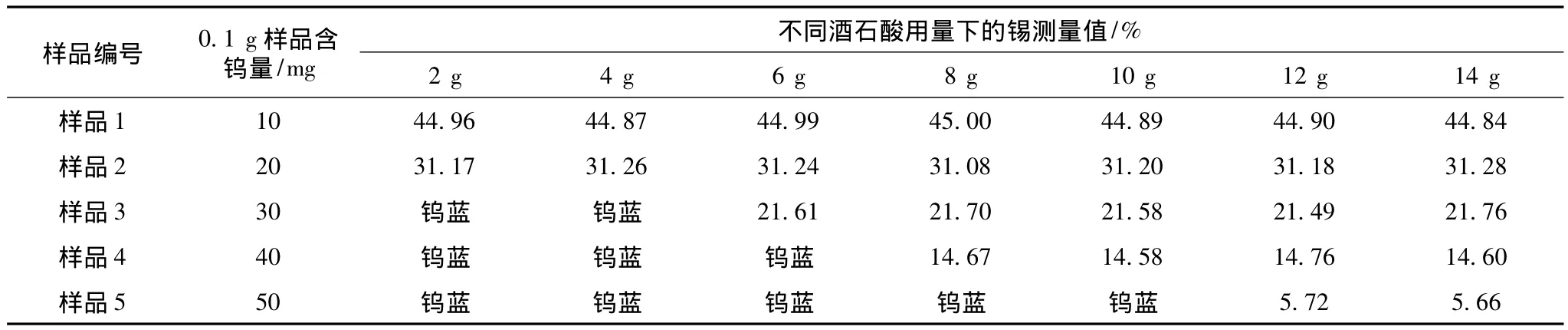
表1 酒石酸用量方法实验
从表2数据可见,当钨的含量低于40 mg时,加入酒石酸6 g可以完全络合钨,在铁粉还原除杂的过程中不会析出钨蓝。当试样中钨低于50 mg时,加入14 g酒石酸可以完全络合钨,且终点清晰结果稳定。实验中发现,在铁粉还原除杂时,若析出钨蓝,可以迅速补加酒石酸,钨蓝会退去,方便操作,同时不会造成过量而浪费。因此,根据经验该方法一般加入10 g酒石酸,若在铁粉还原时,析出钨蓝则再补加适量酒石酸,至钨蓝退去,不用担心酒石酸加入量不够而在铝片还原时析出钨蓝,影响终点观察。
2.3 还原铁粉除干扰杂质放置时间实验
含钨锡料中可能还伴生有铜、砷、锑、钼、铋等杂质元素,会干扰锡的测定。因此用还原铁粉将它们还原成单质而除去,还原时间是比较关键的一点,所以对样品1进行还原时间实验,数据见表2。

表2 还原时间实验
从表3数据可见,还原时间在10 min、20 min时,杂质没有完全除去,结果不稳定。时间在30 min以上可以除杂完全,所以该方法确定的还原时间为30 min。
2.4 测试结果及方法精密度实验
对样品1和样品4两个样品按上述方法平行测定7次,结果平均值与辛可宁沉淀钨分离钨的测试结果对照见表3。

表3 辛可宁分离法对照及方法精密度 %
2.5 标准回收实验
为考察方法的稳定性,进行了加入标准溶液回收实验,即在碱溶样品水浸洗出坩埚后加入一定的锡标准溶液,按上述方法测定样品含锡量,测定结果如表4。
结果表明,标准回收率为99.3%~100.1%,可以满足试样分析要求。

表4 标准回收实验
3 结语
采用过氧化钠熔融法分解,用酒石酸络合试样中的钨,从而不用分离钨可以直接测定含钨锡料中的锡,较好地解决了碘酸钾容量法测定含钨锡料中的锡钨干扰问题,大幅降低了测试成本,同时缩短了分析时间,可靠性较为理想,精密度满足分析工作的要求,拓宽了方法的适应性。
[1] 北京矿冶研究总院分析室.矿石及有色金属分析手册[M].北京:冶金工业出版社,1989.77-81.
[2] 北京矿冶研究总院分析室.矿石及有色金属分析手册[M].北京:冶金工业出版社,1989.225-226.
[3] 王桂珍.钨矿中锡的测定[J].理化检验-化学手册,2003,(4):234.
