与掺杂浓度相关的ZnS∶Mn纳米粒子的发光性质
2013-03-11杜鸿延魏志鹏孙丽娟楚学影李金华王晓华
杜鸿延,魏志鹏*,孙丽娟,楚学影*,方 铉,方 芳,李金华,王晓华,王 菲
(1.长春理工大学 理学院,吉林 长春130022;2.云南林业职业技术学院,云南昆明650224)
1 引言
目前常用的荧光半导体CdSe/ZnS纳米材料曾被誉为国际上纳米材料在实际应用中一个最成功的实例,但镉的剧毒、CdSe易分解等问题极大地限制了CdSe荧光纳米晶的临床应用和深入研究。因而,开发同样可以获得优异光学性质但不含毒性元素的其他荧光半导体纳米材料显得非常重要。Ⅱ-Ⅵ族半导体纳米材料以其新颖的光电性质受到人们极大的关注,其中ZnS是研究最为深入的材料之一[1]。ZnS主要以立方闪锌矿结构(ZB)和六角形纤锌矿结构(WZ)两种形式存在,在稳定的低温阶段形成立方闪锌矿结构,其带隙能为 3.72 eV[3];在温度高达1 296 K 时形成六角纤锌矿结构[2],其带隙能为3.77 eV[4]。ZnS 光传导性好,在可见光及红外范围内分散度低并且具有优良的荧光效应及电致发光功能,可用于很多发光材料的制备。
荧光纳米粒子是具有优良发光性质的纳米材料,这类材料在受到光激发或加上电压后会产生强的荧光,因此这些材料在平面显示器件、光电子元件(如发光二极管)、量子点激光器等技术领域有很重要的应用前景。纯相ZnS材料所能激发的光波范围有限,其颗粒形态、颗粒大小及其分布对光电性能均有较大影响,所以人们对掺杂型半导体纳米粒子进行了研究。掺杂型半导体通常引入的杂质离子是少量或微量的,一般不会改变母体半导体的晶体结构,但掺杂进去的杂质会产生新的电子能级或对母体的电子能级产生微扰,形成新的电子-空穴复合中心,从而使掺杂型半导体具有全新的光学性质。最早开展的掺杂型半导体纳米粒子的研究是1994年 N.Bhargva[5]等人报道的Mn掺杂ZnS纳米粒子的合成和性质研究。他们发现ZnS∶Mn纳米粒子和其体相材料相比具有更高的荧光量子产率,而荧光寿命有所缩短,并认为这是由于纳米粒子尺寸减小导致掺杂Mn的d电子态和ZnS的s-p态产生强的杂化所致。尽管随后的研究表明他们对荧光寿命缩短的观察结果是错误的,但这一发现使得人们对掺杂型纳米粒子的研究兴趣倍增。目前大部分的工作集中于Mn[6]掺杂Ⅱ-Ⅵ族半导体纳米粒子的研究上,此外,关于 ZnS掺杂 Al[7]、Cu和稀土离子等的研究已见报道。2008年Anuja[8]等人的研究表明掺杂Cu的ZnS系统出现了从纤锌矿到闪锌矿的相变。
由于Mn离子和Zn离子的电荷相等,离子半径近似,Mn离子可以较好地掺入ZnS晶格而不会对晶格产生较大影响。相关研究多集中在掺入杂质后对于发光的影响,而掺杂浓度对样品发光强度、波长等方面影响的研究未见报道。故本文采用溶胶法制备Mn掺杂的ZnS纳米粒子,希望可以通过改变掺杂浓度获得发光性质可调,具有良好生物偶联功能的掺杂型ZnS纳米材料,为进一步开发此种安全无毒的纳米材料在生物医学领域中的应用奠定基础。
2 实验部分
2.1 化学药品
二水合乙酸锌产自天津市科密欧化学试剂研究所,九水合硫化钠四水合乙酸锰购于汕头市西陇化工厂,氢氧化钠购于北京化工厂,3-巯基丙酸(MPA)购于ALDRICH化学试剂公司,实验用水为自制的去离子水。
2.2 掺杂ZnS∶Mn纳米晶的制备
掺杂ZnS纳米粒子的制备方法有很多,如微波法、溶胶-凝胶法、喷雾热解法、水热法等。由于溶胶法制备的纳米粒子水相分散稳定性好、操作简便,所以采用了溶胶法进行ZnS∶Mn纳米粒子的制备。主要过程如下:首先准备5 mL浓度为0.05 mol/L 的乙酸锌溶液,取65.22 μL 的3-巯基丙酸加入10 mL的去离子水中。将乙酸锌溶液缓慢地加入到3-巯基丙酸的水溶液中,此时溶液变浑浊,再加水稀释至30 mL,此时溶液恢复澄清,然后取1.5 mL浓度为0.005 mol/L和3 mL浓度也为0.005 mol/L的乙酸锰溶液加入上述溶液,即是掺杂浓度分别为3%和6%Mn的含量,搅拌均匀后用浓度为4 mol/L的NaOH溶液将pH值调节至10左右,在剧烈搅拌条件下向其中注入5 mL浓度同样为0.05 mol/L的硫化钠水溶液,继续搅拌15 min,得到ZnS透明溶胶。
2.3 表征方法
利用Rigaku D/max 2500型X射线衍射仪(XRD)对样品晶体结构进行分析验证;利用FEI Tecnai F20型高分辨透射电子显微镜(HRTEM)观察粒子的形貌;利用法国JY公司的LabRam HR-800型光谱仪和Perkin Elmer instruments公司的LS 55型荧光光谱仪分别获得了样品的光致发光光谱(PL)和荧光光谱。
3 结果与讨论
3.1 ZnS∶Mn 的晶体结构表征
图1为不同Mn掺杂浓度的ZnS∶Mn纳米粒子XRD衍射图。从图中可以看出,在 28.47°、47.58°、56.49°有明显的衍射峰,通过与 JCPDS 标准卡对比,分别对应 ZnS的(111)、(220)、(311)这3个晶面,说明所制备的样品为硫化锌的立方闪锌矿结构,并且从XRD上可以看出当掺杂Mn的含量达到6%时都没有出现分相。进一步观察发现,对于(111)晶面,未掺杂的ZnS样品其中心峰位在28.47°,Mn离子掺杂浓度为3%时,该衍射峰中心峰位移至28.33°;而当掺杂浓度达到6%时,该峰位进一步向小角度偏移至28.18°。由于Mn的离子半径为0.08 nm,Zn的离子半径是0.074 nm,Mn的离子半径大于 Zn的离子半径,这种随着掺杂浓度增大,衍射峰向小角度偏移的现象可以理解为Mn离子取代了Zn离子,使得晶体内部发生晶格膨胀的结果。

图1 溶胶法制备的ZnS∶Mn纳米粒子的X射线衍射及JCPDS标准卡数据Fig.1 XRD patterns of ZnS∶Mn nanoparticles prepared with gel process and the standard JCPDS data
根据Debey-Scherrer方程可以通过衍射峰的宽度计算出粒子的平均粒径,方程如下:D=Kλ/βcosθ[9],其中 D 为晶粒直径,λ 为所用单色 X 射线波长,β为半峰值强度处所测得的衍射线宽化度(以弧度计),θ为布拉格衍射角,即入射与某一组晶面所成的折射角。通过计算得出没有掺杂的样品的平均粒径约为7.0 nm;掺杂浓度为3%的ZnS∶Mn纳米粒子的平均粒径约为5.5 nm;掺杂浓度为6%的样品粒径约为4.5 nm,即随着掺杂浓度的增大,平均粒径减小。
3.2 样品的荧光性质
图2为不同掺杂浓度的ZnS∶Mn纳米粒子的荧光激发谱和发射谱。其中左侧曲线是固定发射波长为420 nm时采集到的激发谱,右侧曲线是以301 nm的紫外光作为激发光所获得的发射谱。对于3组样品,以301 nm的紫外光作为激发光,在420 nm附近均可观察到明显的发射峰,这是由于ZnS纳米粒子表面缺陷引起的发光[10]。从图中还可以看出,由于掺杂浓度的增加,纳米粒子的平均粒径减小,由于量子尺寸效应使得带隙能增大导致荧光激发光谱发生蓝移[11],而由于掺杂产生的缺陷发光使得荧光发射光谱发生红移。为了比较不同掺杂浓度的样品的荧光发射强度,在相同测试条件下,对相同粒子浓度的溶液样品进行了荧光发射光谱的采集,由于荧光光谱测试是对液体进行测试,先把样品稀释为相同的浓度,再进行发光强度的对比,结果发现掺杂浓度3%的样品在420 nm荧光发射强度最强。随掺杂浓度的增加,粒径减小,这一荧光强度有所增加,这是由于粒径减小后比表面积增大,导致纳米粒子表面效应增强而引起的。但是当继续增加掺杂浓度到6%时,荧光强度反而下降,这是由于激活中心Mn的浓度较低时,离子之间距离较远,能量传递效率不高,所以荧光强度不大。随着Mn浓度的增加,发光中心增加,所以荧光强度增加。当达到3%以后,再增加Mn的浓度,荧光强度反而因复合发光中心的形成呈现浓度猝灭现象[12]。
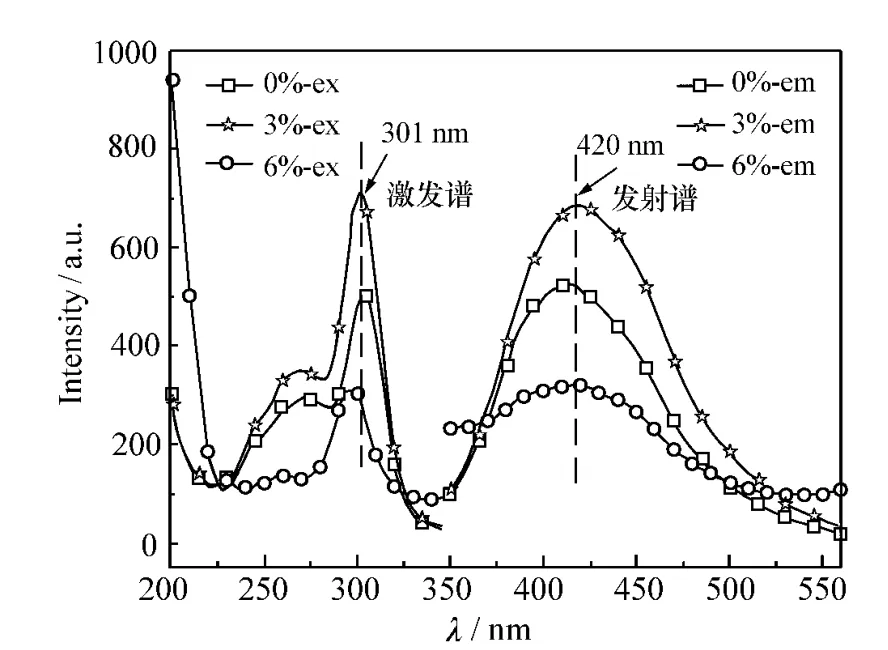
图2 溶胶法制备的不同掺杂浓度的ZnS∶Mn纳米粒子的荧光激发谱和发射谱Fig.2 Excitation and emission spectra of ZnS∶Mn prepared at different doping concentrations with gel process
图3是以297 nm的紫外光作为激发光对两种掺杂浓度的ZnS∶Mn样品进行荧光测试的结果,可以观察到590 nm附近有很明显的发光峰。对于ZnS∶Mn纳米粒子来说,这附近的发射谱带是掺杂Mn离子在ZnS基质中的特征发射带,由Mn离子的4T1-6A1跃迁产生。在ZnS晶体中,掺杂Mn2+离子取代ZnS晶格中Zn2+离子位点,激发光被ZnS母体吸收后,使其电子受到激发,空穴则被Mn离子俘获,电子和空穴在Mn离子上复合导致Mn离子的激发,然后以发射荧光的形式释放能量[13]。可以看出随着掺杂浓度的增加,Mn2+的发射峰发生蓝移,说明通过改变掺杂离子的浓度,能够获得波长可调的荧光发射。
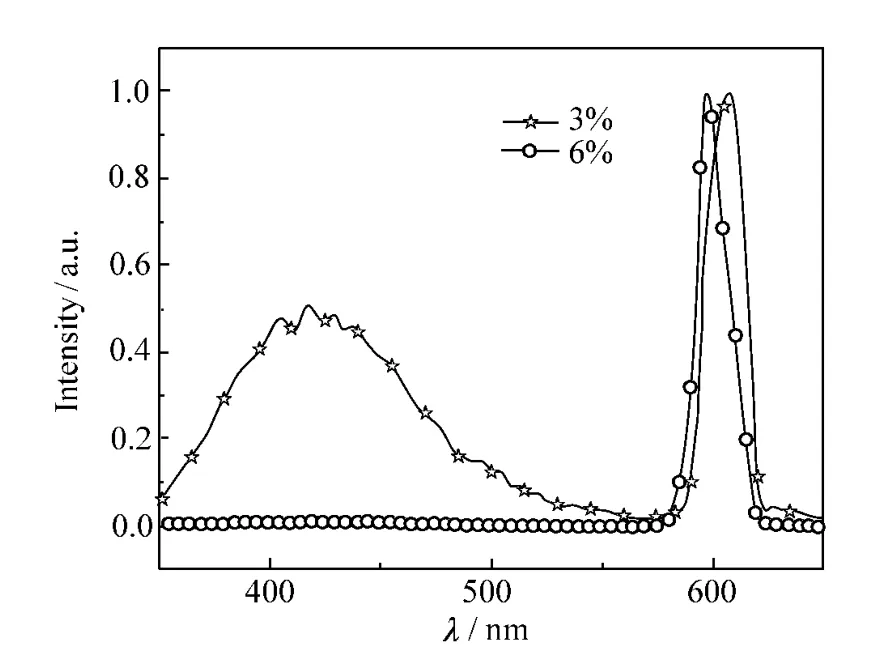
图3 溶胶法制备的ZnS∶Mn纳米粒子的荧光光谱Fig.3 Fluorescence spectra of ZnS∶Mn nanoparticles prepared with gel process

图4 加热陈化处理后 ZnS∶Mn纳米粒子的HRTEM图Fig.4 HRTEM photo of ZnS∶Mn nanoparticles after heating ageing

图5 3%掺杂的ZnS∶Mn纳米粒子的PL谱Fig.5 PL spectra of ZnS∶Mn nanoparticles with 3%doping concentration
由于掺杂浓度为3%的ZnS∶Mn样品在图2中的发射谱强度最大,本文针对这一掺杂浓度的样品,研究了制备过程中温度对纳米粒子形貌和光致发光性质的影响。图4是掺杂浓度为3%的ZnS∶Mn样品经过50℃陈化1 h后的高分辨透射显微镜图(HRTEM),可以看到所得产物为球状粒子,尺寸分布均匀,经过加热陈化平均粒径增大约为20 nm。图5是浓度为3%掺杂的ZnS∶Mn样品经过50℃陈化1 h和没有陈化的样品的光致发光光谱。由于在空气中加热陈化可以通过溶液中的溶解氧在纳米粒子表面的吸附钝化来改善纳米粒子的发光强度[14],观察到了加热陈化1 h后的样品在590 nm附近出现了很明显的发光峰,说明加热陈化有利于ZnS∶Mn样品中Mn2+的发光。
4 结论
本文采用溶胶法制备了Mn掺杂的ZnS纳米粒子,探讨了掺杂离子浓度及加热陈化对于纳米粒子晶体结构和发光性质的影响。结果表明:改变掺杂离子的浓度可以调节ZnS∶Mn纳米粒子在590 nm处Mn的发光波长;并且发现随Mn离子掺杂浓度的增加,410 nm处的发光强度增加,当浓度增加到一定范围时发现了浓度荧光猝灭现象,而加热陈化有利于ZnS∶Mn纳米粒子中Mn2+在590 nm处产生荧光。
[1] 邹定海,赖松林,程树英,等.退火温度对电子束蒸发的ZnS薄膜性能的影响[J].电子元件与材料,2010(11):35-37.ZOU D H,LAI S L,CHENG SH Y,et al..Influence of annealing temperature on properties of ZnS thin films prepared by electron-beam evaporation[J].Electronic Components Materials,2010(11):35-37.(in Chinese)
[2] YEH C Y,LU Z W,FROYEN S,et al..Zinc blende wurtzite polytypism in semiconductors[J].Phys Rev B,1992,46:10086-10097.
[3] FANG X SH,ZHAI T Y,GAUTAM U K,et al..ZnS nanostructures:from synthesis to applications[J].Progress Materials Science,2011,56:175-287.
[4] CHEN H,SHI D,QI J,et al..The stability and electronic properties of wurtzite and zinc-blende ZnS nanowires[J].Phys Lett.A,2009,373:371-375.
[5] BHARGAVA R N,GALLAGHER D.Optical properties of manganese-doped nanocrystals of ZnS[J].Phys.Rev.Lett.,1994,72:416-419.
[6] BEGUM R,CHATTOPADHYAY A.In situ reversible tuning of photoluminescence of Mn2+-doped ZnS quantum dots by redox chemistry[J].Langmuir,2011,27:6433-6439.
[7] NAGAMANI K,REVATHI N,PRATHAP P,et al..Al-doped ZnS layers synthesized by solution growth method[J].Current Appl.Physics,2012,12(2):380-384.
[8] DATTA A,PANDA S K,CHAUDHURI S.Phase transformation and optical properties of Cu-doped ZnS nanorods[J].J.Solid,State Chem,2008,181:2332-2337.
[9] DIECKMANN Y,CÖLFEN H,HOFMANN H,et al..Particle size distribution measurements of manganese-doped ZnS nanoparticles[J].Anal.Chem.,2009,81:3889-3895.
[10] WANG X F,XU J J,CHEN H Y.A new electrochemiluminescence emission of Mn2+-doped ZnS nanocrystals in aqueous solution[J].J.Phys.Chem.C,2008,112:17581-17585.
[11] 李娟娟,徐光明.掺杂ZnS纳米粒子的制备及应用[J].化学进展,2010,22(5):861-866.LI J J,XU G M.Preparation and applications of doped ZnS nanoparticles[J].Progress Chem.,2010,22(5):861-866.(in Chinese)
[12] 毛丽红.纳米硫化锌发光材料的制备与发光性能研究[D].上海:上海师范大学,2005.MAO L H.Nanometer ZnS luminescence materials preparation and luminous property research[D].Shanghai:Shanghai Normal University,2005.(in Chinese)
[13] ZOU W SH,SHENG D,GE X,et al..Room-temperature phosphorescence chemosensor and rayleigh scattering chemodosimeter dual-recognition probe for 2,4,6-trinitrotoluene based on manganese-doped ZnS quantum dots[J].Anal.Chem.,2011,83(1):30-37.
[14] HE Y,WANG H F,YAN X P.Exploring Mn-doped ZnS quantum dots for the room-temperature phosphorescence detection of enoxacin in biological fluids[J].Anal.Chem.,2008,80:3832-3837.
