碳化过程中铁的腐蚀及控制措施
2012-12-23康跃辉孙秋菊
康跃辉,孙秋菊
(1.大连化工研究设计院,辽宁大连 116023;2.唐山三友化工股份有限公司,河北唐山 063305)
碳化过程中铁的腐蚀及控制措施
康跃辉1,孙秋菊2
(1.大连化工研究设计院,辽宁大连 116023;2.唐山三友化工股份有限公司,河北唐山 063305)
在纯碱生产中,常常因为铁含量的偏高而导致纯碱白度不够。影响铁含量升高的因素除了设备自身腐蚀外,还涉及到氧的浓度、设备内部液面的波动以及S2-的浓度等。
自身腐蚀;氧浓度;铁含量;产品质量;措施
氨盐水的碳酸化过程是纯碱生产的中心环节,而此过程中的诸多设备都是铸铁(Fe含量95%以上,碳含量0.05~4%)材质的。铸铁本身的腐蚀以及液体和气体对设备、管道内壁的冲刷,使大量铁元素变成Fe2+,并被氧化成不溶物最终混在纯碱中影响产品的质量。本文将联系理论与本厂实践详细阐述影响铁腐蚀的几个主要因素及几种控制措施。
1 影响铁腐蚀的因素
1.1 铸铁自身的腐蚀
众所周知,铸铁和碳素钢一样存在着多种金相结构,一般为铁素体、渗碳体和石墨。它们具有相同的电极电位。其中,石墨的电位最高,为+0.37V,铁素体的电位最低,为-0.44V,渗碳体介于两者之间。
当铸铁浸渍在强电解质溶液中时,由于结构上的非均一性,其表面必然形成电位差较大的腐蚀电池,电位最低的铁元素成为阳极以二价离子形式存在于溶液中,是阳极过程。

系统中溶入的Fe2+会进一步被氧化成Fe2O3,混入成品中,最终影响产品质量。
1.2 去极化剂对铁腐蚀的影响
1.2.1 O2浓度的影响
由上述可知,由于设备自身的腐蚀,会有一部分铁元素失去电子,而变成Fe2+溶于液体物料中,此为腐蚀电池的阳极过程。如果系统中不发生其它电极过程,那么这种阳极过程会很快停止。因为金属中积累起来的电子会使电位强烈的跃向负方,这就阻止了阳极过程的继续进行。一旦溶液中存在着去极化剂,它们就会在阴极石墨表面吸收电子,形成阴极过程。例如,溶液中的溶解氧会在电解质中发生如下反应:

可以看出溶液中的溶解氧与Fe2+生出氢氧化亚铁,它会进一步被氧化成Fe2O3,混入成品中,最终导致成品铁含量超标。
此外,氧含量最终影响成品含铁量的原因还反映在其对设备防腐层的破坏。在纯碱行业中,为了延缓设备腐蚀的速度,一般向设备中加入一定量的S2-(混有S2O、SO),使其产生一层硫膜,避免设备与物料的直接接触。而O2的介入使大量的S2-(混有S2O、SO),被氧化成高价硫,而不能形成硫膜。

从而加剧设备的腐蚀程度,增加物料中Fe含量。
我厂主要是通过控制中和水含铁量来间接控制纯碱中的含铁量。理论上讲,当窑气和炉气中O2浓度很大时,会加剧腐蚀电池中阳极反应和阴极反应的进行,从而使大量的Fe元素溶于物料中,导致中和水中Fe含量升高。
为了进一步确定这一理论,我厂做了如下试验。配制不同O2浓度的清洗气,该清洗气以7 500~ 9 000Nm3/h的量进清洗塔,检测在没有回卤的情况下,中和水中铁浓度的变化。表1为本实验的主要数据(平均值)并附有折线趋势图(图1)。

表1 中和水Fe含量及清洗气O2浓度
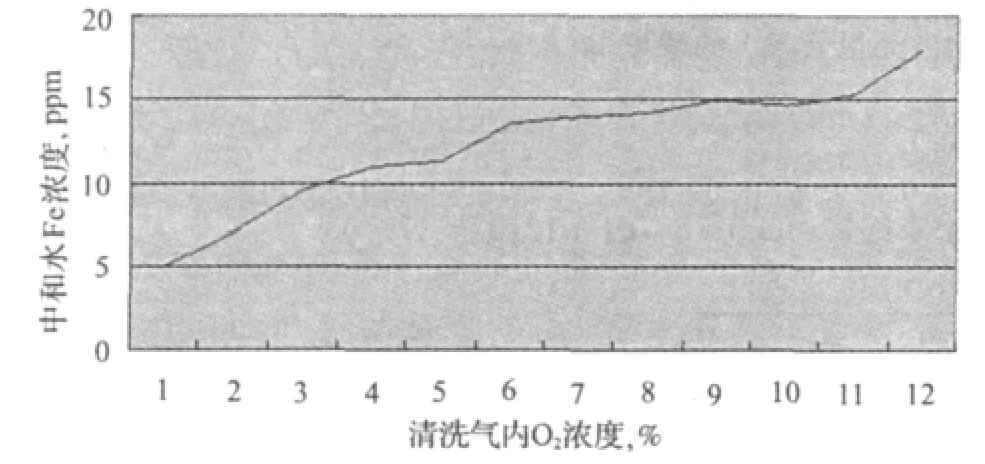
图1 中和水Fe与清洗气O2浓度变化
以上数据显示,随着氧浓度的增加,中和水Fe呈上升趋势。由此可以看出,O2的浓度高是导致最终产品含铁量高的一个主要因素。

此时H+作为去极化剂,吸收Fe丢失的电子,再加上受溶解氧的影响,加剧了设备的腐蚀倾向。

1.3 CO2对铁腐蚀的影响
在氨盐水碳酸化过程中,随着CO2的不断吸收,溶液中的pH值也会逐渐减小,此时溶液呈酸性,而起保护层作用的FeS膜在酸性环境下易分解,特别是清洗塔,由于碱疤被清洗,FeS膜更易与溶液接触,也就更易受酸性影响而被分解,减小其对设备的缓蚀作用,导致清洗塔出液——中和水Fe含量高。最终影响成品质量。
1.4 其他因素对铁腐蚀的影响
1.4.1 过洗
上面说到,清洗塔中CO2浓度过高会导致中和水Fe含量增大,而中和水中CO2浓度正常时,也可能造成中和水Fe含量大的原因是过洗。当清洗时间过长时,塔壁已没有或者有很少碱疤。此时,气体的鼓动会破坏硫膜,使清洗塔失去保护层,进而导致铁高。
1.4.2 温度、压力和波动影响
在温度过高区域,或者由于塔况不稳造成液面和压力的波动时,有些不紧密的FeS膜便会脱落,导致保护层的缺损,最终导致Fe含量上升。
2 控制铁腐蚀的措施
2.1 保护膜的形成
2.1.1 FeS的形成及防腐原理
纯碱工业中,一般通过在制碱系统中添加和维持一定的S2-含量,来缓解设备腐蚀和保证产品质量。我厂主要是通过向吸收塔中加Na2S来获得S2-。
上述可知,铸铁设备在经过腐蚀和被氧化之后,形成氧化铁层,而这些氧化铁层在遇到S2-后会生成FeS。其反应式为:

此时FeS是一层黑色的无孔隙的薄膜,它紧密吸附在钢铁表面,这层薄膜虽然不像纯铝表面上的氧化铝那样坚固,但它也具有保护层的作用,有效的阻止阳极区域Fe2+的溶出,能耐氨盐水对设备的腐蚀,制成的重碱及纯碱不致含有铁锈,保证了纯碱的白度及铁含量。
物料中S2-的浓度需控制在一定的范围内,一般情况下,氨盐水中S2-浓度为0.01~0.03tt,特殊情况时(如更换设备,开停设备),S2-的含量可暂时增加至0.05tt。如果S2-浓度不足,Fe2+会混入碱中,形成Fe2O3,使产品变红,产生红碱。
2.1.2 Mg2+的加入
纯碱生产中,有时因为操作的波动或者温度、压力的影响而使硫膜遭到破坏或者不易形成硫膜,此时可以在设备中加入一定量的Mg2+。

此时,镁的沉淀物会生成白色的结疤,附着在设备的内壁,起到一定的防腐作用。但由于其量不好控制,因此用的较少。
2.2 溶解氧浓度的控制
为了延缓设备的腐蚀,也就是使设备中的腐蚀电池达到平衡,那么应尽量避免或减少物料中可作去极化剂的O2的含量。
氨盐水的碳酸化作为纯碱生产的中心工序,其溶解氧的主要来源为窑气和炉气。因此,为了达到成品含铁量合格的目的,在操作中必须严格控制窑气和炉气中的O2含量,保证所供气体的质量。或者在输送途中设置除氧装置,从而降低设备的O2摄入量,最终达到降低生产“红碱”机率的目的。
2.3 中和塔的控制
2.3.1 温度控制
从理论上讲,用较高温度的氨盐水对清洗作业较为有利,能加快碱结疤的溶解速度。但是,过高的温度会在一定程度上造成硫膜的脱落,从而降低了对设备的保护作用,因此,在生产操作中,应保证氨盐水温度在38℃左右。
2.3.2 压力的控制
在纯碱生产中,要求碳化塔(中和塔、制碱塔)维持一定的净塔压,这样不仅有利于CO2的吸收,而且减少设备的暴空。减少设备内壁与O2直接接触的机率,防止物料中Fe的氧化物含量增加。目前我厂净塔压一般控制在0.235~0.240MPa之间。
2.3.3 中和水中CO2浓度的控制
CO2的浓度过高,会导致溶液中pH值下降,从而加速硫膜的溶解,破坏设备的防腐层,最终导致中和水中Fe含量超标,而如果CO2浓度过低,则达不到预碳化的目的。因此,在生产操作中,一般控制中和水CO2浓度在55~60tt。
2.3.4 其它因素的控制
如果外部所供气体所含废气量较大,会导致塔内波动。物料的急剧冲刷会造成硫膜的脱落。为了防止这一现象的发生,生产中应尽量保证供给碳化塔的气体质量。一般中段气、清洗气浓度为40%,下段气浓度为90%左右。并且保证设备的平稳操作。
3 结 语
综上所述,导致纯碱含铁量大的因素主要有设备的自身腐蚀,外界因素破坏FeS膜。为了增大纯碱白度,在操作过程中,应尽量保证物料中S2-的浓度,减少进气中O2的浓度,确保碳化塔平稳运行。
[1] 陈学勤.氨碱法制碱工艺[M].沈阳:辽宁科学技术出版社,1984
[2] 大连化工研究设计院,纯碱工学[M].北京:化学工业出版社,1990
[3] 孙锡吾.纯碱工业设备的腐蚀与防护[J].纯碱工业,1984(3):14~12
[4] 王葆林,朱建华,等.从腐蚀控制中寻找财富[J],全面腐蚀控制.2003,17(2):1~3
[5] 候德榜.制碱工学(下册)[M].北京:化学工业出版社,1960
TQ 114.16
B
1005-8370(2012)02-17-03
2012-02-10
