Fenton氧化深度处理焦化废水的研究
2012-11-06赵华章
赖 鹏, 赵华章
(1. 国家开发银行股份有限公司四川省分行, 四川 成都 610027; 2. 北京大学环境工程系,北京 100871)
Fenton氧化深度处理焦化废水的研究
赖 鹏1, 赵华章2
(1. 国家开发银行股份有限公司四川省分行, 四川 成都 610027; 2. 北京大学环境工程系,北京 100871)
采用Fenton氧化对焦化废水进行了深度处理。结果表明:Fenton氧化反应迅速,可迅速降低焦化废水生化出水的COD;H2O2和Fe2+的投加量对Fenton氧化具有明显的影响;pH=3时反应体系具有最佳的COD去除效果。在H2O2投加量为1.994 mL/L,FeSO4·7H2O投加量为0.543 g/L,pH=3,温度为35 ℃的条件下,反应出水COD低于100 mg/L,去除率可达72.7%;Fenton氧化可有效去除生化出水中的难降解有机物。实验结果表明Fenton氧化是深度处理焦化废水的有效工艺。
Fenton氧化; 焦化废水; 深度处理; 难降解有机物
焦化废水主要来源于钢铁行业炼焦的焦化厂,是炼焦炭或制煤气过程中产生的难降解有机工业废水。焦化废水水质成分复杂,含有高浓度的氨氮和有机化合物,其中有机物主要为酚类化合物、多环芳香族化合物(PAHs)以及含氮、氧、硫的杂环化合物及脂肪族化合物[1,2]。目前,国内焦化废水处理普遍采用以生物处理为核心的传统活性污泥或A2/O工艺,但大部分焦化废水处理后仍然无法达标排放(尤其是 COD,化学需氧量),因此需要研究对焦化废水进行深度处理的方法。
Fenton氧化反应由国外研究者 Fenton在 1894年发现,为高级氧化工艺(Advanced Oxidation Processes)的一种。其主要特点是通过羟基自由基(·OH)的强氧化性(标准电极电势为2.8 V,除F2以外最强的氧化剂)将有机物有效分解,甚至转化为CO2和H2O。Fenton反应具有氧化能力强、反应速率快、选择性小等优点,其主要影响因素为废水特性、Fe2+和H2O2的投加量、pH、温度、反应时间等。近年来,Fenton氧化被广泛的运用于炼油废水、焦化废水、食品废水、垃圾渗滤液、制药废水和染料废水等的处理研究中,大大提高了难降解有机物的去除效率[3-6]。
本文采用Fenton氧化工艺对焦化废水生化出水进行深度处理研究,考察反应时间、药剂投加量、pH、反应温度等不同影响因素条件下的处理效果和特点,这对工程实际操作具有较强的理论指导意义。
1 实验部分
1.1 主要实验仪器和材料
专用 COD消解加热器和专用消解管(酸性重铬酸钾氧化法,美国HACH公司);pH-201型pH计(意大利HANNA公司)。
实验水样:实验中采用废水为某焦化厂A2/O工艺的生化出水,该水样水质呈深褐色,有强烈的刺鼻气味,pH为6.5~7.5。由于该某焦化厂生化出水COD波动较大,实验中通过稀释的方法将实验水样的COD控制在200~300 mg/L。
实验试剂及设备:FeSO4·7H2O、H2O2(浓度为30%)、KMnO4溶液(0.01 mol/L)、MnSO4(100 g/L)。所有试剂均为分析纯,利用去离子水配制。MY-3000型搅拌机和恒温水浴锅。
1.2 实验方法
1.2.1 Fenton氧化实验方法
取实验水样1 L,pH根据实际需要调节。将水样倒入实验杯,加入预先计算好投加量的FeSO4·7H2O固体颗粒,先以200 r/min搅拌使其快速溶解,然后迅速加入相应量的H2O2继续搅拌,不同时间间隔取样测试水质。取样量为25 mL(测试H2O2浓度),利用滴管加入4.5 mol/L的NaOH,控制pH为9左右,利用玻璃棒进行搅拌,待絮体完全沉淀后取上清液迅速分析。除研究温度影响外其他实验均在室温下进行。研究反应时间、H2O2投加量、Fe2+投加量、pH、温度等条件对反应过程的影响。
1.2.2 COD测试干扰的排除方法
Fenton反应出水中残留的H2O2会造成COD测试的误差[7],因此研究中需要测试出水中 H2O2的浓度以及所占COD的比例。测试方法参考文献提供的酸性高锰酸钾滴定法[8],具体操作如下:取氧化出水10 mL,置于250 mL碘量瓶中;加入2 mol/L H2SO420 mL与100 g/L的MnSO4溶液3滴,摇匀;用0.01 mol/L的 KMnO4滴定液滴定至溶液呈粉红色,记录KMnO4滴定液用量,计算得出 H2O2的浓度。H2O2的浓度对应COD的线性关系由预实验事先求得。测定出水的COD时,先测出水样的总COD值,再测出水样中残留H2O2贡献的COD值,两者的差值为水样的真实COD。
1.2.3 GCMS分析方法
样品前处理采用二氯甲烷液液萃取的方法,采用美国Agilent公司的6890N气相色谱系统(GC)和5973质谱系统(MS)的组合,DB-35MS毛细管柱,MSD ChemStation工作站进行自动分析。具体的操作参数如先前的研究报道[9-11]。
2 结果与讨论
2.1 反应时间的影响
研究中先根据文献调研结果选择理论的 H2O2和 Fe2+的投加量,并在 pH=3的条件下进行反应。具体操作为:H2O2投加量采用理论的投加量(Qth),即按照COD=1 000 mg/L计算,则每L废水理论加入H2O2(30%)的量为6.38 mL,当水样COD改变时,所需 H2O2的量依此类推计算[12]。按照文献[8]提供H2O2:Fe2+=10:1的量(摩尔比)投加Fe2+。
研究中采用H2O2(30%)投加量为Qth(1.595 mL,FeSO4·7H2O 为 0.434 4 g),采样时间为 5~150 min。不同反应时间出水的COD的变化如图1所示。

图1 不同反应时间下出水COD的变化Fig. 1 Change of COD with reaction time
从图1中可以看出,在Fenton氧化过程中,水样的COD在10 min内由初始的263.1 mg/L迅速降低至150 mg/L左右,可见Fenton反应与体系中难降解有机物反应相当迅速。反应10 min后COD降低变得较为缓慢,在120 min时出水COD降至112.2 mg/L,去除率达到 54.4%。在后续实验中采用 120 min为反应时间。
Fenton氧化反应实际为一系列的链式反应,其反应变化通常认为包含以下历程:
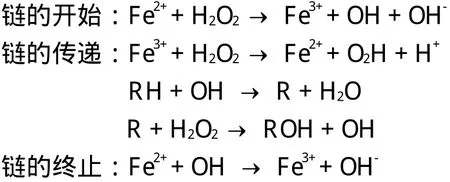
从以上反应历程看出,Fe2+和H2O2反应迅速产生Fe3+和·OH,Fe3+会进一步消耗H2O2产生活性自由基。这些自由基对有机物进行氧化攻击,并在传递电子的过程中消耗了H2O2。实验中测试发现,反应150 min后出水中仍含有约200 mg/L的H2O2,这与H2O2︰Fe2+=10︰1这一投加量相关,表明在此投加量下H2O2是相对过量的,反应出水的Fe离子主要以Fe3+的形式存在。
2.2 H2O2投加量的影响
固定最终反应时间为120 min,反应体系pH=3,H2O2︰Fe2+=10的操作条件,研究 H2O2投加量对Fenton反应的影响。不同 H2O2投加量条件下出水COD的变化如图2所示。

图2 不同H2O2投加量下出水COD的变化Fig. 2 Change of COD with dosage of H2O2
可以看出,随着H2O2投加量的增加,出水COD逐渐降低。在反应 120 min后,H2O2投加量为0.125~0.5 Qth时COD的降低变化不明显。当投加量为1~1.5 Qth时,出水COD的降低趋势呈现较大幅度的提高。对于不同 H2O2投加量条件下(由低到高),120 min后的COD去除率分别为37.6%、36.5%、37.0%、46.4%、65.5%和76.8%。当投加量为1.25 Qth和1.5 Qth时,出水COD分别降低至83.9 mg/L和58.0 mg/L,具有良好的去除效果。这是由于 H2O2的增加提高了·OH生成的浓度和持续性,从而提高了氧化效率[13]。考虑到实际处理中的经济因素,后续实验采用H2O2投加量为1.25 Qth。
2.3 Fe2+投加量的影响
在反应时间为120 min,pH=3,H2O2的投加量为1.994 mL/L(1.25 Qth)条件下研究Fe2+投加量对Fenton反应的影响。不同操作条件下出水COD的变化如图3所示(图中比例为H2O2︰Fe2+)。
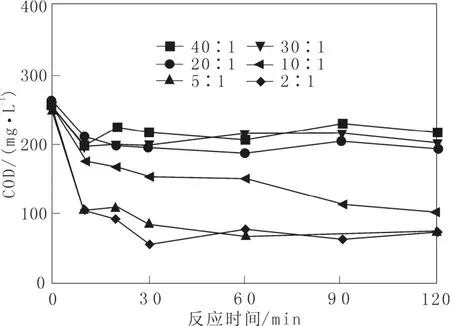
图3 不同Fe2+投加量下出水COD的变化Fig. 3 Change of COD with dosage of Fe2+
从图3中看出,Fe2+投加量较低时COD的去除效果不佳。在H2O2:Fe2+为40、30和20的情况下COD的绝对去除量仅为50 mg/L左右,出水COD保持为200 mg/L左右。H2O2:Fe2+为10、5和2的情况下COD去除效果明显,且H2O2:Fe2+为5和2情况下COD的去除变化不大。反应120 min后,不同投加量条件下COD去除率分别为18.7%、27.0%、33.7%、58.3%、70.3%和71.1%,具有明显的差异。
Fe2+在Fenton反应中起着重要的作用[14]。Fe2+浓度的增加可以加速·OH生成速率和浓度从而进一步提高氧化效率,但过多的 Fe2+会导致·OH自身发生复合反应,氧化效果增加不明显,反而有略微下降[13]。此外,增加 Fe2+浓度可以提高后续混凝的去除效率[14]。在本研究中,H2O2︰Fe2+=2时反应开始便出现了明显的絮凝现象,不利于后续操作。实验中测试残留H2O2的浓度发现,当H2O2︰Fe2+为5和2时,出水中 H2O2浓度极低,表明 H2O2在氧化反应中被充分消耗,推测生成的·OH浓度较高,因而氧化效率高。考虑到实际操作中的经济因素,后续采用Fe2+投加量为H2O2︰Fe2+=10。
2.4 体系pH的影响
反应体系的pH条件在Fenton氧化过程中起到了重要作用。众多报道其最佳效果发生在pH=3的体系中,主要原因是催化H2O2分解的Fe的有效形式是Fe(OH)2+,pH=3时Fe(OH)2+的浓度相对较高,从而保证了生成的·OH浓度。实验中固定 H2O2和Fe2+投加量分别为1.994 mL/L和0.543 g/L(H2O2:Fe2+=10),通过改变反应体系的pH研究Fenton反应的COD去除变化,结果如图4所示。
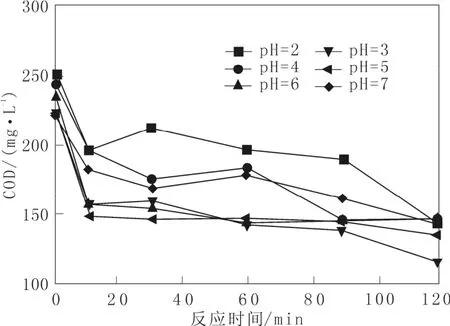
图4 不同pH条件下出水COD的变化Fig. 4 Change of COD with pH
从图4中看出,随着反应时间的增加出水COD逐渐降低。pH=3时,Fenton反应氧化效率最高,pH=2次之,pH在4~6时COD的去除情况没有明显变化,pH>7时氧化效率进一步降低。该结果证实pH=3为本研究体系发生 Fenton反应的最佳条件。Kang和Hwang在研究Fenton反应处理垃圾渗滤液时系统的研究了氧化和混凝两种作用机理对于 COD去除率的贡献[14]。结果表明在pH=2.5~4时氧化的效率最高(40%以上),而一旦 pH>4,氧化作用迅速下降,到pH=7时氧化效率低于10%;对于Fenton反应过程中的混凝作用来说,COD最佳去除条件为pH=4~5左右,去除率在20%以上,而当pH=3时,混凝作用引起的COD去除率不足20%。本研究中COD的最佳去除效果发生在pH=3附近,由此证明此时主要的有机物去除机理为氧化而非混凝。
2.5 反应温度的影响
通常温度升高对化学反应均有促进作用,主要是由于温度升高可以降低化学反应的活化能,加速化学反应的速率。在 H2O2投加量为 1.994 mL/L,FeSO4·7H2O投加量为0.543 g/L,反应体系pH=3的条件下,研究了反应温度对于Fenton反应的影响,结果如图5所示。
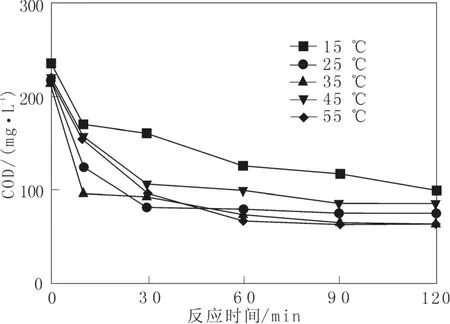
图5 不同反应温度条件下出水COD的变化Fig. 5 Change of COD with reaction temperature
从图5中看出,随着温度的升高,COD的去除率逐渐增加。25~55 ℃条件下的出水COD去除率相差不大,但均明显高于15 ℃时的情况。反应120 min后,15~55 ℃条件下氧化出水的COD去除率分别为61.3%、70.0%、72.7%、69.4%和72.3%。可见,在45 ℃和55 ℃条件下,Fenton氧化的去除率已不再升高,与 35 ℃相比反而略有降低。这主要是由于温度较高会加速体系中H2O2分解为H2O和O2的速率,从而影响 Fenton氧化的效率。25~35 ℃为Fenton氧化较为理想的反应温度条件。此外,15~55℃条件下氧化 120 min后出水的 H2O2浓度分别为120.0 ,102.1, 34.0 ,17.0 ,8.5 mg/L和0。随着温度的逐渐升高,出水中的H2O2的浓度逐渐降低,进一步证实较高的温度对于H2O2自身分解有显著促进作用。
2.6 Fenton反应前后难降解有机物的变化
为了表征Fenton氧化处理焦化废水生化出水前后的变化,在pH=3,投加H2O2和FeSO4·7H2O分别为1.994 mL/L和0.543 g/L,室温下反应120 min进行Fenton氧化,将反应出水进行GCMS测试,并与原生化出水进行比较。通过GCMS谱库检索,原生化出水中检测到的难降解有机物主要为:2,5-二甲基苯酚、3,5-二甲基苯酚、2,4,6-三甲基苯酚、2-甲基喹啉、3,6-二甲基吲唑、1(2H)-异喹啉、吖啶、咔唑等,而Fenton氧化出水没有检测出相应的有机物,反应后水质清澈,无刺鼻气味,可见原有的难降解有机物如二甲基苯酚和大部分喹啉类化合物等得到了完全的去除。
3 结 论
Fenton氧化反应迅速,10 min内可以迅速降低焦化废水生化处理出水的COD。增加H2O2的投加量可使 COD去除率显著增加。较低 Fe2+投加量去除COD的效果不佳,在H2O2:Fe2+为10、5和2的条件下COD去除效果明显。反应体系pH=3时具有最佳的COD去除效果。25~35 ℃为Fenton氧化较为理想的反应温度条件。GCMS测试表明Fenton氧化可有效去除二甲基苯酚和大部分喹啉类化合物等难降解有机物。在 H2O2投加量为 1.994 mL/L,FeSO4·7H2O投加量为 0.543 g/L,反应体系 pH=3,温度为 35 ℃的条件下,反应出水 COD低于 100 mg/L,其去除率可达72.7%。研究表明Fenton氧化是深度处理焦化废水的一种有效方法。
[1] Qian Y, Wen Y, Zhang H. Efficiency of pre-treatment methods in the activated sludge removal of refractory compounds in coke-plant wastewater [J]. Water Research, 1994, 28(3):701-710.
[2] Zhang M, Tay J H, Qian Y, et al. Coke plant wastewater treatment by fixed biofilm system for COD and NH3-N removal [J]. Water Research,1998, 32(2):519-527.
[3] Goi A and Trapido M. Hydrogen peroxide photolysis, Fenton reagent and photo-Fenton for the degradation of nitrophenols: a comparative study [J]. Chemosphere, 2002, 46: 913-922.
[4] Liou M J, Lu M C, Chen J N. Oxidation of explosives by Fenton and photo-Fenton processes [J]. Water Research, 2003, 37: 3172-3179.
[5] Xu X R, Li H B, Wang W H, et al. Degradation of dyes in aqueous solutions by the Fenton process [J]. Chemosphere, 2004, 57: 595-600..
[6] Chen W S, Juan C N, Wei K M. Mineralization of dinitrotoluenes and trinitrotoluene of spent acid in toluene nitration process by Fenton oxidation [J]. Chemosphere, 2005, 60: 1072-1076.
[7] Szpyrkowicz L, Juzzolin C, Kaul S. A comparative study on oxidation of disperse dyes by electrochemical process, ozone, hypochlorite and Fenton reagent [J]. Water Research, 2001, 35(9): 2129-2136.
[8] 覃舟. 高级氧化技术处理高浓度化纤废水(液)的研究[D]. 陕西:长安大学硕士学位论文, 2004.
[9] 赖鹏, 赵华章, 叶正芳, 倪晋仁, 曾明. 生物滤池A/O工艺处理焦化废水研究[J]. 环境科学, 2007, 28(12): 2727-2733.
[10]Lai P, Zhao H Z, Wang C, et al. Advanced treatment of coking wastewater by coagulation and zero-valent iron processes [J]. Journal of Hazardous Materials, 2007, 147: 232-239.
[11]Lai P, Zhao H Z, Ye Z F C, et al. Assessing the effectiveness of treating coking effluents using anaerobic and aerobic biofilms [J]. Process Biochemistry, 2008, 43: 229-237.
[12] 杨岳平, 吴星义, 徐新华,等. 印染废水的UV-Fenton氧化处理研究[J]. 高效化学工程学报, 2001, 15(3): 242-247.
[13]许海燕, 李义久, 刘亚菲. Fenton-混凝催化氧化法处理焦化废水的影响因素[J]. 复旦学报(自然科学版), 2003, 42(3): 440-444.
[14]Kang Y and Hwang K. Effects of reaction conditions on the oxidation efficiency in the Fenton process [J]. Water Research, 2005, 34(10):2786-2790.
Study on Advanced Treatment of Coking Wastewater by Fenton Oxidation Process
LAI Peng1,ZHAO Hua-zhang2
(1. China Development Bank Sichuan Branch, Sichuan Chengdu 610027, China;
2. Department of Environmental Engineering, Peking University, Beijing 100871, China)
Advanced treatment of coking wastewater by Fenton oxidation process was studied. The results show that the COD can be removed quickly by Fenton oxidation,dosages of H2O2and Fe2+can obviously affect the COD removal efficiency. The best COD removal efficiency can be gotten when pH=3. When dosages of H2O2and Fe2+are 1.994 mL/L and 0.543 g/L respectively, the COD can be removed to less than 100 mg/L at pH=3 and 35 ℃ ,and the COD removal efficiency is up to 72.7%. Fenton oxidation process can effectively remove refractory organic compounds in coking wastewater. Therefore, Fenton oxidation process is an effective means for advanced treatment of coking wastewater.
Fenton oxidation; Coking wastewater; Advanced treatment; Refractory organic compounds
X 703
A
1671-0460(2012)01-0011-05
国家自然科学基金资助项目,项目号:20607001。
2011-11-28
赖鹏(1980-),男,四川成都人,工程师,博士研究生,2008年毕业于北京大学环境工程专业,研究方向:难降解工业废水处理技术与理论,第一作者身份发表SCI论文3篇。E-mail:laipengpku@gmail.com,电话:028-86029896。
