2006—2010年药品不良反应报告和监测工作质量评价
2012-11-06李小东安徽省淮北市人民医院药剂科安徽淮北235000
李小东(安徽省淮北市人民医院药剂科,安徽淮北 235000)
药品不良反应(adverse drug reaction,ADR)报告和监测是指ADR的发现、报告、评价和控制的过程[1]。据世界卫生组织(WHO)专家组报告,全球死亡患者有1/3不是死于自然疾病本身,而是死于不合理用药。国家食品药品监督管理局(SFDA)报告我国每年有250余万人因ADR而入院,而住院患者ADR发生率占住院患者总人数的10% ~20%[2]。随着ADR报告和监测工作在我国的不断深入,临床对ADR严重性和危害性的认识也在不断提高。为了解某三甲医院ADR报告和监测工作的实际情况、发现工作中存在的不足、提出相应的对策、进而为提高工作水平提供依据,现对该院2006—2010年报告的ADR进行回顾性分析。
1 资料与方法
1.1 资料来源与处理
检索全国药品不良反应监测网络中该院2006—2010年上报的ADR报告,选取患者一般资料、报告单位部门、报告人、报告人职业、级别、不良反应的结果、报告人评价等字段生成Excel表格,按年度下载保存数据,并采用SPSS1 7.0软件进行统计分析。
1.2 数据分析
对数据中的患者一般资料、报告人科室分布、报告人职业结构、ADR级别分类、ADR转归、关联性评价等内容进行回顾性分析。
2 结果
2.1 一般资料
2006—2010年该院上报ADR共1 527例,其中男性808例,女性719例,各年度性别分布经统计学分析,差异无统计学意义(P>0.05)。ADR年度报告数量呈波浪式上升,ADR发生率最低为1.19%,最高为2.36%,低于SFDA报告的我国ADR发生率,理论上存在漏报现象,见表1。
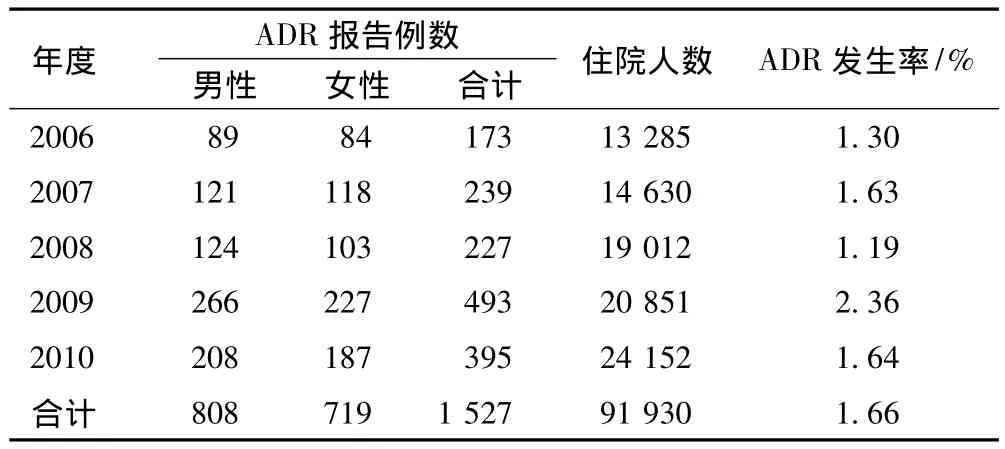
表1 2006—2010年ADR报告的基本情况Tab1 Basic situation of ADR reports during 2006-2010
2.2 ADR报告呈报科室分布
5年来该院共有27个临床和医技科室呈报ADR,呈报科室分布不均衡,排序前10位科室呈报的总例数为1 124例,构成比为73.9%,见表2。有些较大科室(表2未列出)如妇产科、神经内科、儿科、肿瘤内科、心脑血管内科呈报例数偏少,5年来口腔科仅有1例报告、皮肤科无1例报告,即使同一科室不同年度呈报例数及构成比也不均衡,如脑外科、门诊注射室、感染科均有零报告年度。
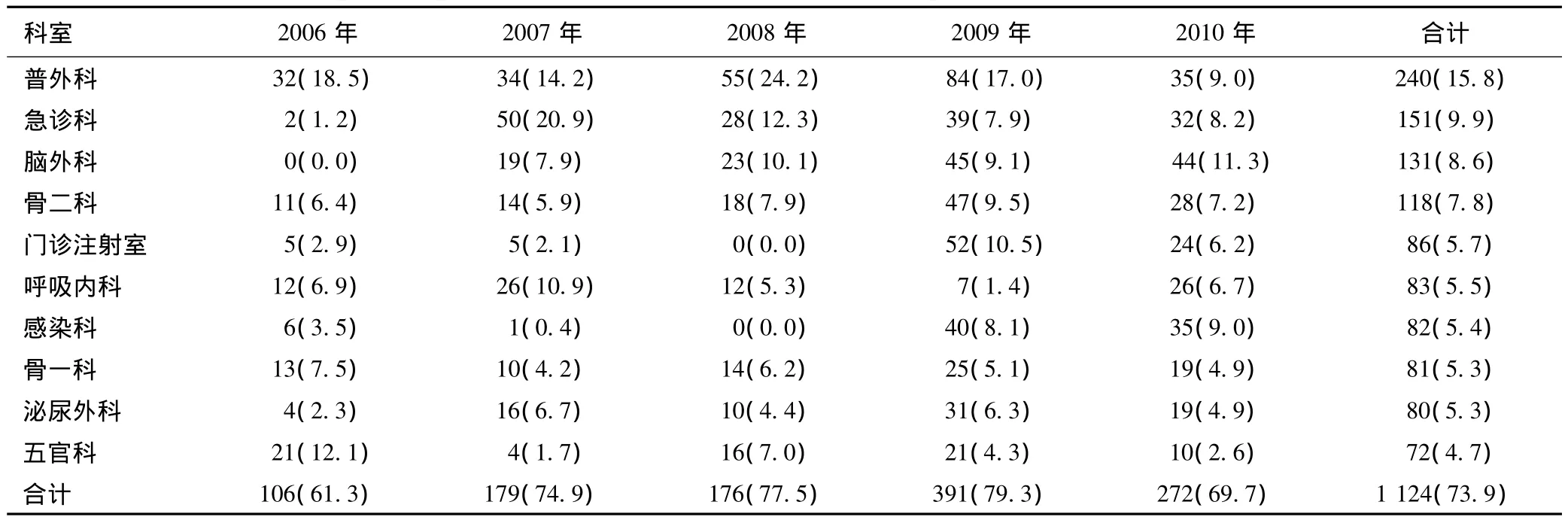
表2 2006—2010年前10位呈报ADR的科室[例(%)]Tab2 Top ten departments ranked by number of ADR reports during 2006-2010[cases(%)]
2.3 ADR报告人职业结构
该院ADR报告人职业主要为医生、护士和药师,但报告人主体为护士,5年来共呈报 ADR报告1 265例,占总数的83.1%,医生仅占14.9%,药师占2.0%。各年度职业结构经统计学分析,差异有统计学意义,2006年情况较好,医生比例达到45.7%,与其他年度比较差异显著,其余年度整体差异无统计学意义。因此,该院2006年ADR报告人职业结构相对较为合理,其余年度报告人主体为护士的情况没有明显变化,见表3。
2.4 ADR报告程度分级
该院ADR报告质量偏低,一般的占93.0%,新的、严重的合计只占7.0%,远低于WHO对该类报告应达30%的标准,接近我国目前7.1%的平均水平[3]。各年度新的、严重的ADR报告率经统计学分析,差异有统计学意义;2007年新的、严重的ADR报告率达19.3%,在5年中情况最好,其他年度与之比较,差异均有统计学意义,见表4。
2.5 ADR的结果与转归
全部ADR经停药或治疗处理后,99.9%的患者治愈或好转,仅有2例患者有后遗症,无死亡病例,情况较好,各年度治愈和好转率经统计学分析,差异无统计学意义,说明该院ADR的结果与转归情况较好,也有可能与新的和严重的ADR报告较少有关,见表5。
2.6 ADR关联性评价
关联性评价经统计学分析,差异有统计学意义;2006年有69.3%判定为肯定,其余年度不到2%,2010年高达56.2%的无法评价,说明该院报告人关联性评价各年度变化较大,见表6。

表3 2006—2010年ADR报告人职业结构Tab3 Occupational structure of ADR reports during 2006-2010
3 讨论
3.1 质量评价及原因分析
3.1.1 ADR报告率不高,有一定的漏报现象:该院近5年来ADR报告病例数虽然显著增加,但住院人次也显著增加,报告率在2009年最高,达到2.36%,其余年度变化趋势不明显。主要原因可能有以下几点:(1)自愿报告制度的缺陷使医护人员缺乏积极性,有漏报现象;(2)部分ADR引起的临床症状与疾病本身较难界定,容易漏报;(3)不合理用药导致的ADR不愿上报,怕承担责任。
3.1.2 呈报科室分布不均衡,部分科室不同年度报告率变化较大:该院部分科室报告数量与科室规模不协调,甚至常年零报告。除门诊注射室外,门诊几乎无报告,部分科室不同年度报告构成比差别较大。据文献报道[4,5],皮肤及其附件损害居ADR前3位,而就诊科室应首选皮肤科,理论上皮肤科不仅能够发现该院发生的ADR,还应该能够发现患者在家自我药疗时发生的 ADR,应是ADR报告的主要力量,姜玲、穆惠荣等[6,7]也报道皮肤科报告例数较多,而该院5年来却是零报告。儿童处于特殊的生理时期,各系统、器官功能不健全,肝脏对药物的分解作用及肾脏对药物的排泄能力低下,免疫机制尚未健全,因此儿童时期对药物的不良反应耐受力比较弱,发生ADR的机会大大高于成人[8]。据2006年参加国家ADR监测的儿童医院报告的相关资料显示,儿童用药不良反应发生率达12.9%,其中新生儿为24.4%,而成人仅为6.9%[9],所以儿科也应该是ADR报告和监测的重点科室,而该院儿科报告数量5年来仅为33份,占全部数量的2.2%。造成的原因可能有3点:(1)各科室重视程度不同导致呈报科室分布不均衡;(2)有些科室(如皮肤科)主要为门诊患者且数量较大,医生没有足够时间诊断ADR;(3)门诊患者用药多为外用或口服,不在本院使用,监测较困难;(4)科室人员岗位调整,导致不同年度报告率变化较大。
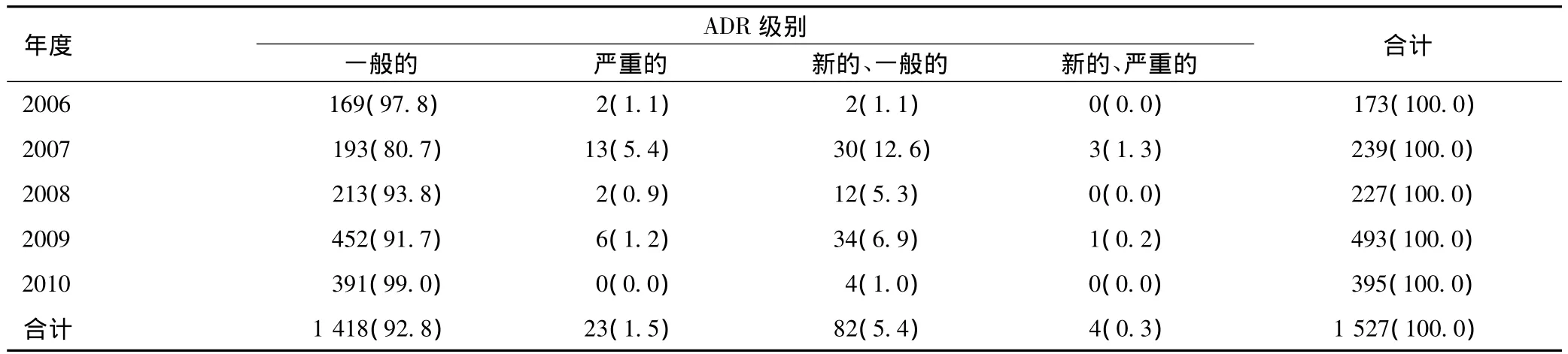
表4 2006—2010年ADR报告分级[例(%)]Tab4 Grading of ADR reports during 2006-2010[cases(%)]
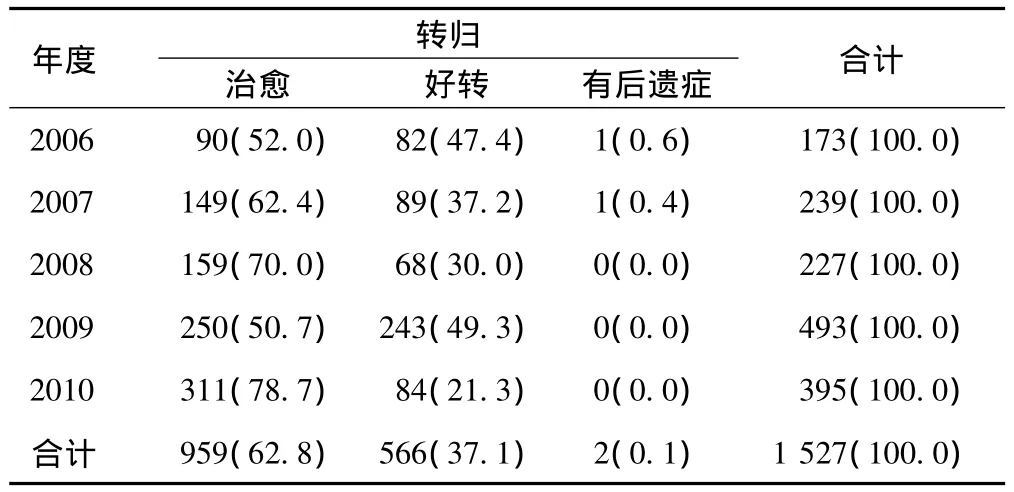
表5 2006—2010年ADR转归情况[例(%)]Tab5 Outcome of ADR during 2006-2010[cases(%)]
3.1.3 呈报人员职业结构不合理:该院医生在2006年ADR报告和监测工作开展初期还能够积极参与(构成比为45.7%),基本与护士持平(构成比为48.5%),但随后便大幅度下滑,护士充当了该项工作的主力军,药师主动查阅病历发现的ADR也减少。造成这种现象主要有下列原因:(1)医生对ADR报告和监测工作缺乏热情和动力;(2)从事ADR监测工作的药师数量有限且要承担其他临床药学工作,无足够时间参与查房、查阅病历。
3.1.4 ADR报告质量偏低:新的、严重的ADR报告数量是ADR报告和监测工作的主要质量指标之一,该院2007年报告质量较高,构成比达19.3%,远超全国平均水平但低于WHO的标准,其余年度构成比较低,甚至2010年只有0.3%。主要原因有:(1)新的、严重的ADR判定相对较复杂,报告人缺乏专业培训;(2)医护人员对于较严重的ADR上报存在顾虑,怕引起医患纠纷。

表6 2006—2010年ADR的关联性评价[例(%)]Tab6 Relevance evaluation of ADR during 2006-2010[cases(%)]
3.1.5 ADR的结果与转归:该院ADR病例5年来仅有2例存在后遗症,其余全部治愈或好转,这一定程度上说明该院在ADR发生后能够及时应对和正确处理,主要因为该院一直高度重视医疗质量工作。
3.1.6 关联性评价质量不高:关联性评价的准确性是ADR报告和监测工作的重要一环,该院各年度关联性评价结果不稳定,2006年有91.3%的报告评价结果为肯定或很可能,质量较好,但2008年有38.3%的报告待评价,2010年有高达56.2%的报告无法评价。可能和下列原因有关:(1)报告人工作不细致,报告表填写不详细,使关联性评价工作无法进行;(2)2006年医生参与热情较高,当年关联性评价工作质量较好,但随后年度护士作为该项工作的主体,由于其专业知识和医生比较有些欠缺,导致关联性评价工作质量下滑。
3.2 对策
3.2.1 加强ADR报告和监测工作的制度建设:(1)设立多学科ADR报告和监测专家委员会,为各科室医护人员提供专家咨询服务,提高报告质量,同时监督医护人员,降低漏报率;(2)医院对ADR报告持鼓励态度,建立报告激励机制,激发医护人员的责任感,形成良好的风气,并将报告和监测工作纳入医疗质量考评;(3)根据医院用药的现状,制定医院内部《药品不良反应重点报告和监测药物目录》,加强对特殊人群和特殊药物的ADR监测;(4)增加专职药师的配置,主动参与查房、查阅病历;(5)建立医院ADR网络报告系统,简化报告程序,设立ADR咨询门诊和咨询热线,方便医护人员的咨询和患者ADR的就诊处理。
3.2.2 加强医护人员的业务知识培训:(1)加强医护人员ADR相关法律法规和基础知识的培训,提高医护人员对ADR的认识,解除医护人员的疑虑。如组织医护人员学习新版《药品不良反应报告和监测管理办法》、合理用药、药物相互作用等基础知识;(2)加强医护人员ADR专业知识的培训,如正确理解ADR的定义、分类、监测方法,掌握报告表的填写方法、因果关系分析方法等。
ADR给人类健康和生命安全带来的危害已日益受到人们的关注,ADR报告和监测是加强药品管理、促进临床合理用药及保障患者用药安全的有效手段,目前该院ADR报告和监测工作仍存在报告率不高、呈报科室分布不均衡、呈报人员职业结构不合理、报告质量偏低、关联性评价质量不高等不足。该项工作仍处于初级阶段,需要不断完善和改革,因此,推动该院ADR报告和监测工作质量不断提高仍是全体医务人员的努力方向。
[1]卫生部.药品不良反应报告和监测管理办法[S].卫生部令第81号.
[2]刘 红,陈孟云,张艳华.我院112例药物不良反应报告分析[J].中国医院药学杂志,2009,29(5):429.
[3]姜 玲,杜德才,沈爱宗,等.我院2002—2006年新的和严重的药品不良反应报告分析[J].中国药房,2008,19(14):1095.
[4]冯英力,许晓玲.我院3437例药品不良反应报告分析[J].中国药房,2010,21(34):3238.
[5]赵陶丽,赵志刚,庄 洁.我院258例药品不良反应报告回顾性分析[J].中国医院用药评价与分析,2010,10(8):748.
[6]姜 玲,沈爱宗,杜德才,等.990份药品不良反应报告描述性分析[J].中国药师,2007,10(7):684.
[7]穆惠荣,王继美.我院2006年药品不良反应报告回顾性分析[J].中国药房,2007,18(32):2534.
[8]肖顺林,罗宏丽,冯碧敏.240例儿童药品不良反应报告分析[J].中国医院用药评价与分析,2011,11(1):67.
[9]赵瑞玲,吴金红,高明娥,等.儿童用药导致严重不良反应/事件的现状及影响因素分析[J].中国医院药学杂志,2010,30(19):1700.
