青藤碱-环糊精包合工艺的优化及包合常数测定
2012-10-28朱士龙林红卫段友构
朱士龙,李 勇,林红卫,段友构,*
(1.吉首大学化学化工学院,湖南 吉首 416000;2.怀化学院化学化工系,湖南 怀化 418008;3.民族药用植物资源研究与利用湖南省重点实验室,湖南 怀化 418008)
青藤碱-环糊精包合工艺的优化及包合常数测定
朱士龙1,李 勇1,林红卫2,3,段友构1,*
(1.吉首大学化学化工学院,湖南 吉首 416000;2.怀化学院化学化工系,湖南 怀化 418008;3.民族药用植物资源研究与利用湖南省重点实验室,湖南 怀化 418008)
目的:考察青藤碱与环糊精形成包合物的最佳条件,测定青藤碱与不同环糊精的包合常数并进行体外释放研究。方法:通过单因素及正交试验确定青藤碱与不同环糊精形成包合物的最佳条件,并在此条件下利用相溶解度法测定青藤碱与β-环糊精、羟丙基-β-环糊精、γ-环糊精的包合常数,对包合物进行体外释放试验研究。结果:青藤碱与不同环糊精形成包合物的最佳条件为物质的量的1:1、包合温度50℃、包合反应3h、包合反应时溶液pH7,青藤碱与β-环糊精、羟丙基-β-环糊精、γ-环糊精的包合常数分别为501.1、150.0、600.3L/mol。结论:青藤碱与环糊精可以形成1:1型稳定的包合物,以环糊精为载体制备的不同青藤碱-环糊精包合物相对于青藤碱具有明显的缓释作用。
青藤碱;环糊精;包合常数;正交试验设计;工艺优化
环糊精是环糊精葡萄糖基转移酶(cyclodexrtin glucosyl transferase,CGTaes)降解淀粉的产物。环糊精作为主体模型可以和不同系列的客体分子发生包合作用[1-2],形成的包合物分子在物理、化学及生物活性等性质上会发生很大改变[3-5],环糊精的这种包合特性已广泛应用于食品、保健品、医药和化妆品等领域[6-10]。
青藤碱(sinomenine,SN)是从天然产物青风藤中提取的一种生物活性成分。具有抗炎、免疫抑制、镇痛、降压、抗心律失常等多种生物活性[11-13],目前广泛应用于保健品、医药工业。青藤碱本身易分解,对碱、光、热不稳定[14],青藤碱存在的这些缺点对其作为药品和保健品的贮存和应用带来了一定阻碍。本实验尝试利用环糊精对青藤碱分子进行包合,通过单因素及正交试验确定青藤碱与不同环糊精形成包合物的最佳条件,在此条件下利用相溶解度法测定青藤碱与β-环糊精、羟丙基-β-环糊精、γ-环糊精的包合常数,并对包合物进行体外释放研究,为青藤碱现有的剂型改进提供参考。
1 材料与方法
1.1 材料与试剂
盐酸青藤碱(批号100802,含量99.12%) 陕西森弗生物技术有限公司;β-环糊精(β-CD)(批号090412,含量98.00%) 陕西礼泉化工有限实业公司;羟丙基-β-环糊精(HP-β-CD)(批号100201,含量99.00%)、γ-环糊精(r-CD)(批号100701,含量98.50%) 上海源叶生物科技有限公司;氯霉素对照品 湖北省药品检验所提供;乳糖、微晶纤维素 天津市巴斯夫化工有限公司;羟丙基甲基纤维素(HPMC K15M) 上海卡乐康包衣技术有限公司;硬脂酸镁 上海运宏辅料有限公司;甲醇为色谱纯;实验所用到的其他化学试剂均为分析纯;实验用水为二次蒸馏水。
1.2 仪器与设备
UV-2450紫外分光光度计、HPLC-10AT高效液相色谱仪(SPD-10AVP紫外检测器)、AUW120D分析天平 日本岛津公司;ZRD6-B药物溶出仪 上海黄海药检仪器厂;ZDY单冲压片机 上海第一制药机械厂;KQ3200型超声波清洗机 昆山市超声仪器有限公司。
1.3 方法
1.3.1 青藤碱与环糊精的纯化
对所购盐酸青藤碱和环糊精分别按照文献[15-16]进行纯化处理。
1.3.2 测定波长选择
分别取青藤碱、β-环糊精、羟丙基-β-环糊精、γ-环糊精,加蒸馏水溶解,以蒸馏水作为对照,分别在紫外分光光度计200~500nm进行扫描,β-环糊精、羟丙基-β-环糊精、γ-环糊精在此范围内均无吸收,青藤碱在265nm处有较大吸收,所以选择265nm为青藤碱测定波长。
1.3.3 标准曲线的制备
精密移取不同体积的青藤碱标准液至100mL容量瓶中用蒸馏水定容,配制一系列不同浓度的标准溶液。以蒸馏水为空白,在波长为265nm处测定吸光度,以吸光度(A)对青藤碱浓度(c)绘制标准曲线。所得线性回归方程为:A=0.8580c+0.0062,r=0.9999,说明青藤碱在0.2~5.0mmol/L内线性关系良好。
1.3.4 环糊精与青藤碱包合物的制备
环糊精与药物客体分子形成包合物的制备方法有多种,本试验利用溶液共混法制备不同环糊精与青藤碱的包合物。25℃条件下,按环糊精与青藤碱物质的量比为1:1取样,在不断搅拌的条件下将青藤碱粉末缓缓加入到环糊精的饱和水溶液中,50℃条件下搅拌5h以确保包合反应进行完全。溶液经0.45μm滤膜过滤冷却至室温后置于冰箱中4℃下放置48h,溶液底部有青藤碱环糊精的包合物结晶析出。
同时,按环糊精与青藤碱物质的比1:1进行简单机械搅拌均匀,作为物理混合物。样品经干燥后备用。
1.3.5 青藤碱含量测定方法
按照文献[17]对包合物中的青藤碱含量进行测定。色谱条件:十八烷基硅烷键合硅胶固定相柱;流动相:甲醇-磷酸盐缓冲液(5.0×10-3mol/L,60:40,V/V);流速1mL/min;进样量10μL;柱温25℃;内标为氯霉素;灵敏度0.02AuFs;检测波长265nm。
对照品溶液:精密称取青藤碱适量溶于甲醇,ρ=0.5mg/mL;包合物溶液:精密称取不同环糊精与青藤碱包合物,溶于甲醇。溶液经0.45μm微孔滤膜过滤,取滤液。
取一定量的对照品和内标物质注入色谱仪中,测量对照品和内标物质的峰面积,计算校正因子。再取含有内标物质的青藤碱样品溶液,注入色谱仪,计算青藤碱含量;同时,进行青藤碱空白回收率测定;在测定包合物中青藤碱含量及空白回收率的基础上,可计算出包合物中实际含有青藤碱量,计算包合率。
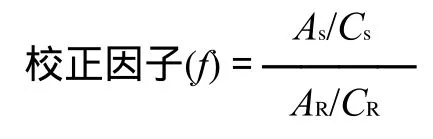
式中:As为内标物质的峰面积;AR为对照品的峰面积;CR为内标物质的浓度;Cs为对照品的浓度。
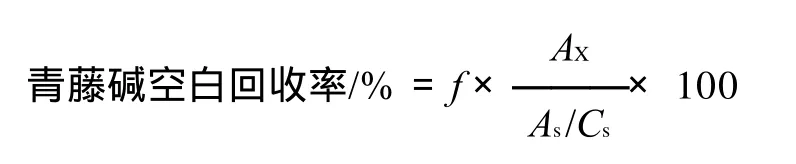
式中:AX为样品峰面积;Cx为样品的浓度; As为内标物质峰面积;Cs为内标物质的浓度;f为校正因子。

1.4 青藤碱-环糊精包合工艺条件的单因素及正交试验考察
因素水平的选择:根据预试验及文献[18],青藤碱与环糊精的配比、包合时间、包合温度及溶液pH值的选择对包合物的形成有较大影响。因此选择上述4项为考察因素,分别进行单因素及正交试验设计。
单因素试验:按照1.3.3节中青藤碱与环糊精包合物的制备方法分别考察青藤碱与环糊精的配比、包合时间、包合温度及溶液pH值等单因素对包合反应的影响。
正交试验:在单因素试验基础上,以上4因素,各取3个水平,进行青藤碱-环糊精包合工艺正交试验,因素水平见表1。

表1 青藤碱-环糊精包合工艺正交试验因素水平Table 1 Factors and levels for orthogonal array design
1.5 环糊精对青藤碱的增溶作用
分别配制不同浓度梯度的β-环糊精溶液、羟丙基-β-环糊精溶液、γ-环糊精溶液,将纯化后的青藤碱加入使之达到饱和,溶液经0.45μm微孔滤膜过滤,稀释相同倍数后利用紫外吸收光谱在265nm处测定吸光度。通过测定青藤碱的含量考察环糊精的种类和浓度对青藤碱溶解度的影响。
1.6 青藤碱与β-环糊精、羟丙基-β-环糊精、γ-环糊精的包合常数测定
环糊精与客体分子形成包合物的包合常数计算方法有多种[19],通过测定包合常数可以深入探讨环糊精分子对青藤碱的包合作用强度,并比较不同环糊精分子对青藤碱包合的差别。经查阅相关资料结合本实验实际情况选取相溶解度法测定青藤碱与不同环糊精包合物的包合常数。分别配制不同浓度梯度的不同环糊精溶液,加青藤碱使之达到饱和,溶液经0.45μm微孔滤膜过滤,稀释相同倍数后利用紫外吸收光谱在265nm处测定其吸光度。
1.7 不同青藤碱-环糊精包合物的释放度测定
为了更进一步探究不同青藤碱-环糊精包合物与青藤碱的性质差别,按照缓释片制备处方分别制备了不同样品的缓释片并进行体外释放试验研究。体外释放试验按照缓释剂指导原则[17]进行。精密称取含相同青藤碱量的不同包合物与环糊精物质的量比1:1的物理混合物以及青藤碱按β-CD包合物缓释片处方制备缓释片,所有样品缓释片均按照释放度测定法参考文献[17]方法,溶出介质为磷酸盐缓冲液,温度(37.5℃±0.5℃),搅拌转速100r/min,分别在 5、10、15、20、30、60、120、180、300min时定位取样5mL(同时补充等量相同溶出介质),经0.45μm微孔滤膜过滤后取续滤液适当以磷酸盐缓冲液稀释,在波长265nm处测定吸光度(A),通过标准曲线计算不同样品中青藤碱含量并计算青藤碱的累计释放率。
2 结果与分析
2.1 不同条件对青藤碱-环糊精包合工艺的影响
2.1.1 单因素试验结果
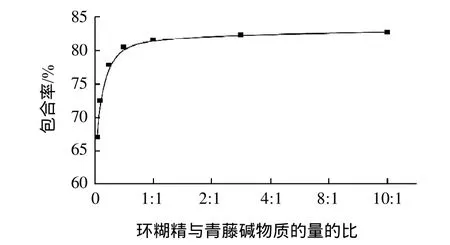
图1 环糊精与青藤碱的配比对包合率的影响Fig.1 Effect of molar ratio of cyclodextrins to sinomenine on inclusion rate
由图1可知,随着环糊精比例的升高,青藤碱包合率也随着升高。开始阶段包合率上升速度很快,当青藤碱与环糊精物质的量的比达到1:1左右时,再增加环糊精的比例,包合率不再增加,推测其可能原因是环糊精对青藤碱分子进行包合时,青藤碱分子进入环糊精分子的空穴中,环糊精和客体分子青藤碱之间需保持一定的主客体比,当青藤碱与环糊精物质的量的比达到1:1时,青藤碱分子基本上已经被包合。
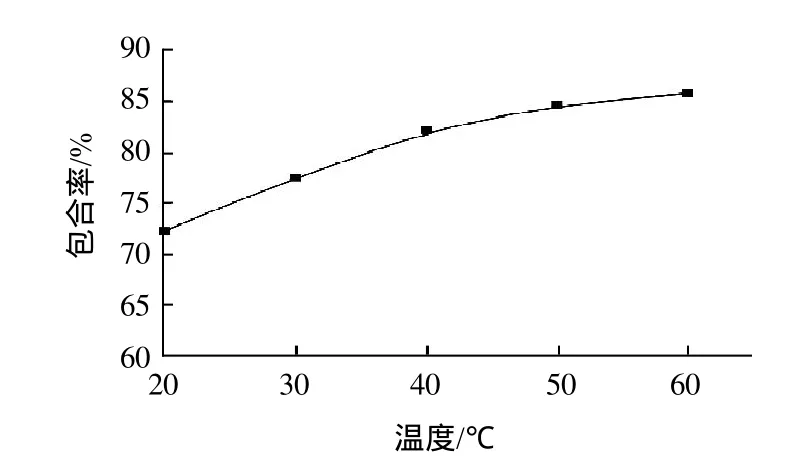
图2 包合温度对包合率的影响Fig.2 Effect of inclusion temperature on inclusion rate
由图2可知,在一定范围内,随着温度的上升包合率呈上升趋势。这是因为升高温度可以加快青藤碱分子和环糊精分子的运动频率,加快包合反应的速度,但由于青藤碱分子不稳定,超过80℃后青藤碱分子易发生分子重排,溶液变成黄色,故包合反应时温度一般不高于60℃。
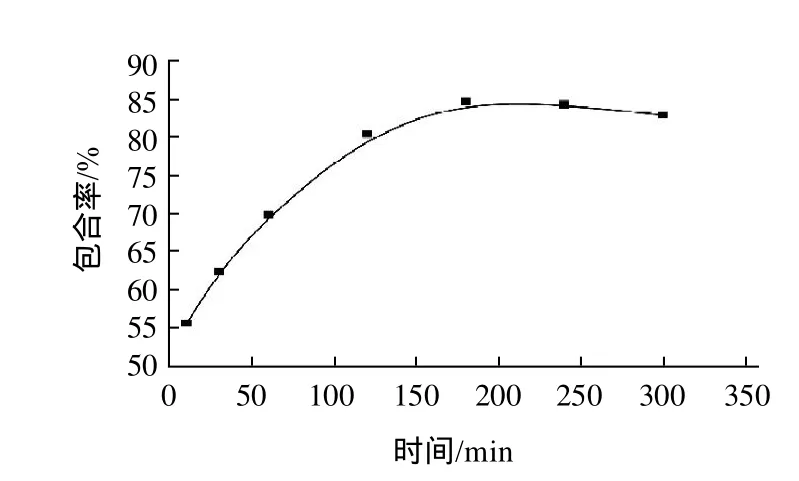
图3 包合时间对包合率的影响Fig.3 Effect of inclusion time on inclusion rate
由图3可知,增加反应时间可以提高青藤碱分子与环糊精分子的包合率,但时间超过300min时,包合率反而下降,推测其可能原因是青藤碱分子与环糊精分子进行包合时是在电磁搅拌的状态下进行的,需要经过一定时间才会反应完全。包合物分子大多以分子间作用力结合,这种结合力比较弱,当大多数青藤碱分子已经被包合,继续增加搅拌时间的话可能会破坏青藤碱-环糊精包合物分子间的作用力,使已经包合的青藤碱-环糊精分子发生离解,降低包合率。
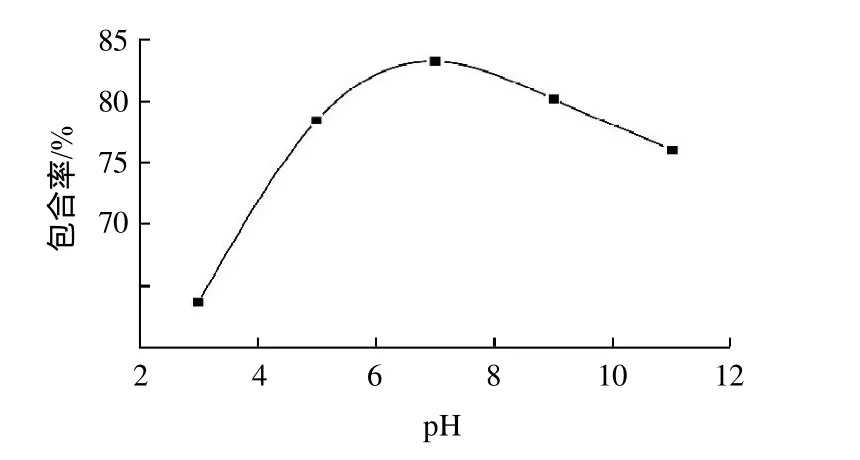
图4 溶液pH值对包合率的影响Fig.4 Effect of medium pH on inclusion rate
由图4可知,酸性条件和碱性条件对青藤碱与环糊精的包合作用均不利,原因是酸性或碱性条件下青藤碱分子中的羧基和羟基会发生电离,影响了与环糊精分子的包合作用。当溶液pH7左右时,包合率达到最大值,说明青藤碱与环糊精分子的包合反应适宜在中性条件下进行。
2.1.2 正交试验结果与分析
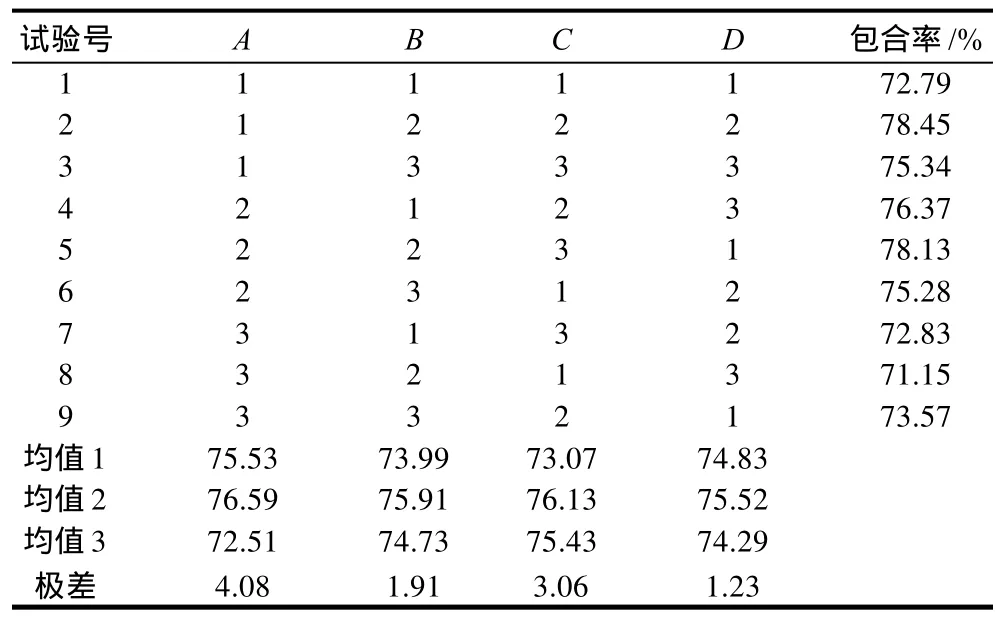
表2 青藤碱-环糊精包合工艺正交试验设计及结果Table 2 Orthogonal array design and experimental results
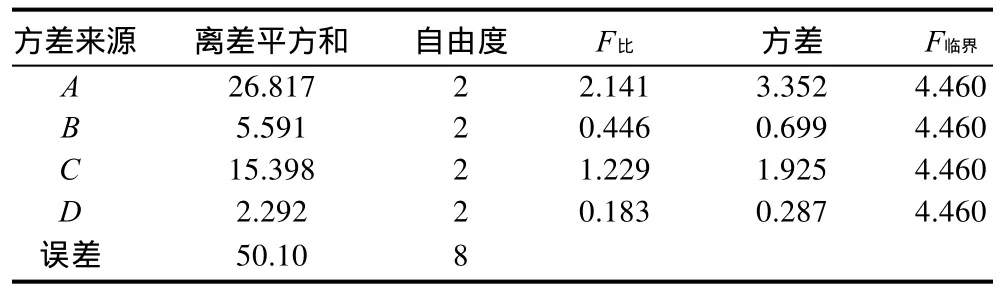
表3 方差分析Table 3 Analysis of variance for the experimental results of orthogonal array design
由表2、3可知,影响青藤碱与环糊精包合因素大小依次为A>C>B>D;方差分析表明,A因素对青藤碱的包合影响最大。由直观分析和效应曲线图可得最佳工艺条件为A2B2C2D2,即青藤碱与环糊精配比为1:1、恒温40℃、电磁搅拌3h、pH7。
2.2 环糊精对青藤碱的增溶作用
将1.5节中不同样品经紫外分光光度计检测后所得环糊精对青藤碱的增溶作用的光谱如图5所示。
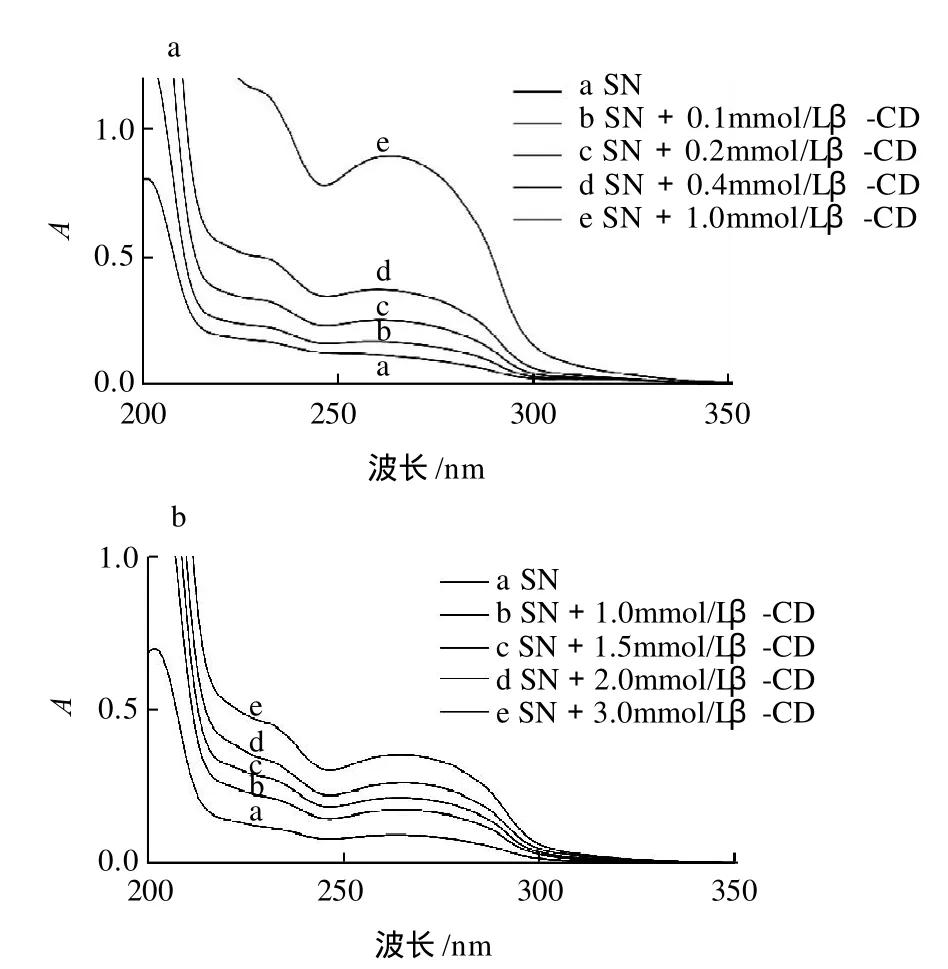
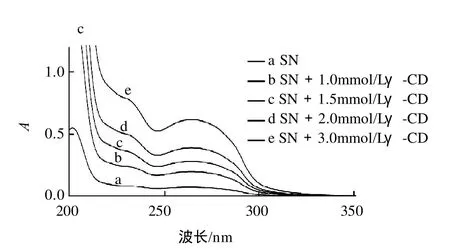
图5 β-环糊精(a)、羟丙基-β-环糊精(b)、γ-环糊精(c)分别对青藤碱增溶的光谱图Fig.5 UV absorption spectra showing the solubilizing effect of cylcodextrins on sinomenine
由图5可知,随着环糊精浓度的增加,青藤碱的溶解度逐渐增大,β-环糊精、羟丙基-β-环糊精、γ-环糊精对青藤碱均有明显的增溶作用,β-环糊精、γ-环糊精对青藤碱的增溶作用明显好于羟丙基-β-环糊精。
2.3 青藤碱与β-环糊精、羟丙基-β-环糊精、γ-环糊精的包合常数测定
由图6可知,青藤碱的溶解度随环糊精的加入呈线性增加,根据Benesi-Hildebrand公式,确定青藤碱与环糊精的包合计量比为1:1,则相溶解度方程为:
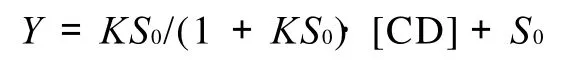
式中:[CD]为环糊精的总浓度;Y为CD存在下客体青藤碱的总浓度;S0为客体青藤碱分子的固有溶解度(曲线的截距);K为包结物的形成常数。以客体浓度对CD浓度作图,如图6所示,由图中斜率和截距可获得包结物的形成常数K。K=斜率/截距(1-斜率)。
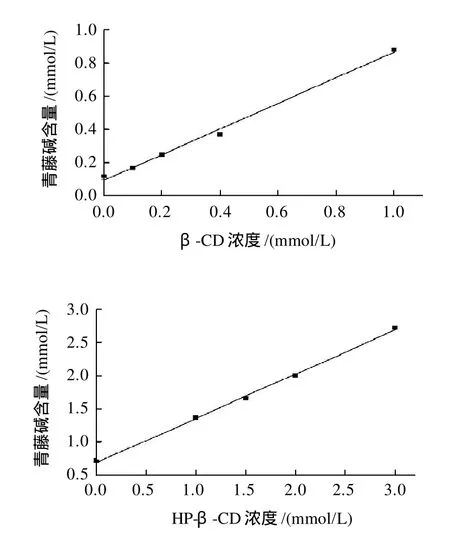
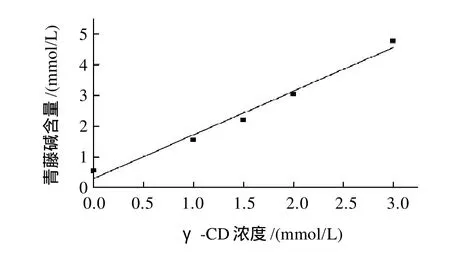
图6 青藤碱在不同环糊精溶液中的相溶解度图(25℃)Fig.6 Effect of different cyclodextrins on the solubility of sinomenine in water at 25 ℃
青藤碱与不同环糊精形成的包合常数由表4给出,青藤碱与β-环糊精、羟丙基-β-环糊精、γ-环糊精的包合常数分别为501.1、150.0、600.3。

表4 青藤碱与不同环糊精的包合常数Table 4 Inclusion constants of sinomenine complexes with different cylcodextrins
2.4 包合物的释放度测定
将青藤碱、不同物理混合物、不同环糊精包合物按照1.7节中体外释放方法进行实验后,所得青藤碱的累计释放率按下式计算:
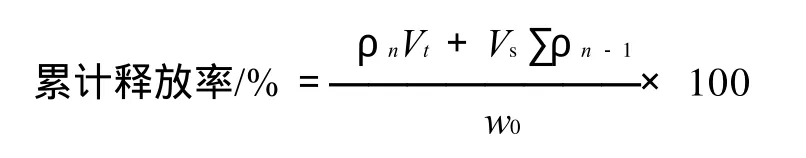
式中:w0为药物含量/mg;Vt为介质体积/mL;Vs为取样体积/mg;ρn为t时间第n次测定时青藤碱的质量浓度/(mg/mL);∑ρn-1为前n-1次测出的青藤碱质量浓度之和。体外释放测定结果如图7所示。
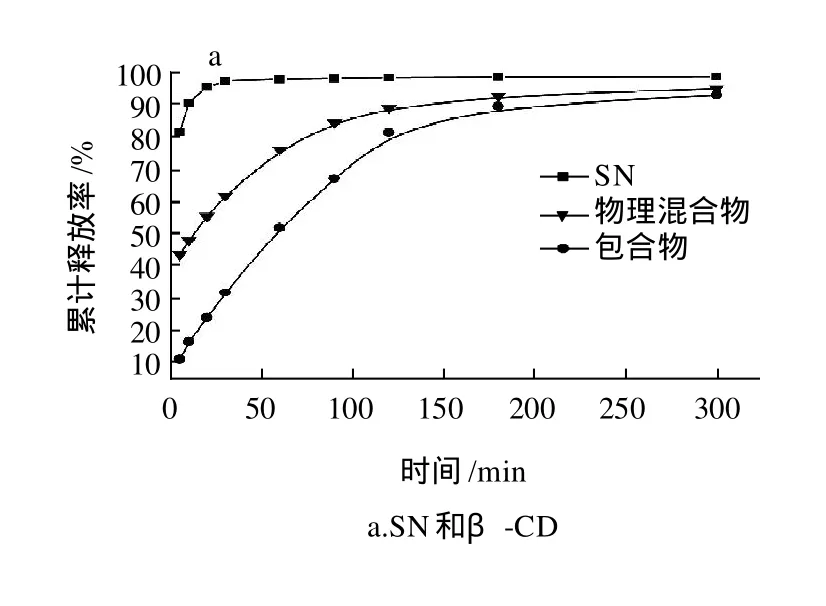
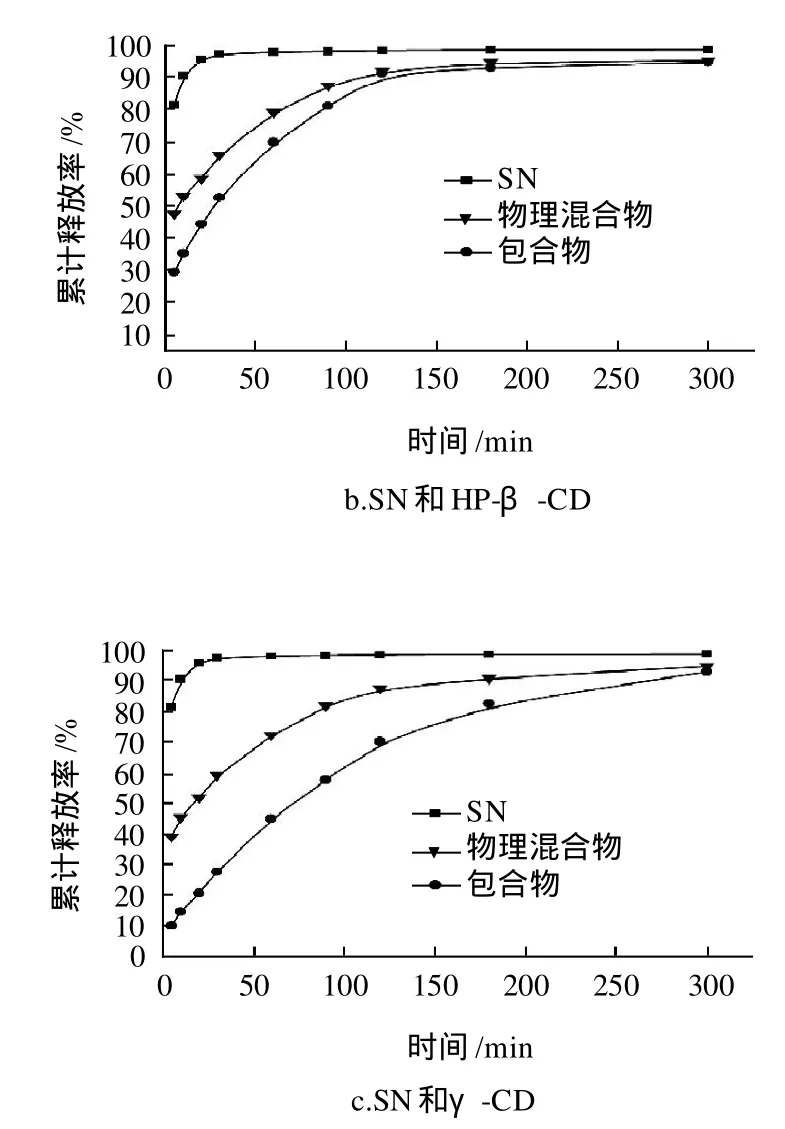
图7 青藤碱、不同物理混合物及不同包合物的累计释放度Fig.7 Cumulative releases (%) of sinomenine, physical mixtures and inclusion complexs
由图7可以看出:在300min内的9个时间点,不同环糊精包合物缓释片的累计释放率均比青藤碱显著降低,青藤碱缓释片在30min时已经基本累计释放完全,但含有相同量青藤碱的环糊精包合物缓释片的累计释放时间远大于青藤碱缓释片的累计释放时间,同样比例的青藤碱与环糊精的物理混合物虽然在一定程度上也能改善青藤碱的释放度,但其释放度效果远不及包合物。实验结果表明以环糊精为载体制备的不同青藤碱-环糊精包合物相对于青藤碱具有明显的缓释作用。
3 结 论
通过单因素及正交试验确定了青藤碱与不同环糊精形成包合物的最佳条件为青藤碱与环糊精的配比1:1、包合温度50℃、包合反应3h、包合反应时溶液pH7,并在上述最佳工艺条件下进行重复性和稳定性实验,平行试验5次,平均包合率为83.2%。利用相溶解度法测定了青藤碱与β-环糊精、羟丙基-β-环糊精、γ-环糊精的包合常数分别为501.1、150.0、600.3。制备了青藤碱、不同物理混合物及不同包合物的缓释片并进行体外释放研究。结果表明在此条件下青藤碱与环糊精可以形成较稳定的包合物,β-环糊精、羟丙基-β-环糊精、γ-环糊精均可显著增加青藤碱的溶解度,以β-环糊精、羟丙基-β-环糊精、γ-环糊精为载体制备的不同青藤碱-环糊精包合物均具有明显的缓释作用。本实验结论可为现有含青藤碱制剂的改进提供参考。
[1] 童林荟. 环糊精化学-基础与应用[M]. 北京: 科学出版社, 2001: 11-25.
[2] LI Song, PURD W C. Cyclodextrins and their applications in analytical chemistry[J]. Chem Rev, 1992, 92(6): 1457-1458.
[3] DAVIS M E, BREWSTER M E. Cyclodextrin-based pharmaceutics:past, present and future[J]. Nature Reviews Drug Discovery, 2004, 3(12): 1023-1035.
[4] 吴文娟, 陈玉珍, 谭载友. 水溶性高聚物对药物-环糊精包合作用的影响[J]. 中国药学杂志, 1999, 34(2): 99-101.
[5] 程霜, 杜凌云, 牛梅菊, 等. β-环糊精和染料木黄酮包合作用的研究[J]. 食品科学, 2006, 27(2): 94-99.
[6] SZEJTLI J, SZENTE L. Elimination of bitter,disgusting tastes of drugs and foods by cyclodextrins[J]. European Journal of Pharmaceutics and Biopharm aceutics, 2005, 61(3): 115-125.
[7] 王晓云, 姜子涛, 李荣. 环糊精及其衍生物与天然抗氧化剂杨梅素的包合作用研究[J]. 食品科学, 2008, 29(5): 125-128.
[8] MOORE E, BERGAMO R, CASLLO R. Direct compression tablets containing a series of four β-cyclodextrin complexes formedby neutralizing an acidic drug[J]. Drug Dev Ind Pharm, 2000, 26(12): 1259-1270.
[9] MONTASSIER P, DUCHENE D, POELMAN M C. Inclusion complexes of tretinoin with cyclodextrins[J]. International Journal of Pharmaceutics, 1997, 153(2): 199-209.
[10] 董峰光, 姜子涛, 李荣, 等. 环糊精及其衍生物与亮蓝包结作用的荧光光谱研究[J]. 食品科学, 2009, 30(21): 144-147.
[11] LIU Liang, EBERHARD B, DENNIS B, et al. Amelioration of rat experimental arthritis by treatment with the sinomenine[J]. Int J Immunopharmac, 1996, 18(10): 529-534.
[12] 傅绍萱. 青藤碱的药理作用Ⅱ-Ⅶ[J]. 药学学报, 1963, 10(11): 673-675.
[13] 叶仙蓉, 颜克序, 吴克美, 等. 青藤碱衍生物的合成及其抗炎镇痛活性[J]. 药学学报, 2004, 39(3): 180-183.
[14] GOTO K, SUDZUKI H. Studies on bimolecular alkaloids partⅠ-Ⅱ[J]. Bull Chem Soc Jpn., 1929(4): 107-111.
[15] 罗烈. 青藤碱衍生物的合成及镇痛抗炎作用的定量构效关系研究[D].武汉: 武汉大学, 2005.
[16] 孙聪善. β-环糊精与几种芳香族客体的包结物结构研究[D]. 天津:天津大学, 2009.
[17] 国家药典委员会. 中国药典: 二部[S]. 北京: 中国医药科技出版社,2010.
[18] 马春芳, 杨联芝, 王军, 等. 苦荞麦麸油β-环糊精包合工艺及其参数优化[J]. 食品科学, 2010, 31(6): 16-19.
[19] 续浩, 陈亮, 马丽花. 水溶液中环糊精包结物的包结常数的测定方法[J]. 分析测试技术与仪器, 2002, 8(2): 72-79.
Optimization of Preparation Process for Sinomenine-Cylcodextrin Inclusion Complex and Its Inclusion Constant
ZHU Shi-long1,LI Yong1,LIN Hong-wei2,3,DUAN You-gou1,*
(1. College of Chemistry and Chemical Engineering, Jishou University, Jishou 416000, China;
2. Department of Chemistry and Chemical Engineering, Huaihua University, Huaihua 418008, China;
3. The Critical Laboratory of Hunan Province on Research and Utilization of Ethnomedicinal Plant Resources, Huaihua 418008, China)
Objectives: To investigate optimal conditions for inclusion complex formation between sinomenine and cylcodextrins and determine the inclusion constants and release in vitro of inclusion complexes prepared with different cyclodextrins. Methods:One-factor-at-a-time and orthogonal array design methods were employed for the optimization of inclusion complex formation conditions. The inclusion constants of sinomenine complexes with β -cylcodextrin (β -CD), hydroxypropyl-β -cyclodextrin(HP-β -CD) and γ -cyclodextrin (γ -CD) formed under optimal conditions were determined by the phase solubility method.Moreover, their release in vitro was tested. Results: The optimal conditions for forming sinomenine-cylcodextrins inclusion complexes were 1:1 of sinomenine-to-cylcodextrin molar ratio, 50 ℃ of temperature, and 3 h of reaction duration at pH 7. The inclusion constants of sinomenine-β-CD, sinomenine-HP-β-CD and sinomenine-γ-CD formed under these conditions were calculated as 501.1, 150.0, 600.3 L/mol, respectively. Conclusion: sinomenine and cylcodextrins can form stable inclusion complexes at a molar ratio of 1:1. Various inclusion complexes show remarkable sustained release effect on sinomenine.
sinomenine;cylcodextrins;inclusion constant;orthogonal array design;process optimization
TQ464.4
A
1002-6630(2012)08-0054-06
2011-03-24
国家自然科学基金面上项目(30870230);湖南省自然科学基金项目(06JJ50020);湖南省教育厅项目(09C760);民族药用植物资源研究与利用湖南省重点实验室开放基金项目(HHUW2010-68);吉首大学研究生校级科研项目(11JDY052)
朱士龙(1986—),男,硕士研究生,研究方向为药物化学分离分析及应用。E-mail:elicss@163.com
*通信作者:段友构(1954—),男,教授,研究方向为天然产物分离分析。E-mail:dyg110125@163.com
