气相色谱-质谱联用分析杜鹃红山茶挥发性成分
2012-10-28李辛雷孙振元李纪元范正琪殷恒福
李辛雷,孙振元*,李纪元,范正琪,殷恒福
(1.中国林业科学研究院亚热带林业研究所,浙江 富阳 311400;
2.中国林业科学研究院林业研究所,林木遗传育种国家重点实验室,北京 100091)
气相色谱-质谱联用分析杜鹃红山茶挥发性成分
李辛雷1,2,孙振元2,*,李纪元1,范正琪1,殷恒福1
(1.中国林业科学研究院亚热带林业研究所,浙江 富阳 311400;
2.中国林业科学研究院林业研究所,林木遗传育种国家重点实验室,北京 100091)
采用固相微萃取和气相色谱-质谱联用技术,分析杜鹃红山茶花朵不同花期、不同部位和一天中不同时间段的挥发性成分及其相对含量,并对其变化规律进行研究。结果表明:杜鹃红山茶花蕾期的挥发性成分有8种、始花期20种、盛花期21种、衰落期17种,其中始花期和盛花期为挥发性成分释放的主要时期;花朵开放过程中,醇类化合物的相对含量逐渐升高,烯类、酯类和烷烃类先升高后降低,醛酮类总体呈下降趋势。杜鹃红山茶盛花期花朵的4个部位中,萼片的挥发性成分有20种,花瓣22种、雄蕊21种、雌蕊13种,其中花瓣和雄蕊为挥发性成分释放的主要部位;花瓣、雄蕊、萼片中烷烃类相对含量均最高,分别占挥发性成分总量的49.86%、51.59%和44.66%;雌蕊中醛酮类含量最高,为83.87%。挥发性成分的相对含量在一天中变化明显,8:00时到12:00时是烯类、醇类、酯类和烷烃类化合物释放的高峰期,而醛酮类在14:00时到18:00时的释放量较高。
杜鹃红山茶;挥发性成分;气相色谱-质谱联用法
山茶(Camellia)原产于我国,是我国十大传统名花之一[1]。山茶花除具有观赏价值,还具有食用和药用功能,我国山茶花栽培应用历史悠久,其观赏性、食用性和药用性已为相关资料所证实[2-4]。已有研究表明山茶花中主要有益成分包括糖类、蛋白质、维生素、微量元素、氨基酸、黄酮类等[3,5],具有抗菌、抗氧化、降血压和调节血脂含量等作用[4]。目前,在山茶花食用价值的利用方面,已开发出金花茶(C. nitidissima)茶用饮料及食品[3]。
观赏植物玫瑰(Rosa rugosa)、白兰花(Michelia alba)及茉莉花(Jasminum sambac)等茶用植物香气成分的研究表明,香气的产生主要由于醇类、烯类、酯类和烷烃类等挥发性成分的存在[6-12]。在山茶花香气成分研究方面,范正琪等[13-14]对3种山茶花挥发性成分进行了测定。杜鹃红山茶(C.azalea Wei)又名张氏红山茶,不同于现有茶花品种仅在冬春季节开花的特性,杜鹃红山茶花期长,为4~12月,且在适宜的栽培条件下,一年四季都可以开花[4],是提取山茶花挥发性成分的良好材料,可用于开发山茶花香精香料及茶用饮料等食品产业,但目前关于其挥发性成分的研究尚未见相关报道。因此,本实验利用气相色谱-质谱联用(gas chromatography-mass spectrometer,GC-MS)技术对杜鹃红山茶不同花期、花朵不同部位和一天中不同时间段的挥发性成分及其相对含量进行分析,研究杜鹃红山茶挥发性成分的变化规律,以期为山茶花食用价值的开发利用提供一定的科学依据。
1 材料与方法
1.1 材料
杜鹃红山茶花朵,采集于中国林业科学研究院亚热带林业研究所苗圃,采样时间为2011年7月。杜鹃红山茶的花期划分为4个阶段,即花蕾期、始花期、盛花期和衰落期,花蕾期指大部分花蕾完全伸出苞叶,花蕾颜色已变红;始花期指花瓣微展,雄蕊被包裹在花瓣中;盛花期指花瓣完全张开,花药已发育成熟;衰老期指花瓣出现褶皱,质地开始变薄。杜鹃红山茶盛花期的花朵分为4个部位,即萼片、花瓣、雄蕊和雌蕊。以一天中8:00(T1)、10:00(T2)、12:00(T3)、14:00(T4)、16:00(T5)、18:00(T6)的挥发性成分含量的变化来表示杜鹃红山茶花朵挥发性成分的日变化。同种环境条件下每个处理选取5株,每株重复采样3次,采后30min内进行挥发性物质的测定。
1.2 仪器与设备
6890N/5975B气相色谱-质谱联用仪、HP-5MS石英毛细管柱(30m×0.25mm,0.25μm) 美国Agilent公司;PDMS/DVB萃取头(65μm) 美国Supelco公司。
1.3 方法
1.3.1 杜鹃红山茶挥发性成分提取
将采集的样品置于顶空样品瓶中,加入0.5μL 40ng/μL癸酸乙酯溶液作为内标物,采用固相微萃取法,40℃条件下,65μm PDMS/DVB萃取头萃取30min进样。
1.3.2 GC-MS条件
电离方式为电子电离(electron ionization,EI),电子能量70eV,进样口温度250℃,柱温35℃保持2min,以5℃/min升至80℃,再以8℃/min升至180℃,再以8℃/min升至250℃;四极杆温度150℃、离子源温度230℃、接口温度为280℃;扫描质量数范围为30~500u。
1.3.3 挥发性成分定性和定量分析
挥发性成分根据质谱数据和气质联用仪标准图谱数据库的检索结果定性;各组分的相对含量根据各化合物峰面积与内标峰面积之比定量。
2 结果与分析
2.1 杜鹃红山茶不同花期挥发性成分
从表1可以看出,花蕾期的挥发性成分为8种、始花期20种、盛花期21种、衰落期17种。挥发性成分中辛烷、壬醛、石竹烯、萘和罗汉柏烯等5种化合物的相对含量高于其他成分,且随花朵的开放呈现先升高再降低的趋势,其主要含量集中于始花期和盛花期;5种化合物含量合计占始花期中总挥发性成分的65.92%、盛花期的61.02%,为主要挥发性化合物。罗汉柏烯、柯巴烯、萘、3-苯基-2-丙烯醛和1,2,3,4,5-五甲基-1,3-环戊二烯仅在始花期和盛花期存在;α-雪松烯仅在始花期存在。杜鹃红山茶花蕾期甲醚、2-丙烯醛的相对含量较高,随花朵开放其相对含量逐渐下降。除辛烷、壬醛外,杜鹃红山茶衰落期2-{4-[2-(4-甲氧基甲苯基)乙烯基]苯基}丙-2-醇的相对含量较高,且其含量随花朵的开放呈逐渐升高的趋势。
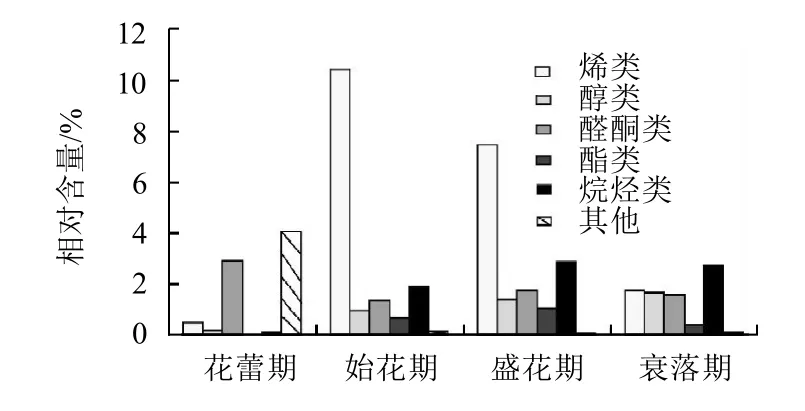
图1 杜鹃红山茶不同花期的主要挥发性成分分类Fig.1 Relative contents of major groups of volatile components at different flowering stages of C. azalea
杜鹃红山茶不同花期的挥发性成分划分为6类化合物,即烯类、醇类、醛酮类、酯类、烷烃类和其他(主要包括甲醚、酸类化合物和胺类化合物)。由图1可知,6类化合物中烯类相对含量最高,其次为烷烃类和醛酮类,3者分别占总挥发性成分的44.17%、16.42%和16.38%;醇类和酯类分别占9.08%和4.50%。花朵开放过程中,烯类、酯类和烷烃类化合物相对含量均呈现先升高后降低的趋势,其始花期和盛花期含量合计分别占不同花期总含量的89.16%、81.09%和62.62%。醇类随花朵开放其相对含量逐渐升高,始花期和盛花期的含量合计占56.89%;醛酮类相对含量总体呈逐渐下降的趋势,始花期和盛花期的含量合计占40.96%。

表1 杜鹃红山茶不同花期的主要挥发性成分及其相对含量Table 1 Major volatile components and relative contents at different flowering stages of C. azalea

表2 杜鹃红山茶花朵不同部位主要挥发性成分及其相对含量Table 2 Major volatile components and relative contents in different parts of C. azalea flowers

续表2
2.2 杜鹃红山茶花朵不同部位的挥发性成分
由表2可以看出,盛花期杜鹃红山茶萼片的挥发性成分20种、花瓣22种、雄蕊21种、雌蕊13种,与花瓣和雄蕊相比,萼片和雌蕊挥发性成分的组成较为简单,相对含量也较低,说明花瓣和雄蕊是杜鹃红山茶挥发性成分释放的主要部位。杜鹃红山茶花朵4个部位含有7种相同的化合物,且各成分在花瓣、雄蕊中的相对含量远高于萼片和雌蕊,如正己烷在花瓣、雄蕊中分别为9.3435%和6.6015%,而萼片、雌蕊中为2.1732%和0%。花瓣中正己烷的相对含量最高,其次是邻苯二甲酸酯、2-乙基-1-己醇和2-甲基丁烷,这几种化合物相对含量之和占花瓣挥发性成分总含量的65.30%,为杜鹃红山茶花瓣的主要挥发性成分。雄蕊中正己烷、2,2, 4-三甲基-戊烷、壬醛和2-(4-乙氧基碳基)苯亚甲基-苯并呋喃-6-醇-3-酮占雄蕊挥发性成分总含量的58.42%,为雄蕊的主要挥发性成分。
如图2所示,6类化合物中烷烃类相对含量最高,其次为醛酮类、醇类和烯类,分别占总挥发性成分的48.21%、17.93%、13.12%和12.22%。花瓣中烷烃类相对含量最高,占花瓣中挥发性成分总量的49.86%,其次为醇类、烯类和酯类;雄蕊、萼片中烷烃类相对含量亦最高,分别占挥发性成分总量的51.59%和44.66%,其次为醛酮类、烯类和醇类;雌蕊中醛酮类相对含量最高,占挥发性成分总量的83.87%,其余化合物含量均较低。

图2 杜鹃红山茶花朵不同部位的主要挥发性成分分类Fig.2 Relative contents of major groups of volatile components in different parts of C. azalea flowers
2.3 杜鹃红山茶挥发性成分的日变化
如表3所示,庚醛、α-蒎烯、(E)-3-甲基-1,3-戊二烯、2-乙基-1-己醇、3,6-二甲氧基-9-(2-苯基乙基)-芴-9-醇、4-乙基苯氧酸-2-丁酯、邻苯二甲酸二乙酯和己烷等化合物的相对含量高于其他成分,为主要挥发性成分。挥发性成分的相对含量在一天中变化较大,其中庚醛相对含量在一天中呈现先降低后升高的趋势,高峰期集中在16:00时到18:00时;α-蒎烯和(E)-3-甲基-1,3-戊二烯呈现先升高后降低的趋势,其峰期分别出现在10:00和12:00时;4-乙基苯氧酸-2-丁酯、邻苯二甲酸二乙酯和己烷峰期均出现在8:00时;2-乙基-1-己醇呈现先升高后降低的趋势,高峰期集中在10:00时到12:00时;3,6-二甲氧基-9-(2-苯基乙基)-芴-9-醇呈现降低升高再降低的趋势,高峰期集中在8:00时到10:00时。
由图3可知,杜鹃红山茶主要挥发性成分数量及其相对含量的日变化为:挥发性成分数量方面,烯类化合物的组分数量最多,且从8:00时到12:00时逐渐升高,然后降低,14:00时后稳定不变;醇类在一天中比较稳定,无明显变化;醛酮类组分数量8:00时到12:00时逐渐降低,14:00时到18:00时呈现先升高再降低的趋势;酯类和烷烃类化合物的组分较少,在某些时段未能检测到。在主要挥发性成分相对含量方面,醛酮类最高,其次为烯类、醇类和酯类,烷烃类较低;醛酮类化合物在一天中呈现先降低再升高的趋势,14:00时到18:00时为其相对含量的高峰期,占挥发性成分的大部分;烯类、醇类化合物在一天中呈现升高降低再升高降低的双峰曲线,8:00时到12:00时占挥发性成分的大部分,10:00时和16:00时出现2个峰值;酯类和烷烃类化合物呈现降低升高再降低的趋势,8:00时到12:00时占挥发性成分的绝大部分。可见,一天中8:00时到12:00时,是烯、醇、酯类和烷烃类化合物释放的高峰期,14:00时到18:00时是醛酮类化合物释放的高峰期。

表3 杜鹃红山茶主要挥发性成分及其相对含量的日变化Table 3 Diurnal variations of major volatile components and relative contents in C. azalea flowers

图3 杜鹃红山茶主要挥发成分及其相对含量的日变化Fig.3 Diurnal variation of major groups of volatile components and relative contents in C. azalea flowers
3 讨 论
范正琪等[13-14]对山茶物种攸县油茶(C. grijsii)及品种‘克瑞墨大牡丹’和‘香神’的研究表明,香气成分以醇、醛、酯、烯、烷及芳樟醇氧化物为主,其中攸县油茶以顺-芳樟醇氧化物Ⅱ和苯乙醇占优势,‘克瑞墨大牡丹’芳樟醇相对含量较高,‘香神’以壬醛和芳樟醇含量最高。本实验中杜鹃红山茶主要挥发性成分不完全相同,且主要成分相对含量差异较大,这可能与物种或者物种特异成分的组成不同有关。已有研究认为腊梅(Chimonanthus praecox)释香过程中烷烃、醇类和酯类物质的含量与腊梅的开放度呈正相关[15];茉莉花采后的未成熟期、成熟期和枯萎期醇类物质含量与茉莉花采后的存放时间呈正相关,酯类物质在成熟期的含量最高[16]。杜鹃红山茶挥发性成分随着花朵的开放而逐渐形成并释放,从花蕾期到盛花期,醇类、酯类和烷烃类化合物的相对含量总体呈上升趋势,这与腊梅和茉莉的研究报道基本相符[15-16],但醛酮类化合物在花朵开放过程中总体上有逐渐下降的趋势,具体原因有待于进一步研究。
对杜鹃红山茶花朵不同部位挥发性成分的分析发现,花瓣和雄蕊是挥发性成分释放的主要部位,但不同部位挥发性成分的组分存在一定差异,即使相同成分在不同部位中的含量亦差异明显,说明植物不同部位挥发性成分及其相对含量不尽相同[17]。杜鹃红山茶挥发性成分的相对含量在一天中变化明显,醇类物质中大部分成分如2-乙基-1-己醇、4-戊烯-2-醇、(E)-2-己烯-1-醇和3-甲基-2-己醇等在10:00时的释放量最大,在18:00时释放量较小,这与李海东等[18]对珍珠梅(Sorbaria kirilowii)挥发性物质中醇类日动态变化的研究基本一致,但本实验醛酮类和酯类物质的释放强度则与其研究结果不尽相同,说明同种物质在一天中的释放强度不仅受环境因子的影响,还与实验材料的特性相关。
杜鹃红茶花期长,原料丰富,花中的挥发油能用于化妆品、香精香料及茶用饮料等,是开发山茶花挥发性物质的良好材料。本实验利用固相微萃取结合GCMS技术对杜鹃红山茶的挥发性成分进行了研究,明确了杜鹃红山茶挥发性成分的变化规律,为进一步开发利用提供了科学依据。但植物挥发性成分形成及释放的机理比较复杂,杜鹃红山茶主要挥发性化合物的具体来源途径,相关酶活性的变化及其与挥发性成分释放的关系等还有待于进一步研究。
4 结 论
杜鹃红山茶不同花期中,始花期和盛花期为挥发性成分释放的主要时期,辛烷、壬醛、石竹烯、萘和罗汉柏烯等化合物是杜鹃红山茶的主要挥发性成分。在花朵不同部位中,花瓣和雄蕊是挥发性成分释放的主要部位,己烷、2-甲基丁烷、2-乙基-1-己醇和邻苯二甲酸酯为花瓣的主要挥发挥发性成分,己烷、2,2,4-三甲基-戊烷、2-甲基丁烷、罗汉柏烯、2-(4-乙氧基碳基)苯亚甲基-苯并呋喃-6-醇-3-酮和壬醛为雄蕊的主要挥发性成分。挥发性成分的相对含量在一天中变化明显,8:00时到12:00时是烯类、醇类、酯类和烷烃类化合物释放的高峰期,而醛酮类化合物在14:00时到18:00时的释放量较高。
[1] 张宏达, 任善湘. 中国植物志: 第49卷3分册[M]. 北京: 科学出版社, 1998: 1.
[2] 高继银, PARKS C R, 杜跃强. 山茶属植物主要原种彩色图集[M].杭州: 浙江科学技术出版社, 2005.
[3] 梁盛业, 陆敏珠. 中国金花茶栽培与开发利用[M]. 北京: 中国林业出版社, 2005: 35.
[4] 江苏新医学院. 中药大辞典[M]. 上海: 上海科学技术出版社, 2000: 191.
[5] 李辛雷, 李纪元, 范正琪, 等. 四种山茶花营养成分及有害元素含量分析[J]. 林业科学研究, 2010, 23(2): 298-301.
[6] SHANG Chunqing, HU Yaoming, DENG Chunhui, et al. Rapid determination of volatile constituents of Michelia alba flowers by gas chromatography-mass spectrometry with solid-phase micro-extraction [J]. Journal of Chromatography, 2002, 942(1): 283-288.
[7] GUTERMAN I, SHALIT M, MENDA N, et al. Rose scent: genomics approach to discovering novel floral fragrance-related genes[J]. Plant Cel1, 2002, 14(10): 2325-2338.
[8] 高丽萍, 王黎明, 张玉琼, 等. 茉莉花香气释放酶的研究[J]. 茶叶科学, 2001, 21(2): 140-143.
[9] GUTH H, GROSCH W. Identification of potent odourants in static headspace samples of green and black tea powders on the basis of aroma extract dilution analysis[J]. Flavor&Fragrance, 1993, 8(1): 173-178.
[10] 刘晓慧, 张丽霞, 王日为. 顶空固相微萃取-气相色谱-质谱联用法分析黄茶香气成分[J]. 食品科学, 2010, 31(16): 239-243.
[11] BARKMAN T J, BEAMAN J H, GAGE D A. Floral fragrance variation in Cypripedium: Implications for evolutionary and ecological studies[J]. Phytochemistry, l999, 44(5): 875-882.
[12] 王力, 林智, 吕海鹏. 茶叶香气影响因子的研究进展[J]. 食品科学, 2010, 31(15): 293-298.
[13] 范正琪, 李纪元, 田敏, 等. 山茶品种‘克瑞墨大牡丹’ 香气成分分析[J]. 林业科学研究, 2005,18(4): 412-415.
[14] 范正琪, 李纪元, 田敏, 等. 三个山茶花种(品种)香气成分初探[J]. 园艺学报, 2006, 33(3): 592-596.
[15] 谢超, 王建晖, 龚正礼. 腊梅释香过程中香气成分的分析研究[J]. 茶叶科学, 2008, 28(4): 282-288.
[16] 郭友嘉, 戴亮, 任清, 等. 用吸附-热脱捕集进样法研究茉莉花香释放过程中的化学成分[J]. 色谱, 1994, 12(2): 110-113.
[17] 苑兆和, 尹燕雷, 李自峰. 石榴果实香气物质的研究[J]. 林业科学, 2008, 44(1): 65-69.
[18] 李海东, 高岩, 金幼菊. 珍珠梅花挥发性物质日动态变化的研究[J].内蒙古农业大学学报, 2004, 25(2): 54-59.
GC-MS Analysis of Volatile Components in Camellia azalea Flowers
LI Xin-lei1,2,SUN Zhen-yuan2,*,LI Ji-yuan1,FAN Zheng-qi1,YIN Heng-fu1
(1. Research Institute of Subtropical Forestry, Chinese Academy of Forestry, Fuyang 311400, China;2. State Key
Laboratory of Tree Genetics and Breeding, Research Institute of Forestry, Chinese Academy of Forestry, Beijing 100091, China)
Volatile compounds in Camellia azalea flowers at different stages during flower development, in their different parts and at different hours of a day were analyzed by solid phase micro-extraction and gas chromatography-mass spectrometry (GCMS). Totally 8, 20, 21 and 17 volatile compounds were identified in early-stage, full bloom and withering flowers, respectively. Volatile compounds were released mainly during the early flowering and full bloom stages. During flower development, the content of alcohols revealed a gradual increase. Alkenes, esters and alkanes revealed an initial increase and a final decrease, while aldehydes and ketones revealed a decrease trend during the whole process. Totally 20 compounds were identified in sepals, 22 in petals, 21 in stamens and 13 in pistils. The major parts releasing volatile components were petals and stamens. Alkanes were the most dominant volatile compounds in sepals, stamens and petals, accounting for 49.86%, 51.59% and 44.66% of the total volatiles, respectively, while the most dominant volatile compounds in pistils were aldehydes and ketones with a relative content of 83.87%. An obvious intraday variation was observed in the relative contents of volatile compounds in Camellia azalea flowers. The peak hours for releasing alkenes, alcohols, esters and alkanes were 8:00 to 12:00, while higher release levels of aldehydes and ketones were found from 14:00 to 18:00.
Camellia azalea;volatile component;gas chromatography-mass spectrometry (GC-MS)
TS207.3
A
1002-6630(2012)16-0130-07
2011-12-21
国家自然科学基金青年科学基金项目(30800886);浙江省科技计划项目(2010C32038)
李辛雷(1978—),男,助理研究员,博士,研究方向为观赏植物遗传育种与应用。E-mail:lixinlei2020@163.com
*通信作者:孙振元(1964—),男,研究员,博士,研究方向为园林植物分子育种。E-mail:sunzy@263.net
