吉西他滨致轻度胰腺癌相关恶病质模型的建立
2012-09-27吴建华江舒曼
吴建华,贾 林,江舒曼
(广州医学院附属广州市第一人民医院消化内科 510180)
晚期胰腺癌,尤其是化学治疗患者多伴有食欲缺乏和体质量减轻等症状,甚至出现肿瘤相关恶病质(cancer-related cachexia),为严重影响患者预后和生存质量的重要因素[1]。Evans等[2]根据癌症患者体质量下降程度将恶病质分为轻度(>5%)、中度(>10%)和重度(>15%),但迄今未见胰腺癌相关恶病质模型的研究报道。在大剂量吉西他滨(gemcitabine,100mg/kg)化疗致重度胰腺癌恶病质模型和实验治疗的前期研究基础上[3],本文通过分析不同剂量吉西他滨化疗对胰腺癌模型体质量、营养状况和进食量的影响及其时-效关系,旨在建立轻度胰腺癌相关恶病质模型的制备方法,为恶病质的早期干预奠定实验基础。
1 材料与方法
1.1 实验材料 24只4~6周龄SPF级BALB/C裸小鼠,18~21g,由中山大学实验动物中心提供和饲养。吉西他滨购自美国礼来公司,高转移人胰腺癌细胞株SW1990由中山大学附属第二医院张世能教授惠赠。
1.2 实验方法
1.2.1 模型制备及分组 SW1990细胞悬液0.2mL接种于裸鼠右侧近前腋的背部皮下做供体瘤,裸鼠在接种胰腺癌细胞后,经过约1周潜伏期,可见接种部位皮下出现淡红色结节,并逐渐长大,呈圆形或椭圆形。每隔3d用游标卡尺测量肿瘤大小,待长至近1cm3的实体瘤后,取出并剪成1mm3的均匀组织块,转种于24只裸鼠右侧颈背部皮下,建立胰腺癌皮下移植瘤模型[4],并随机分为对照组(G0组)、吉西他滨3次组(G3组,吉西他滨50mg/kg,腹腔内给药,术后第1、4、7天)、吉西他滨4次组(G4组,吉西他滨50mg/kg,腹腔内给药,术后第1、4、7、10天),每组8只,术后第25天处死裸鼠。
1.2.2 观察指标 (1)记录实验前及建模后每周1次的日均进食量;(2)测量实验前及建模后每隔3d的体质量,实验结束时处死动物,称去瘤后小鼠体质量;(3)每隔3d用游标卡尺测量肿瘤的最大长径A和最小短径B,按公式V=0.5×A×B2计算肿瘤体积,实验结束时取出移植瘤,称瘤质量;(4)每隔3d用游标卡尺测量动物的腹部皮褶厚度,皮下脂肪=皮褶厚度×0.5;(5)每隔3d用游标卡尺测量前臂直径d,按公式C=d×3.14计算前臂周径。
1.3 统计学处理 采用SPSS 17.0统计软件进行单因素方差分析及组间两两比较的SNK检验,计量资料数据均采用±s表示。以P<0.05为差异有统计学意义。
2 结 果
2.1 不同剂量吉西他滨对胰腺癌移植瘤体积和瘤质量的影响及时-效关系 随实验时间延长,对照组肿瘤体积迅速增大,化疗组的移植瘤体积增长缓慢。在实验的第5天,化疗组肿瘤体积显著小于对照组(P<0.05),这种抑制作用一直持续至实验结束。从第13天开始,G4组肿瘤体积小于G3组肿瘤体积,但差异无统计学意义(P>0.05)。见表1。
实验结束时处死动物,G0组的瘤质量[(1.31±0.12)g]显著高于G3组的(0.38±0.12)g和 G4组(0.33±0.09)g(P<0.05);G3组和G4组的瘤质量则差异无统计学意义(P>0.05)。G3组与G4组的抑瘤率分别为47.3%、51.0%,二者比较差异无统计学意义(P>0.05)。
2.2 不同剂量吉西他滨对胰腺癌模型鼠重的影响及时-效关系 从实验第5天开始,化疗组体质量明显低于对照组(P<0.05),第9天时,G3组与G4组平均体质量分别下降7.9%、8.1%;第13天时,G3组平均体质量下降9.7%,较G4次组14.1%下降少。整个实验过程中,G3组体质量略高于G4组,但差异无统计学意义(P>0.05)。见表1。
表1 不同剂量吉西他滨对胰腺癌模型体重及营养指标的影响及时-效关系(±s,n=8)
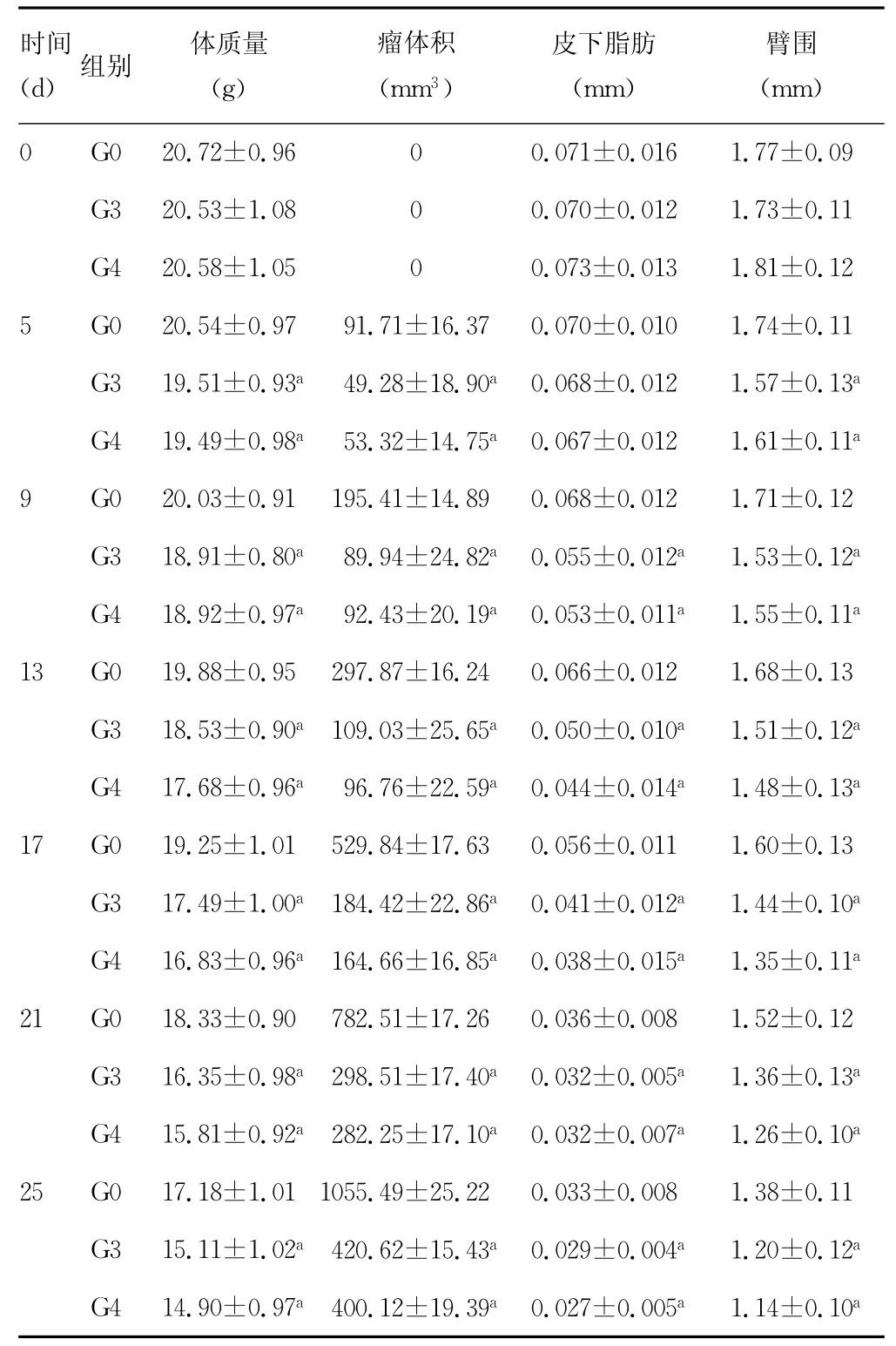
表1 不同剂量吉西他滨对胰腺癌模型体重及营养指标的影响及时-效关系(±s,n=8)
a:P<0.05,与G0组比较。
(d) 组别 体质量(g)时间 瘤体积(mm3)皮下脂肪(mm)臂围(mm)0 G0 20.72±0.96 0 0.071±0.016 1.77±0.09 G3 20.53±1.08 0 0.070±0.012 1.73±0.11 G4 20.58±1.05 0 0.073±0.013 1.81±0.12 5 G0 20.54±0.97 91.71±16.37 0.070±0.010 1.74±0.11 G3 19.51±0.93a49.28±18.90a0.068±0.012 1.57±0.13a G4 19.49±0.98a53.32±14.75a0.067±0.012 1.61±0.11a 9 G0 20.03±0.91 195.41±14.89 0.068±0.012 1.71±0.12 G3 18.91±0.80a89.94±24.82a0.055±0.012a1.53±0.12a G4 18.92±0.97a92.43±20.19a0.053±0.011a1.55±0.11a 13G0 19.88±0.95 297.87±16.24 0.066±0.012 1.68±0.13 G3 18.53±0.90a109.03±25.65a0.050±0.010a1.51±0.12a G4 17.68±0.96a96.76±22.59a0.044±0.014a1.48±0.13a 17G0 19.25±1.01 529.84±17.63 0.056±0.011 1.60±0.13 G3 17.49±1.00a184.42±22.86a0.041±0.012a1.44±0.10a G4 16.83±0.96a164.66±16.85a0.038±0.015a1.35±0.11a 21G0 18.33±0.90 782.51±17.26 0.036±0.008 1.52±0.12 G3 16.35±0.98a298.51±17.40a0.032±0.005a1.36±0.13a G4 15.81±0.92a282.25±17.10a0.032±0.007a1.26±0.10a 25G0 17.18±1.01 1055.49±25.22 0.033±0.008 1.38±0.11 G3 15.11±1.02a420.62±15.43a0.029±0.004a1.20±0.12a G4 14.90±0.97a400.12±19.39a0.027±0.005a1.14±0.10a
2.3 不同剂量吉西他滨对胰腺癌模型臂围和皮下脂肪的影响及时-效关系 在实验第5天,化疗组与对照组臂围之间出现明显差异(P<0.05),这种差异随着时间延长越来越明显。从实验第13天到实验结束,G4组平均臂围小于G3组,但差异无统计学意义(P>0.05)。见表1。实验开始时各组动物皮下脂肪之间差异无统计学意义,随着时间的延长,各组动物的皮下脂肪都有减少。在第9天到第17天,化疗组的平均皮下脂肪显著少于对照组(P<0.05),G3组平均皮下脂肪较G4组多,但二者差异无统计学意义(P>0.05)。见表1。
2.4 不同剂量吉西他滨对胰腺癌模型日均进食量的影响及时-效关系 吉西他滨化疗1周后,裸鼠进食量出现明显下降,化疗组的进食量与对照组比较显著降低(P<0.05)。在第14天时,G4组进食量显著低于G3组(P<0.05),见表2。但在实验后期两组之间进食量差异无统计学意义(P>0.05)。
表2 不同剂量吉西他滨对胰腺癌模型进食量的影响及时-效关系(±s,g,n=8)
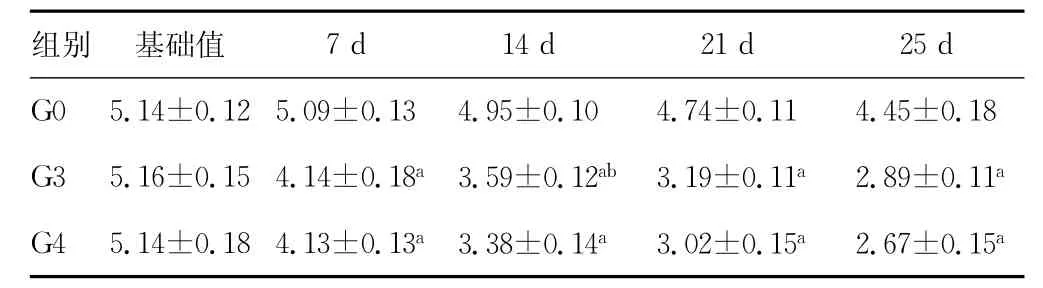
表2 不同剂量吉西他滨对胰腺癌模型进食量的影响及时-效关系(±s,g,n=8)
a:P <0.05,与G0组比较;b:P <0.05,与G4组比较。
7d 14d 21d 25d G0 5.14±0.12 5.09±0.13 4.95±0.10 4.74±0.11 4组别 基础值.45±0.18 G3 5.16±0.15 4.14±0.18a3.59±0.12ab 3.19±0.11a2.89±0.11a G4 5.14±0.18 4.13±0.13a3.38±0.14a3.02±0.15a2.67±0.15a
3 讨 论
恶病质在临床上的表现多为食欲缺乏、体质量减轻、脂肪和骨骼肌分解增加,其中食欲缺乏、体质量减轻是最明显症状[5-6]。肿瘤患者的恶病质发生率和病死率分别为80%和20%[7],与较低的生存质量和较差的预后相关,并导致肿瘤治疗抵抗[8-10]。改善恶病质状态可以提高晚期肿瘤患者的生活质量,增强肿瘤患者对化疗的耐受能力,在肿瘤治疗的整个过程中是不可忽视的,早期干预和改善恶病质状态也因此成为国内外学者的重要课题[11-13]。
周伟等[14]通过观察实验过程中荷瘤鼠体质量和血清生化指标的改变,成功建立结肠癌相关性恶病质动物模型;国外学者Da等[15]和Xu等[16]在建立癌症恶病质动物模型后对恶病质进行了治疗学研究。在建立恶病质模型时,这些学者的共同点是在实验中测量动物的体质量与相关营养学指标来判定是否出现恶病质,但都未对恶病质的轻重进行分级,更未见吉西他滨致胰腺癌轻度恶病质模型建立方法的报道。
吉西他滨是目前治疗胰腺癌的一线药物,但有些患者在接受治疗过程中也产生了不同毒副作用,如疲倦乏力、恶心呕吐、食欲下降、体质量降低、营养不良和血液系统毒性反应等,这些不良反应缩短了患者进入恶病质状态时间。本研究借鉴国内外学者建立恶病质模型的方法,在予小剂量吉西他滨(50mg/kg)治疗胰腺癌动物模型时,测量动物的体质量及相关营养学指标,成功建立吉西他滨致胰腺癌恶病质动物模型,并且根据吉西他滨对动物进食量和相关营养学指标的时-效关系将恶病质程度进行了分级,在每隔2d用药,用药3次后,胰腺癌模型的体质量下降小于10%,符合Evans等[2]的轻度恶病质标准,而对照组动物体质量在实验第21天时,体质量下降约10%,证明胰腺癌动物模型在早期未进入恶病质状态。本实验成功地建立了胰腺癌轻度恶病质模型,为后续治疗肿瘤相关恶病质奠定了实验基础。
[1] Freelove R,Walling D.Pancreatic cancer:diagnosis and management[J].Am Fam Physician,2006,73(3):485-492.
[2] Evans WJ,Morley JE,Argiles J,et al.Cachexia:A new definition[J].Clin Nutr,2008,27(6):793-799.
[3] 贾林,尚鸳鸳.抗抑郁药米氮平对吉西他滨治疗胰腺癌模型的辅助作用[J].中华胰腺病杂志,2009,9(6):380-382.
[4] 贾林,刘艳虹.吉西他滨联合光动力疗法治疗人胰腺癌裸鼠移植瘤的研究[J].中华消化杂志,2009,28(5):314-317.
[5] Paccagnella A,Morassutti I,Rosti G.Nutritional intervention for improving treatment tolerance in cancer patients[J].Curr Opin Oncol,2011,23(4):322-330.
[6] Blum D,Omlin A,Fearon K,et al.Evolving classification systems for cancer cachexia:ready for clinical practice?[J].Support Care Cancer,2010,18(3):273-279.
[7] Muscaritoli M,Anker SD,Argilés J,et al.Consensus definition of sarcopenia,cachexia and pre-cachexia:joint document elaborated by Special Interest Groups(SIG)“cachexia-anorexia in chronic wasting diseases”and “nutrition in geriatrics”[J].Clin Nutr,2010,29(2):154-159.
[8] Davidson W,Ash S,Capra S,et al.Weight stabilization is associated with improved survival duration and quality of life in unresectable pancreatic cancer[J].Clin Nutr,2004,23(2):239-247.
[9] Ferrucci LM,Bell D,Thornton J,et al.Nutritional status of patients with locally advanced pancreatic cancer:apilot study[J].Support Care Cancer,2011,19(11):1729-1734.
[10]Bennani-Baiti N,Walsh D.Animal models of the cancer anorexia-cachexia syndrome[J].Support Care Cancer,2011,19(9):1451-1463.
[11]周毅,何捷,刘旭荣.康莱特注射液配合胃肠外营养治疗癌症恶病质[J].中国肿瘤,2006,15(9):635-636.
[12]Higashiguchi T.Cancer patient therapy and nutritional support[J].Gan To Kagaku Ryoho,2011,38(8):1235-1240.
[13]Uomo G,Gallucci F,Rabitti PG.Anorexia-cachexia syndrome in pancreatic cancer:recent development in research and management[J].JOP,2006,7(2):157-162.
[14]周伟,江志伟,姜军,等.一种癌性恶病质动物模型的建立[J].中国实验外科杂志,2004,21(4):490-491.
[15]Das SK,Eder S,Schauer S,et al.Adipose triglyceride lipase contributes to cancer-associated cachexia[J].Science,2011,333(6039):233-238.
[16]Xu H,Carwford D,Hutchinson KR,et al.Myocardial dysfunction in an animal model of cancer cachexia[J].Life Sci,2011,88(9/10):406-410.
