用哲学理念来思考物理化学的基本概念和联系*
2012-09-25阳历莫婉玲梅付名
阳历 莫婉玲 梅付名
(华中科技大学化学与化工学院 湖北武汉 430074)
物理化学是一个概念和公式比较集中的学科。如果说它复杂,那只能从侧面说明还有很多逻辑和思维可以参与的空间,还有很多联系等待我们去建立。这种联系加进一点哲学思考,会有意想不到的清晰效果。
1 范畴问题——绝对与相对
1.1 基于自然规律本身的特性产生的绝对和相对
热力学是物理化学的重要内容之一。热力学有许多概念与公式,其中热力学能U和熵S是系统本身固有的特性,具有明确的物理意义,是基于自然规律的特性而提炼出来的绝对的概念,而焓H、Holmholtz自由能A及Gibbs自由能G则是在实际应用过程中由U、S、p、V、T等物理量推断产生的相对概念,这些绝对及相对的量又通过如下热力学方程关联:
H=U+pV
A=U-TS
G=H-TS
dU=TdS-pdV
dH=TdS+Vdp
dA=-SdT-pdV
dG=-SdT+Vdp
从更普遍的意义上说,标准摩尔生成焓、燃烧焓、规定熵等都基于一个规定的起点,一切过程和变化都以这个起点为参照对象,具有一定的绝对性。只有这个绝对的概念成立了,利用Hess定律,计算任意两个相对状态转化的焓变、熵变及Gibbs自由能变化才能成立。例如:
(1)
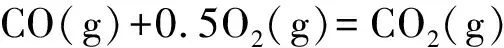
(2)
式(1)减去式(2),得式(3):
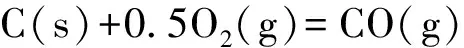
(3)
1.2 基于人为规定或总结的绝对和相对
上面讲到的都是自然过程中客观存在的绝对和相对。物理化学中还有很多人为产生的绝对和相对。通常对于一些概念的基本定义,都具有绝对性质,而基于这些概念的经验式有很多都只是相对的。
例如,电化学电解质溶液中离子的电荷、质量摩尔浓度及电导、电导率和摩尔电导率属于绝对概念,任何电解质溶液都具有这些性质。而离子强度、平均活度因子等则属于相对概念,这些绝对与相对概念之间的关系已由人们进行规定和总结。在表1中给出了其中的一些例子。

表1 物理化学中人为规定或总结的绝对和相对的典型例子
基于对绝对和相对概念的理解,可以进一步引出下面一对名词及其蕴含的原理。
2 性质问题——广度和强度
2.1 广度和强度的依赖统一
物理化学中表示系统性质时分别使用了广度性质与强度性质。前者如U、H、G等,表示与系统中物质的量相关;后者如T、p等,表示与物质的量无关;但二者又是紧密相关的。对于气体,一般是以状态方程的形式使二者依赖统一,如理想气体的状态方程,pV=nRT。对于封闭系统,可用热力学方程将广度性质与强度性质关联起来,如dU=TdS-pdV,当组成一定的系统,可用数学上更普遍的表达式如U=f(T,p)或U=f(T,V)表示二者的关联。
2.2 广度和强度的对立转化
广度性质和强度性质在某些条件下可以转化。如广度性质的物质的量就变为强度性质,广度性质的偏物质的量也是强度性质。可以看出,所谓强度性质,即是排除了物质数量干扰的量度标准,而广度性质是多起点的强度性质的总和。
2.3 广度和强度的严格区分
对于一个化学反应过程,广度性质往往起统筹的作用,强度性质往往起限制的作用。但如果是对于能量传递过程,广度性质就要和强度性质分离开来考虑。
(4)
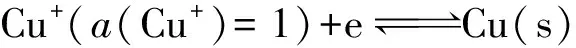
(5)

(6)
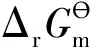
3 等效问题——真实与近似
3.1 等效的实现
这里将以电化学里一个重要的定义来解释等效的实现过程。
电解质的活度、平均离子活度及离子活度之间有如下的定义关系:
这里的离子平均活度a±定义的合理性可以这样理解,平均就是将溶液中所有离子视为无差别的质点,并将其性质平均化。这可以作为等效原理成立的基础。
等效原理的另一个作用对象不是溶液中的质点,而是化学反应,也就是以化学反应为单位进行等效。基于Arrhenius经验式,对于非基元反应,k=Aexp(-Ea/RT)中的表观活化能、表观指前因子、表观速率系数等都是等效的概念,这可以从以下关系中看出。对于某一基元反应,有k1=A1exp(-Ea1/RT);对于另一基元反应,有k2=A2exp(-Ea2/RT)。如果表观速率系数为k=Aexp(-Ea/RT),那么就可以根据表观速率系数k与基元反应速率系数k1、k2的关系,求出A与A1、A2以及E与E1、E2的关系。
3.2 近似是一种以多胜少的掩盖
以盐桥为例,它的作用是消除液接电势。液接电势是由于不同离子在界面的浓度和迁移速率不同,造成界面处溶液浓度改变而产生的不可逆电势。为什么这种不可逆电势会消除呢?因为盐桥里的离子承担了主要的运输任务,其他离子的作用被省略了,于是就得到了一种近似。
类似的还有Donnan平衡的消除过程。当加入的电解质浓度远大于大分子溶液的浓度时,渗透压可以用非电离大分子溶液的van′t Hoff渗透压公式进行计算。
3.3 为什么等效是正确的?
这种等效为什么是可行的呢?所有本质上的差别到哪里去了呢?从哲学观点可以这样理解:具体事物或者事物的某个具体过程相当于一个选择透过性膜,将物质属性中与研究对象没有关系的方面都过滤掉了,剩下的是等效结果。如真实气体与理想气体,当p→0时,分子间距离很远,分子间作用力很小,可以忽略;分子自由活动空间远远大于分子本身体积,以至于分子本身的体积可以忽略;此时的真实气体行为与理想气体等效。对于如何认识客观世界,哲学家康德说:“没有染指人的观念的所谓的客观世界与我们的认识没有关系,我们只能认识我们的世界。”
基于以上观点,我们可以重新看待“近似”。近似不再仅仅是对真实的一种逼近或者割舍,而在某种程度上就是真实本身。
所以可以说,等效过程在执行中是可行的,在性能上是无损的。
4 结语
基于以上3方面讨论,可以得出一个有趣的结论:世界在本质上是等效的。进一步抽象一下,所有的自发现象(无论是自然科学的还是社会科学的)都可以等效为“从不稳态到稳态的自发过程”;反过来,所有的非自发现象,也都可以等效为“从稳态到不稳态的非自发过程”。
最后我们要运用上面讨论的3个原理,继续解释新的未知。比如:Clausius-Clapeyron方程为什么和van′t Hoff等温方程非常相似?可以解释是化学势的概念把它们在本质上统一起来。但是化学势的本质又是什么呢?可以解释为“从不稳态到稳态的自发趋势的大小”。具体分析一下,这个定义里包含了绝对与相对、强度与广度以及近似与真实等要素。首先,“稳态”是绝对的静止的概念,“不稳态”是相对于稳态的概念;“趋势”代表着强度性质,而“大小”代表着强度的广度性质;而这个定义本身是对客观真实世界与主观理想的近似等效。
从这个意义上甚至可以说,哲学是一种最高形式的关于现实的抽象等效。
