103Pd-110Agm合金膜制备工艺研究
2012-07-18陈大明金小海李忠勇郭飞虎秦红斌
刘 卓,陈大明,金小海,李忠勇,郭飞虎,秦红斌
(原子高科股份有限公司,北京 102413)
放射性粒子近距离治疗肿瘤是利用放射性粒子植入肿瘤或肿瘤周围组织,让肿瘤接受局部放射治疗的技术。目前,临床使用的永久植入的粒子源主要是125I和103Pd。125I、103Pd具有合适的半衰期,能量低,不会产生有害气体,易于辐射防护[1]。由于核素的特性,103Pd对增殖周期较短的肿瘤组织比较有效,而125I对增殖周期较长的肿瘤组织比较有效。若将两种核素制备成复合源,就可在早期尚不能确定是哪种恶性肿瘤时或是在肿瘤生长的不同阶段,既可有效地控制增殖较快的恶性肿瘤组织,又可较长时间覆盖肿瘤的倍增周期,其功效将远远大于单一种子源。本研究通过文献调研及理论计算,设计将合金膜应用于复合种子源的制备,最终确定了复合种子源的制备方法,主要分两步:1)在载体银棒上制备103Pd-110Agm合金膜;2)对其进行碘化。
制备103Pd-110Agm合金膜的方法主要有:化学镀法、物理气相沉积法(PVD)、化学气相沉积法(CVD)、电镀法、真空溅射法等[2]。化学镀具有设备简单、对载体形状要求低、镀层均匀、可低温操作[3-8]等优点。因此,本研究采用化学镀法,在载体银棒上沉积103Pd-110Agm合金膜,研究载体预处理中的敏化和活化过程,优化化学镀的反应条件,分析镀层各组分含量并检测其微观机构。
1 主要仪器与试剂
1.1 主要仪器
旋转搅拌器:原子高科股份有限公司自制;恒温水浴锅:上海申生科技有限公司;BS110S分析天平:德国赛多利斯公司;可调量程移液器:德国艾本德公司;JSM6360LV扫描电镜:日本电子JEOL。
1.2 主要试剂
氯化钯:分析纯,北京化学试剂公司;硝酸银:分析纯,国药集团化学试剂有限公司;乙二胺四乙酸纳、氨水:分析纯,北京北化精细化学品有限责任公司;85%水合肼:分析纯,北京市旭东化工厂;103Pd和110Agm溶液:放射性浓度均为3.7TBq/L,原子高科股份有限公司产品。
2 实验方法
2.1 载体预处理
载体为直径0.5mm,长度3mm的银棒。首先,将载体放入无水乙醇浸泡30min,用沸水清洗后烘干,然后对载体进行敏化和活化。敏化液组成:N2H4和 NH3的混合溶液,分别配制0.5、1.0、1.5、2.0、2.5、3.0、4.0、5.0mmol/L的PdCl2活化液,考察不同活化液浓度对镀膜的影响。将载体分别放入敏化液和活化液中,至载体表面变成深褐色时取出,在高温下干燥至恒重。
2.2 化学镀法制备103Pd-110Agm合金膜
将预处理后的载体置于镀液中进行化学镀。镀液组成列于表1,操作条件列于表2。对镀液中钯银摩尔比、金属离子总浓度、氨水浓度(NH3·H2O)、还原剂肼浓度(N2H4)、络合剂乙二胺四乙酸二钠浓度(Na2EDTA)、温度、时间、转速等条件进行优化。
向容器中依次加入 PdCl2、AgNO3、Na2EDTA、NH3·H2O、N2H4溶液,使镀液总体积为3mL,加入15根小银棒,采用103Pd、110Agm作为示踪剂,103Pd、110Agm放 射 性 活 度 分别约为20、30MBq/L,用移液器取100μL上清液。调节水浴温度及旋转搅拌器的转速,控制反应时间,进行化学镀,待反应完成后,用移液器取100μL上清液,然后取出银棒,用蒸馏水清洗三次,用γ井型探测器测量镀液前后上清液及银棒的活度。考虑到化学镀过程的稳定性,避免膜中引入其他金属离子,采用络合系数较大的Na2EDTA作为络合剂,NH3·H2O作为pH调节剂,采用水合肼作为还原剂。

表1 镀液组成

表2 操作条件
2.3 103Pd-110Agm 合金膜的检测
采用扫描电镜定性分析103Pd-110Agm合金膜的表观形貌,γ井型探测器定量分析膜中103Pd、110Agm含量。
3 结果与讨论
3.1 预处理结果
预处理前后银棒表面状态扫描电镜结果示于图1。图1b为PdCl2溶液浓度为1.0时银棒表面电镜图。比较图1a和图1b可见,银棒处理后表面有晶体出现。实验结果表明,PdCl2溶液的浓度范围在0.5~2.0mmol/L时可以有效地接种103Pd;如果PdCl2的浓度过高会导致接种过程难于控制,镀膜表面会有断层现象,而浓度过低时接种过程较缓慢。

图1 预处理前后银棒表面状态
3.2 钯银摩尔比对镀膜的影响
沉积收率和膜中Ag的摩尔百分含量随钯银摩尔比的变化曲线示于图2和图3。由图2和图3可知,钯银摩尔比对化学镀110Agm的沉积收率影响较小,110Agm沉积收率一直保持在99%以上。4Ag(NH3)4++N2H4+4OH-=4Ag0+16NH3+N2+4H2O与2Pd(NH3)42++N2H4+4OH-=2Pd+8NH3+N2+4H2O电极电位相比,银的还原反应电极电位较大,相同的反应条件下,Ag比Pd更容易发生沉积反应,即Pd和Ag化学共沉积中的Ag优先沉积,相对于Pd的沉积反应,Ag能够在更低的反应物浓度和较弱的络合条件下发生反应,因此,在低Ag含量镀液中,Ag的沉积反应进行的更彻底,沉积收率更高。图3中,当镀液中Ag的摩尔百分含量超过40%时,镀膜将是纯银膜,低于40%,膜中的银含量与镀液中银含量呈线性关系,为保证镀层是合金膜,且103Pd有较高的沉积收率,最终选择Pd与Ag摩尔比为9∶1。

图2 沉积收率随钯银摩尔比变化曲线
3.3 金属离子总浓度对镀膜的影响

图3 膜中Ag摩尔百分含量随钯银摩尔比变化曲线
沉积收率和膜中Ag的摩尔百分含量随金属离子总浓度的变化曲线分别示于图4和图5。由图4可以看出,随着金属离子总浓度的升高,沉积收率也随之升高,因为金属离子总浓度作为M+N2H4+OH-→M+NH3+N2+H2O的反应物,参与化学反应,升高反应物的浓度,反应向正方向进行,沉积收率升高。但是金属离子总浓度过高时,反应速率过快,有少量的金属离子会沉积在容器壁上,所以沉积收率会略有下降,由于Ag的反应速率比Pd快,所以下降的更明显,但是下降幅度不会太大,溶液中的络合剂Na2EDTA和NH3会控制溶液中游离金属离子的浓度,从而控制反应速度。由图5可知,金属离子总浓度低时,Ag比Pd更容易被还原,因为Ag比Pd更具有反应竞争力。综合考虑节约资源和降低成本,使金属离子保持较高的沉积收率,最终确定金属离子总浓度为5~7mmol/L。
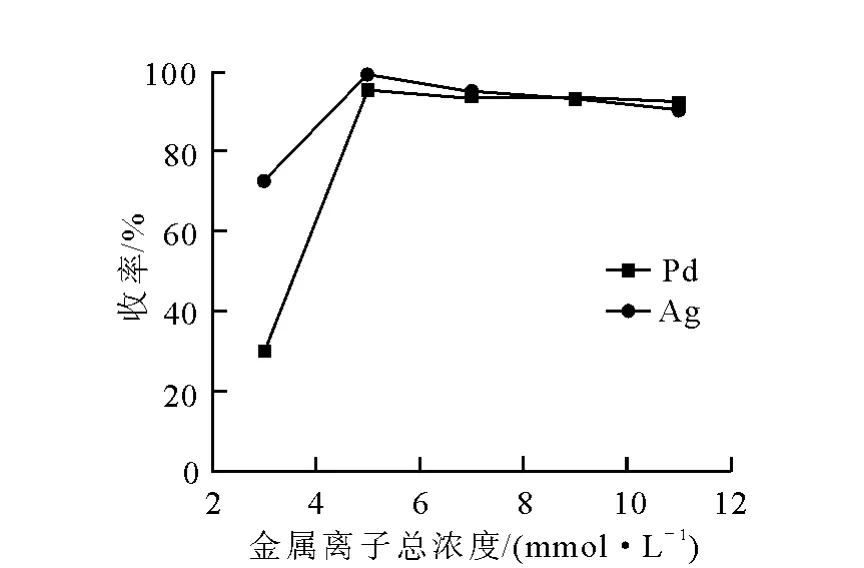
图4 沉积收率随金属离子总浓度变化曲线

图5 膜中Ag摩尔百分含量随金属离子总浓度变化曲线
3.4 NH3·H2O浓度对镀膜的影响
沉积收率及膜中Ag摩尔百分含量随NH3·H2O浓度变化曲线分别示于图6和图7。由图6和图7可知,NH3·H2O浓度在一定范围内,两种金属的沉积收率基本保持不变,但NH3·H2O浓度过高时,镀液不稳定,膜中沉积收率降低。NH3·H2O除了提供N2H4发生氧化还原反应所需的OH-,还能够络合金属离子,在一定范围内,对两种金属的沉积收率影响不大,但当NH3·H2O浓度过高时,使金属离子总浓度比自由离子的浓度降低,而且镀液稳定性降低,沉积收率也随之降低。NH3·H2O浓度较高时,Ag容易被还原,NH3·H2O浓度较低时,Pd容易被还原。为保证化学镀过程两种金属离子沉积收率较高,最终选择NH3·H2O浓度为2~4mmol/L。

图6 沉积收率随氨浓度变化曲线

图7 膜中Ag摩尔百分含量随NH3·H2O浓度变化曲线
3.5 N2H4浓度对镀膜的影响
沉积收率和膜中Ag的摩尔百分含量随N2H4浓度的变化曲线分别示于图8和图9。由图8可知,两种金属的沉积收率随N2H4浓度升高而升高,当N2H4的浓度为10mmol/L时,沉积收率趋于平衡,N2H4的浓度≥15mmol/L,镀液不稳定。化学反应过程中,N2H4的浓度较低时是控制性反应物,当N2H4过量时,不再是控制性反应物,反应已达到平衡。还原剂用量过大时,N2H4本身存在自分解使镀液不稳定。由图9可知,N2H4浓度较高时,更有利于103Pd的还原反应。综上所述,最终肼的浓度确定为10mmol/L。
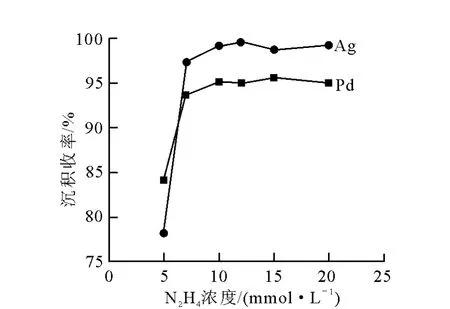
图8 沉积收率随N2H4浓度变化曲线

图9 膜中Ag摩尔百分含量随N2H4浓度变化曲线
3.6 Na2EDTA浓度对镀膜的影响
沉积收率和膜中Ag的摩尔百分含量随Na2EDTA浓度的变化曲线分别示于图10和图11。由图10可知,Na2EDTA的浓度在0.05~0.2mol/L 范 围 内,沉 积 收 率 趋 于 平 衡,Na2EDTA浓度过高会降低金属离子的沉积收率。Na2EDTA通过与金属离子络合来调节自由金属离子浓度,随着Na2EDTA的加入,金属离子与Na2EDTA形成络合物吸附在镀膜表面,使金属离子络合物活性增强,沉积收率增加。但当Na2EDTA浓度过大时,促使金属离子以稳定的络合物形式存在,镀液中自由金属离子浓度下降,沉积收率降低。图11中,Na2EDTA浓度高时,镀液中自由的金属离子浓度降低,但103Pd离子浓度降低的更明显。考虑到使两种金属离子沉积收率最高,确定Na2EDTA浓度为0.15mol/L。
3.7 温度对镀膜的影响
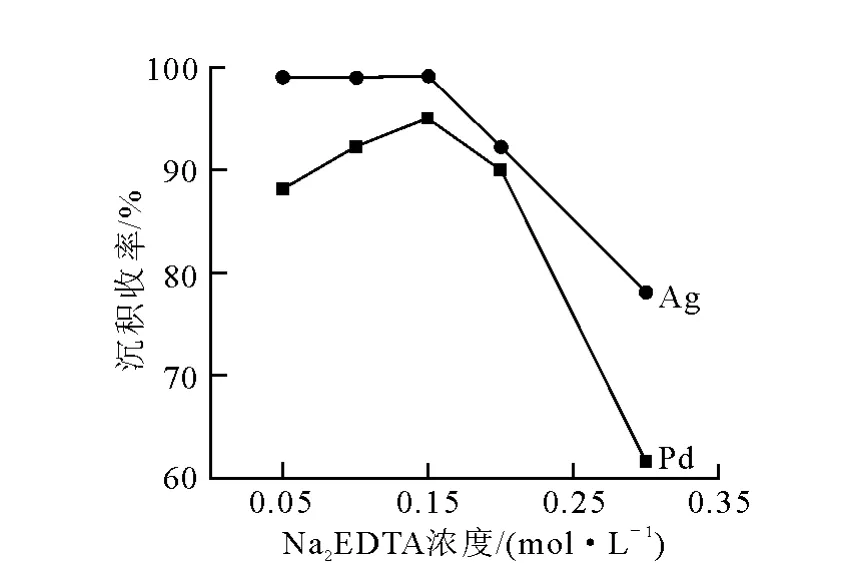
图10 沉积收率随Na2EDTA浓度变化曲线

图11 膜中Ag摩尔百分含量随Na2EDTA浓度变化曲线
沉积收率和膜中Ag的摩尔百分含量随镀液温度变化曲线分别示于图12和图13。由图12可知,103Pd、110Agm的沉积收率都随温度的升高而增大。由图13中可知,在40℃时,103Pd离子不能有效实现化学镀,镀膜是纯银膜。随着温度的升高,膜中的银含量趋于平稳。在60℃时,化学镀效率达到最大值,70℃时镀液中出现黑色悬浮物,镀液不稳定。在一定范围内,这两种金属的沉积反应是吸热反应,温度越高,镀速越快,同时减少了浓差极化,沉积收率越高。但超过这一范围时,氨会挥发,肼会分解,金属不会在载体上沉积,而是被还原在镀液中,造成镀液不稳定,沉积收率下降。综合考虑沉积收率和反应速率,确定化 学 镀103Pd-110Agm合 金 的 最 佳 温 度 为60℃。
3.8 时间对镀膜的影响
沉积收率和膜中Ag的摩尔百分含量随镀膜时间的变化曲线分别示于图14和图15。由图14可见,随着时间延长,Ag的沉积收率基本不受影响,Pd的沉积收率随时间的延长而升高。由于Ag的反应速率较快,可以在较短时间内达到平衡,而Pd的反应速率较慢,Pd的沉积收率随时间的延长而缓慢升高。图14和图15可见,反应60min后达到平衡,因此确定化学镀时间为60~90min。
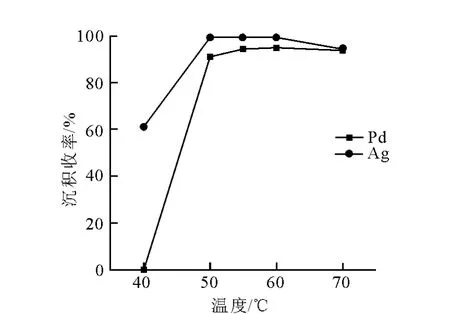
图12 沉积收率随温度变化曲线

图13 膜中Ag摩尔百分比随温度变化曲线

图14 沉积收率随时间变化曲线

图15 膜中Ag摩尔百分比随时间变化曲线
3.9 旋转搅拌器转速对镀膜的影响
沉积收率和膜中Ag的摩尔百分含量随旋转搅拌器转速的变化曲线分别示于图16和图17。由图16和图17可见,转速对103Pd和110Agm的化学镀沉积收率、膜中110Agm的摩尔百分含量影响均不大。在此氧化还原反应中,决定化学镀沉积收率的因素是该反应的电动势。而转速的大小并不会影响反应的电动势。但转速会影响化学镀膜的表观形态,当转速较高时,膜的表观形态是具有光亮的金属光泽,而转速较低时,膜的表观形态则是灰黑色。不同转速下镀膜的表观形态电镜图示于图18。由图18可见,低转速时金属晶体之间排列较松散,高转速时金属晶体之间排列较紧密。这是由于转速较慢时,金属离子的沉积速度较慢,晶体微粒生长的较大,堆积不紧密,由于光的漫反射作用,膜表面呈现出灰黑色;相反,当转速较快时,沉积速度较快,晶体微粒较小,堆积紧密,由于光的镜面反射作用,此时膜表面呈现出光亮的金属光泽。综合膜的表面形态和沉积收率,确定转速为40~60r/min。

图16 沉积收率随转速的变化曲线

图17 膜中Ag摩尔百分含量随转速变化曲线
3.10 镀膜的定性分析
取几根化学镀过程中不同阶段的银棒,在扫描电镜下进行表观和能谱分析,结果示于图19。对比分析图19中不同阶段银棒的表观形貌可见,预处理后,银棒表面有晶体生长,化学镀后银棒表面形成了一层致密的金属膜。合金膜能谱图结果示于图20。由图20可知,镀层中含有两种元素分别是103Pd和110Agm,分析结果与理论一致。

图18 转速影响镀膜的表观形态电镜图

图19 膜的表观形貌

图20 合金膜能谱图
3.11 合金膜定量分析
103Pd沉积实验结果列于表3。表3中A是γ井型探测10s的总计数,按照沉积收率S1=×100%计算103Pd沉积收率>93%,三次测量103Pd沉积收率的标准差为0.81%。103Pd能量较低,容易受到载体的影响,按照吸收率D1=(1-×9/15)×100%(式中9为比例倍数,15为银棒总数)计算载体银棒对103Pd的吸收率约为58%,银棒对103Pd吸收率的标准偏差为0.80%。三次实验标准差较小,说明该反应过程稳定,重复性好。
110Agm沉积实验结果列于表4。由表4可知,按照S=2×100%计算,110Agm沉积收率>98%,110Agm沉积收率的标准差为0.54%。110Agm能量较高,载体对其能量影响很小,按照D2=(1-×9/15)×100%计算载体银棒对110Agm的吸收率约15%,银棒对110Agm吸收的标准偏差为0.099%。三次实验标准偏差较小,说明该反应过程稳定,重复性好。
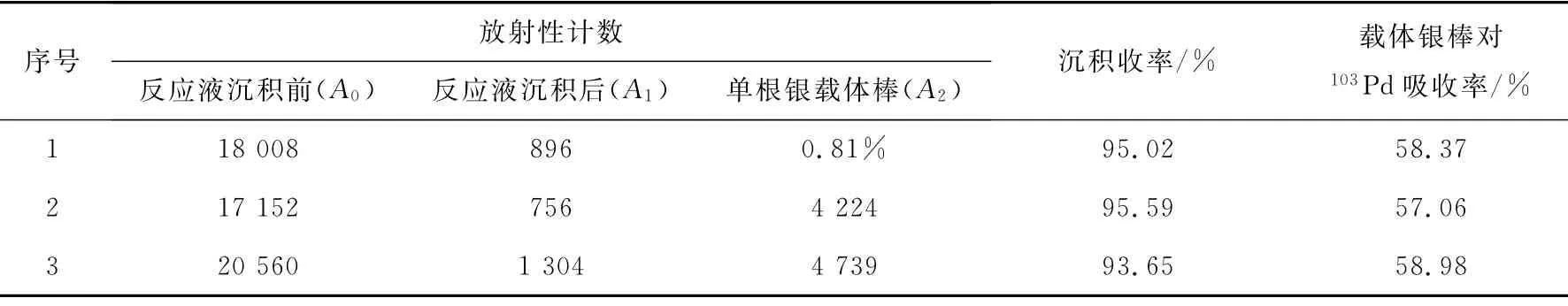
表3 103Pd沉积实验

表4 110 Agm 沉积实验
4 小 结
化学镀法制备103Pd-110Agm合金膜,优化后镀液组成为:103Pd与110Agm摩尔比为9∶1;金属离子总浓度为5~7mmol/L;NH3·H2O浓度 2~4mol/L;pH 10~12;N2H4浓度为10mmol/L;Na2EDTA浓度0.15mol/L;恒温水浴槽保持温度为60℃时,旋转搅拌器转速40~60r/min,反应时间为60min。在该条件下进行化学镀,103Pd沉积收率>93%,110Agm沉积收率>98%,载体银棒对103Pd吸收率约为58%,对110Agm的吸收率约为15%。
[1] 王俊杰,庄永志.放射性粒子近距离治疗肿瘤[M].北京:北京大学医学出版社,2001:12-17.
[2] 王和义,傅依备,邢丕峰,等.浆料涂敷-化学镀技术在微孔陶瓷表面沉积钯银合金膜[J].膜科学与技术,2000,20:25-29.
[3] 增高峰,史蕾,徐恒泳.用化学镀法制备Pd/Ag膜时膜厚和组成的控制[J]催化学报,2009,30:1 227-1 232.
[4] 李亮,余桂郁,杨南如.化学镀法制备钯银陶瓷合金透氢膜 [J].南京化工大学学报,1998,20:1-4.
[5] Cheng YS,Yeung KL.Palladium-silver composite membranes by electroless plating technique[J].Journal of Membrane Science, 1999, 158:127-141.
[6] David A,Pacheco T,Margot A,et al.Preparation of palladium and silver alloy membrane on a porousα-alumina tube via simultaneous electroless plating[J].Journal of Membrane Science,2005,247:21-27.
[7] Junya O,David A,Pacheco T,et al.Hydrogen permeability study of the thin Pd-Ag alloy membranes in the temperature range across theα-β phase transition[J].Journal of Membrane Science,2006,282:370-374.
[8] 李宁.化学镀实用技术[M].北京:化学工业出版社,2004:308-317.
