DMDAAC-AM辐射接枝淀粉基水凝胶的制备与吸水性能研究
2012-05-16郭正潮刘文涛何素芹朱诚身宋伟强
郭正潮,梁 佳,刘文涛,何素芹,朱诚身,宋伟强,2
(1.郑州大学 材料科学与工程学院,河南 郑州 450001;2.河南工业大学 材料科学与工程学院,河南 郑州 450001)
水凝胶是一种经适度交联而具有三维网络结构的新型功能高分子材料。水凝胶材料以其独特的吸水、保水和良好的生物相容性广泛应用于农业、工业、医药、环保和生物工程材料领域[1-2]。辐射法制备水凝胶因操作简单、无须添加交联剂和引发剂等优点而受到关注[3-4]。与化学引发方法相比,辐射引发方法具有操作简便、可控性好等优点[5-7],特别是不使用化学引发剂,没有引发剂残留,因而可以广泛应用于对洁净度要求较高的领域。
二甲基二烯丙基氯化铵(DMDAAC)是一种阳离子水溶性单体,这类含胺基单体接枝淀粉的反应较为困难,所以需要加入合适的促进剂,现有文献中一般是DMDAAC与丙烯酰胺(A M)接枝共聚淀粉。该阳离子接枝的淀粉基水凝胶二次污染小、可生物降解。目前已经有研究人员用化学引发的方法制得了淀粉、丙烯酰胺、二甲基二烯丙基氯化铵接枝共聚物[8-9],但采用辐射引发制备淀粉接枝DMDAAC-AM的相关研究还未见报道。本工作拟通过DMDAAC、A M与天然高分子化合物淀粉的接枝共聚,在交联剂N,N’-亚甲基双丙烯酰胺的作用下得到兼有天然和合成高分子两者特性的阳离子淀粉凝胶,并对其性质进行研究。
1 材料和方法
1.1 主要原料及设备
食用玉米淀粉:青岛海达尔淀粉有限公司;二甲基二烯丙基氯化铵(DMDAAC):工业级,65%水溶液,山东鲁岳化工有限公司;丙烯酰胺(A M)、N,N’-亚甲基双丙烯酰胺(MBA):分析纯,天津科密欧化学试剂开发中心;丙酮:分析纯,天津化学试剂一厂;冰醋酸:分析纯,天津化学试剂三厂。
H H W-2型数显恒温水浴箱:金坛市双捷实验仪器厂;DFZ-6050型真空干燥箱:上海精密仪器仪表有限公司;梅特勒-托利多AL104型电子分析天平、JJ-1精密增力电动搅拌器:金坛市宏华仪器厂;60Co放射源:活度7.4 PBq,河南省科学院同位素研究所生产;FTS-135红外光谱仪:美国BIO-RAD公司产品。
1.2 辐射交联法制备阳离子淀粉凝胶
将6 g淀粉溶解于60 mL蒸馏水中,85℃糊化30 min,冷却至室温。机械搅拌下,加入9.8 g DMDAAC、4.2 g季铵盐和一定量 MBA(必要时可以在50℃水浴中加热促进溶解)。均匀搅拌30 min。充氮气排除空气,密闭封口,置于辐照室内辐照一定时间,使样品吸收剂量达到3 k Gy。之后取出凝胶,切成约5 mm的等高小柱体。将切割后的凝胶放入真空烘箱中,60℃干燥至恒重。
1.3 红外光谱分析
取凝胶样品,MBA用量为1.6 g的组进行红外光谱分析(FTIR),在红外分析之前,先对该组样品进行纯制:称取一定量的粗品,置入索氏抽提器中,用V(丙酮)∶V(冰醋酸)=50∶50的混合溶剂作为抽提溶剂,回流18 h,以除去均聚物,抽提后的剩余物经真空干燥,取出,得到纯接枝物[10]。
红外分析时,采用溴化钾压片法进行制样,放入FTS-135红外光谱仪进行分析,记录400~4 000 c m-1的红外谱图。
1.4 阳离子淀粉凝胶溶胀比的测定
采用称重法考察阳离子淀粉凝胶吸水后的溶胀动力学。将充分干燥的凝胶样品准确称重,记为m0,放入20℃去离子水中溶胀,每隔一定时间取出凝胶,用湿润的滤纸擦去表面多余的水分,称重,记为m1。称重后再将凝胶重新放入水中,使其继续溶胀。此过程重复多次,直至凝胶达到溶胀平衡,此时凝胶的质量记为meq,依次记录t时刻凝胶溶胀的质量为m2、m3……mt。计算凝胶样品的溶胀比。每种样品测量3次,取其平均值。
分别用(1)式和(2)式计算溶胀比和平衡溶胀比。由于凝胶是一个交联的网状结构,因此可以用Peppas动力学模型对阳离子淀粉凝胶的吸水膨胀行为进行动力学分析。(3)式是Peppas方程,适 用 于 0<St/Seq<0.6 范 围 内 的数据[11-13]。

式中,St为t时间的溶胀比;Seq为平衡时的溶胀比;k为溶胀常数(网络结构常数);n为扩散指数(溶胀特征指数)。
1.5 沉降积的测定
交联淀粉的交联度与沉降积呈线性负相关,因此可以用沉降积间接表示交联度[14-17]。准确称取0.5 g干燥后的交联淀粉样品于100 mL烧杯中,用移液管加25 mL蒸馏水制成质量分数为2%的溶液。将烧杯置于82~85℃水浴中,稍加搅拌,保温2 min,取出冷却至室温;用两支刻度离心管分别倒入10 mL糊化后的淀粉液,对称装入离心机内,开动机器,缓慢加速到4 kr/min;用秒表计时,运转2 min停转;取出离心管,将上层清液倒入另一个同样的离心管中,读出体积V(mL),计算沉降积C(mL)。对同一样品进行3次平行测定。按下式计算沉降积:

2 结果与讨论
2.1 阳离子淀粉凝胶的FTIR分析
纯玉米淀粉和阳离子淀粉凝胶的FTIR谱图示于图1。分析图1a可知,575、765、857、1 096~1 159 c m-1出现淀粉-CH2摇摆振动吸收峰,3 428 c m-1宽峰归属于淀粉的-OH伸缩振动;对比分析图2a可知,阳离子淀粉凝胶的红外谱图中除了淀粉所有的特征峰之外,还有峰3 197 c m-1归属于伯酰胺的—NH伸缩振动,1 656 c m-1归属于C=O伸缩振动(酰胺Ⅰ谱带),1 604 c m-1归属于N-C=O对称伸缩振动(酰胺Ⅱ谱带),1 457 c m-1归属于与-N+相连双甲基(CH3)2的典型对称弯曲振动。1 326 c m-1处为C-N的伸缩振动吸收峰。以上数据可以有效证明阳离子的存在,而1 090 c m-1处为C-O-C的伸缩振动吸收峰,可以辅助说明阳离子改性反应的有效性。
2.2 阳离子淀粉凝胶的溶胀动力学及其分析
阳离子淀粉水凝胶的溶胀行为示于图2。由图2可见,阳离子淀粉凝胶的初始吸水溶胀速率较大,St随着时间的延长而迅速增加;当时间超过10 h后,溶胀比增加缓慢,几乎不再改变,说明达到溶胀平衡。此外,平衡溶胀比大小与MBA用量有关。MBA用量越大,平衡溶胀比越小;不过,在实验条件下,当 MBA用量>1.6 g时,平衡溶胀比相差很小,几乎不再改变。
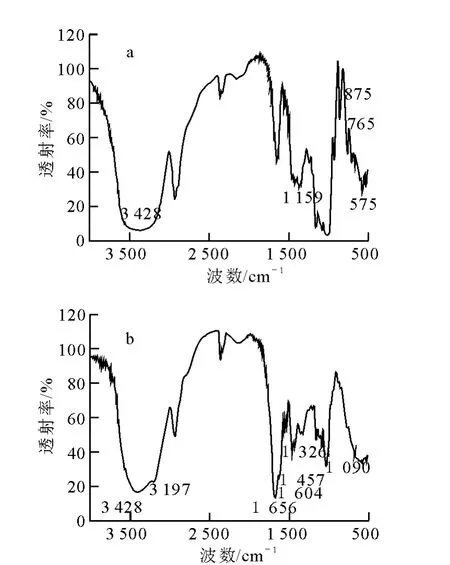
图1 纯玉米淀粉和阳离子淀粉凝胶的FTIR谱a——纯玉米淀粉;b——阳离子淀粉
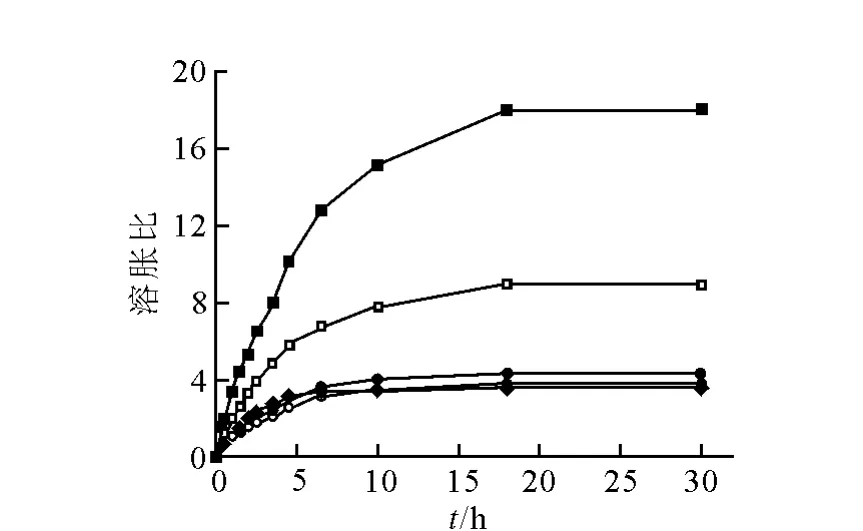
图2 阳离子淀粉水凝胶的溶胀行为□——MBA用量为0.2 g;□——MBA用量为0.4 g;●——MBA用量为1.6 g;○——MBA用量为2.2 g;◆——MBA用量为3.8 g
吸水溶胀是水凝胶的一个重要特征。凝胶的溶胀是一个复杂的过程,通常包括三个连续的过程:1)水分子进入凝胶内部;2)凝胶中高分子链发生松弛;3)整个高分子链在水中伸展,凝胶网络溶胀。凝胶溶胀的过程同时也是小分子水扩散到凝胶内部的过程,所以本工作借助Peppas扩散动力模型来深入分析阳离子淀粉凝胶溶胀的具体过程。用Peppas理论模型对0<St/Seq<0.6范围内的数据进行分析,对(3)式两端取对数,得:

按上式对溶胀比进行线性拟合,由斜率可以得出n,由截距得出k,结果列于表1。

表1 不同交联剂MBA用量下的膨胀常数和扩散指数
根据Peppas模型,当n=0.5时,凝胶的吸水为Fickian扩散;当0.5<n<1时,为不规则的Non-Fickian扩散;当n=1时,凝胶扩散为Casell扩散(聚合物松弛)。不同MBA用量时,阳离子淀粉凝胶的扩散指数n均处于0.56和0.72之间,说明阳离子淀粉凝胶的吸水膨胀过程符合不规则的Non-Fickian扩散,即膨胀过程取决于凝胶中水分子渗透和聚合物网络松弛的共同作用[11]。随着凝胶交联度的增加,凝胶网络孔径变小,溶胀度下降。
2.3 阳离子淀粉凝胶的沉降积
交联剂MBA用量对沉降积的影响示于图3。从图3中可以看出,阳离子淀粉凝胶的沉降积随着交联剂MBA用量的增加而下降。但当MBA用量达到一定量时,沉降积较低,而且不再随MBA用量的增加而呈明显下降趋势。可以说明在辐射条件下不需要使用太多的交联剂就可以形成致密网格的凝胶。
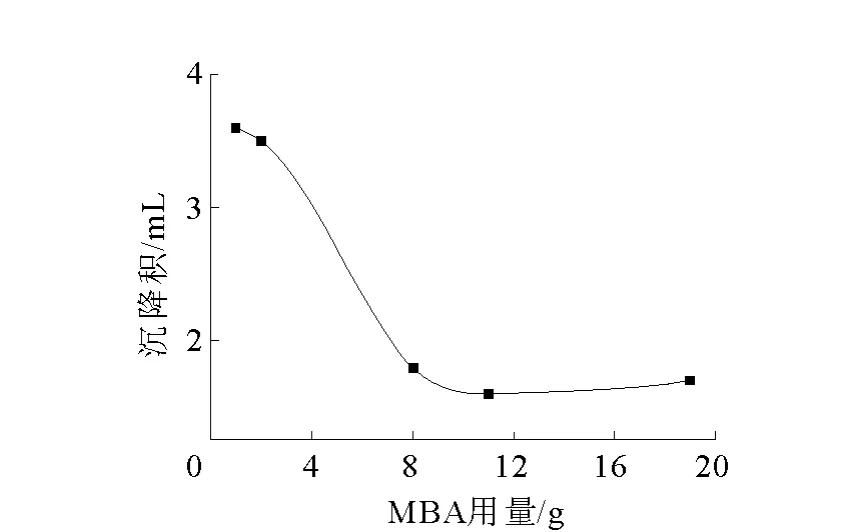
图3 交联剂MBA用量对阳离子淀粉凝胶沉降积的影响
3 结 论
采用辐射接枝/交联技术,可以制备阳离子淀粉凝胶。其中,凝胶的膨胀比与N,N’-亚甲基双丙烯酰胺交联剂的用量有关,随着交联剂用量的增加而下降。而当交联单体的用量较高时膨胀比相差不大。用Peppas模型对凝胶的吸水膨胀动力学进行研究表明,阳离子淀粉凝胶的吸水溶胀符合Non-Fickian扩散机制。此外,阳离子淀粉凝胶的沉降积随着N,N’-亚甲基双丙烯酰胺交联剂的用量增加而下降。
[1] 顾雪荣,朱育平.凝胶化学[M].北京:化学工业出版社,2005:250-323.
[2] Peppas NA.Hydrogels in medicine and phar macy,f undamentals,preparation method and str ucture of hydrogels[M].Vol I.Boca Raton:CRS Press,Florida,1986.
[3] 赵新,崔建春,刘多明,等.辐射合成水凝胶的结构与溶胀特性[J].高分子学报,1994,(5):600-603.
[4] 陈玉伟,王建龙.辐射诱导合成水凝胶及其处理重金属废水的研究进展[J].化学进展,2009,21(10):2 250-2 256.
[5] 石文娟,赵国华.辐射变性淀粉研究进展[J].食品工业科技,2008,29(2):305-307.
[6] 陈惠元,彭志刚,丁钟敏,等.辐射技术在淀粉改性中的应用[J].核化学与放射化学,2007,29(1):53-56.
[7] Naotsugu Nagasawa,Toshiaki Yagi,Tamikazu Ku me.Radiation crosslinking of car boxy methyl starch[J].Car bohydrate Poly mers,2004,58:109-113.
[8] 范宏,陈卓.淀粉/DMDAAC-A M 接枝共聚物的合成及表征[J].高分子材料科学与工程,2002,18(5):62-65.
[9] Liu QX,Li JL,Xu WC.Preparation and application of starch-acrylamide-dially di methyl ammoniu m chloride graft copoly mer[J].Mater Sci For u m,2011,675-677:403-406.
[10]李永红,李海燕,张普玉.淀粉与二甲基二烯丙基氯化铵的接枝共聚研究[J].河北化工,2006,29(11):30-32.
[11]Thakur A,Waachoo RK,Singh P.Structural parameters and swelling vehavior of PH sensitive ploy(acrylamide-co-acrylic acid)hydrogels[J].Chem biochem Eng Q,2011,25(2):181-194.
[12]陈俊.基于聚(N,N’一二乙基丙烯酸胺)的温度和p H值敏感性水凝胶的合成及其性能研究[D].兰州:兰州大学,2010.
[13]Peppas NA,Merrill EW.Hydrogels as swollen elastic net works[J].Journal of Applied Poly mer Science,1977,21:1 763-1 770.
[14]张友松.变性淀粉生产与应用手册[M].北京:中国轻工业出版社,1999.
[15]张钟,刘正,蔡治华,等.糯玉米交联淀粉的制备及性质研究[J].中国粮油学报,2002,17(2):31-33.
[16]徐忠,周美琴,杨成.交联淀粉的制备工艺研究[J].食品科学,2008,29(8):194-196.
[17]王占忠,刘钟栋,陈肇锬.小麦交联淀粉的制备及性质的 研 究 [J].中 国 粮 油 学 报,2004,19(1):26-30.
