一种苯并咪唑类荧光传感器的合成和对Zn2+的识别研究
2012-04-26周成勇谢承志
高 巍,周成勇,谢承志
(1.长治学院 化学系,山西 长治 046011;2.天津医科大学 药学院,天津 300192)
1 引言
作为生命体系中众多的微量元素之一,Zn2+是细胞内很多酶和转录因子的重要组成部分[1-4]。有研究表明,Zn2+可能是细胞新陈代谢的主要调控因子[1,5],近些年来,锌离子在神生物学领域也得到了人们极大地关注,其在神经递质传递过程中起着重要作用[6-8],同时,在视网膜[9]、胰腺[10]、肠[11]等一些组织器官中,也发现了游离的锌离子。
虽然Zn2+在生命体系中有着重要的作用,但其很多的作用机制目前还不清楚。因此,发展特异性识别Zn2+的传感器尤为重要。
荧光化学传感器由于其特有的高灵敏度与低检出限,长久以来成为人们分析检测生命体系和环境中各种阴、阳离子和生物小分子的重要手段。本文合成了一种对Zn2+有特异性响应的苯并咪唑衍生物HA,通过荧光滴定光谱、Job’s Plot、紫外可见光谱等手段对其识别机制进行了研究。
2 实验部分
2.1 实验仪器和试剂
邻苯二胺、氨基乙酸、冰乙酸、水杨醛、浓氨水、乙腈均为分析纯试剂。
Hitachi U-3900紫外可见分光光度计,Hitachi F-4600荧光光谱仪,红外光谱仪。
2.2 实验方法
合成了一个Zn2+探针HA,通过荧光光谱以及紫外可见吸收光谱等手段对HA 在乙醇溶剂中和对Zn2+的响应进行了研究。所用的HA 溶液为2.5 mmol/L的乙醇溶液。在荧光光谱研究中HA 的浓度为6.25μmol/L。狭缝宽度为激发2.5 nm,发射2.5 nm,激发波长为318 nm。
紫外可见光谱中HA 的浓度为5μmol/L,Zn2+浓度为5μmol/L。
2.3 化合物HA 的合成和表征

图1 HA 的合成线路图
将1 mmol的邻苯二胺和1 mmol氨基乙酸加入到100 ml烧瓶中,加入15 ml冰乙酸,搅拌下升温至溶解。缓慢加入1 mmol的水杨醛,逐渐升温至140℃反应2 h,抽滤并收集滤液,用浓氨水调节pH值至中性,有大量淡黄色沉淀生成。抽滤,干燥,用乙腈重结晶,得到淡黄色粉末HA。红外分析:3324(OH),1632(C=N),3324(NH伸缩),1591(NH弯曲)
3 结果与讨论
3.1 荧光光谱研究
3.1.1 荧光滴定光谱

图2 荧光滴定光谱
荧光滴定实验在乙醇溶液中进行。将5μl 2.5 mmol/L的HA加入到盛有2 mL乙醇的比色皿中,化合物在318 nm激发光照射下呈现出蓝色荧光,每隔4分钟向体系中加入1μl浓度为1 mmol/L的Zn2+。由图2可以看出,荧光光谱发生蓝移,454 nm处的荧光发射强度逐渐降低,在403 nm处出现新的荧光发射并随着Zn2+浓度的增大而逐渐增强。当二者的浓度比为1:1时,体系荧光光谱趋于稳定。由此可以初步推断,化合物HA 和Zn2+之间通过配位结合成了1:1的配合物。由于Zn2+的配位,使得配体分子HA 发生扭曲,从而使刚性降低,共轭效应减弱,最终导致荧光光谱发生了蓝移并且强度降低。
3.1.2 Job’s Plot

图3 Job’s Plot工作曲线
设计了Job’s Plot实验来进一步认证反应的摩尔比,纵坐标为403 nm处的荧光强度,横坐标为[Zn2+]/([HA]+[Zn2+]),通过图3我们可以看到Zn2+与HA 的反应摩尔约为1:1,每个Zn2+提供四个配位点而HA 为三齿配体占据三个位点,第四个配位点被溶剂分子或离子占据,从而形成四面体型锌配合物。
3.1.3 离子选择性实验
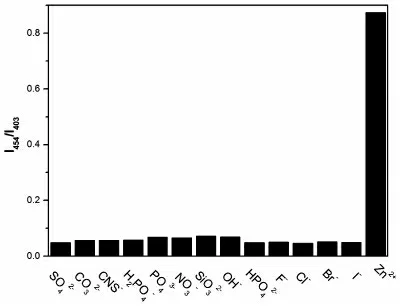
图4 阴离子选择性实验

图5 阳离子选择性实验
文章设计了离子选择性实验来考察探针分子HA对Zn2+识别的选择性。在离子选择性实验中HA 的浓度为6.25μmol/L,所有阴离子的浓度为40μmol/L,阳离子浓度为6.25μmol/L。实验结果表明探针分子HA 只对Zn2+表现出了较好的选择性。在图5中,由于Cu2+、Co2+、Ni2+等自身的单电子结构从而在一定程度上造成了体系荧光的猝灭。
3.2 紫外可见光谱
由HA 及ZnHA的紫外可见光谱不难看出,Zn2+的加入对体系的吸收光谱产生了较大影响。位移主要发生在300-370 nm范围内,这一变化主要是Zn2+与HA 的N、O之间形成的配位键而产生的吸收导致的,这进一步证明HA与Zn2+之间发生配位而形成了配合物。

图6 HA与ZnHA的紫外可见光谱
4 结论
本文发展了一种特异性的Zn2+荧光探针HA,该化合物在有Zn2+存在的情况下,荧光光谱发生蓝移,斯托克位移达51 nm,并且对Zn2+的响应具有特异性,可以用于体系中Zn2+的含量测定。荧光滴定实验、job’s plot实验以及紫外可见光谱表明:该探针分子通过配位键与Zn2+之间形成了比例为1:1的配合物。本研究为Zn2+的识别和检测提供了一种新手段,也对Zn2+相关的疾病预防和检测有积极的意义。
[1]T. V. O’Halloran,Science,1993,(261):715-725.
[2]B. L. Vallee and K. H. Falchuk,Physiol. Rev.,1993,(73):79-118.
[4]C. J. Frederickson,J. Y. Koh and A. Ⅰ. Bush,Nat. Rev.Neurosci.,2005,(6):449-462.
[3]J. M. Berg and Y. Shi,Science,1996,271 .1081-1085.
[5]J. J. R. Frausto Da Silva and R. J. P. Williams,OxfordUniversity Press,Oxford,1991,p. 561.
[6]S. Y. Assaf and S. H. Chung,Nature,1984,(308):734-736.
[7]S. Ueno,M. Tsukamoto,T. Hirano,et al,J.Cell Biol.,2002,(158):215-220.
[8]A. M. Hosie,E. L. Dunne,R. J. Harvey et al,2003,(6):362-369.
[9]S. Redenti,H. Ripps and R. L. Chappell,Exp.Eye Res.,2007,(85):580-584.
[10]M. F. Dunn,BioMetals,2005,(18):295-303.
[11]L. J. Giblin,C. J. Chang,A. F. Bentley,et al.Cytochem.2006,(54):311-316.
