多孔结构Li3V2(PO4)3/C正极材料的制备及电化学性能
2012-04-23刘素琴黄可龙房雪松
张 新, 刘素琴*, 黄可龙, 房雪松, 程 凤
(中南大学化学化工学院,湖南长沙 410083)
NASICON结构的Li3V2(PO4)3具有结构稳定、工作电位高(3.16~4.15 V,vs.Li/Li+)、理论比容量较高(197mAh/g)和优良的循环稳定性等优点[1-2],被认为是有巨大发展潜力锂离子电池的正极材料之一。然而同其它聚阴离子化合物一样,Li3V2(PO4)3存在较大电流密度下充、放电比容量低,即材料的电导率较低的缺陷[3-5]。通常的解决方法是对其进行高导电材料包覆、过渡金属掺杂或控制活性粒子的尺寸[6-8]。
多孔材料具有较大的比表面积,可以增强活性物质与电解液的接触,从而提高了材料的反应活性位点;该形貌易于高电导率的电解液的渗入,提高了材料的锂离子扩散速度;电解液在多孔材料内部的渗入也缩短了锂离子的扩散距离。多孔材料的特性对锂电正极材料电化学性能有着明显改善作用,Gaberscek[9]等通过溶胶凝胶法合成多孔LiFePO4/C复合材料,该材料表现出优越的电化学性能,即使在3 400mA/g倍率下循环50次,再在低倍率下循环材料仍有良好的放电比容量。Fan[10]等由简易的一步法制备得到多孔Li2FeSiO4/C材料,材料的循环性能得到有力的改善。然而,目前国内外对多孔结构Li3V2(PO4)3/C复合材料材料的研究仍鲜有报道。
本文采用高温固相法以Li2CO3、NH4H2PO4、V2O5、草酸及淀粉为原料成功合成出多孔结构Li3V2(PO4)3/C复合材料,并对其物理及电化学性能进行研究。
1 实验材料和方法
1.1 材料合成
以Li2CO3(天津市化学试剂研究所,AR),V2O5(湖南湘中精细化学品厂,AR),NH4H2PO4(上海试剂一厂,AR),草酸(长沙湘科精细化工厂,AR)以及淀粉(湖南师范大学化学试剂厂,AR)为原料。将一定化学计量比的混合物置于高速行星式球磨机中球磨5 h后置于100℃真空干燥箱内干燥6 h,再将该混合物送入SR-JX-4-13型马弗炉 (长沙市远东电炉厂)300℃左右预处理5 h,自然冷却后再移入管式炉中在氩气保护下以不同温度焙烧10 h,得到Li3V2(PO4)3/C样品。
1.2 样品表征与测试
用XD-98型全自动X射线衍射仪(XRD)进行样品的物相分析,测试条件:Cu Kα靶,管电压为40 kV,管电流40mA,扫描范围10°~70°,扫描速度为4.0(°)/m in。在JSM-6390型扫描电镜上进行形貌观察。
将合成样品、乙炔黑、PTFE按质量比80∶15∶5的比例混合均匀后涂于约1 cm2的铝箔集流体上,120℃干燥12 h后,20MPa下压片制成正极。在充满氮气保护的MBRAUN手套箱中进行电池组装。以锂片作为负极,电解液为1mol/L LiPF6/EC+DMC+EMC(体积比1∶1∶1),组装成模拟电池。充放电测试采用武汉蓝电电子有限公司生产的LandBTI240电池测试系统,充放电电压范围为3.0~4.3V。采用IM6电化学工作站进行交流阻抗测试,测试电位4.3 V,频率范围100 kHz~0.01 Hz,正弦波振幅为5mV。每个电池在测试之前都在测试电位下恒压约3 h。
2 实验结果与讨论
2.1 样品XRD及SEM分析
图1为不同烧结温度下所得Li3V2(PO4)3/C样品的XRD衍射图。从图可以看出经700℃煅烧的样品有少量杂相,这是由于烧结温度低,不利于离子的扩散。在相同的时间内,Li3V2(PO4)3的构晶离子(Li+、V3+、PO34-)来不及重排,从而造成了杂相的生成。随着温度的升高,在750、800、850℃煅烧所得的各个样品没有发现其它杂相,都为具有P21/n空间群的单斜晶系结构的纯相晶体,这与参考文献[11-13]研究结果相吻合,其原因是温度升高原子振动加剧,离子的扩散速度增大,有利于晶体的生长。同时发现样品各晶面的衍射峰相对强度随着温度的升高而变强,材料的结晶性能更好。另外,在图1的所有XRD图谱中没有碳的衍射峰,这证明实验所引入的碳为无定形碳或者含量少且不影响Li3V2(PO4)3的结构。

为了考察温度对材料形貌的影响,对不同烧结温度下所得Li3V2(PO4)3/C样品进行SEM检测,其结果如图2所示。从图2(a)中,可观察到700℃烧结的样品没有明显的多孔结构,其原因可能在于烧结温度过低,不利于多孔的形成。当温度提高到750℃时,材料出现多孔结构,尤其是800℃合成的材料孔隙大而且多,而到850℃时材料孔隙减少,其原因可能在于温度过高,材料严重团聚,导致孔隙的减少。由SEM图发现材料多孔形貌与烧结温度有着密切关系:温度太低不利于多孔的形成,而温度过高就会造成材料的过度团聚从而影响孔隙的数量与大小,只有在适当的温度下才能制备出形貌优越的多孔材料。

2.2 多孔Li3V2(PO4)3/C形成机理
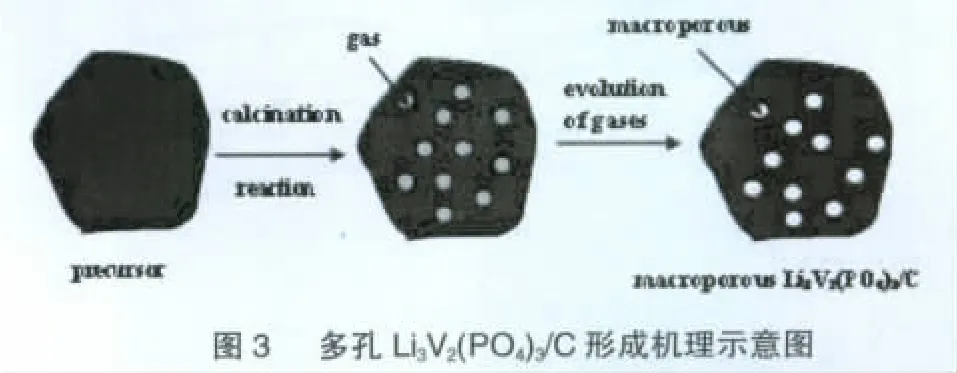
多孔材料的形成主要原因在于实验中大量气体的产生,其反应方程式如下[14]:2 V2O53 Li2CO3+6 NH4H2PO4+4 HOOCCOOH·H2O→2 Li3V2(PO4)3+11CO2+6NH3+21 H2O。Dominko[15]等以柠檬酸铁为原料,不论是以高温固相法还是溶胶凝胶法,都成功地制备出多孔结构LiFePO4/C,他们认为多孔结构的产生是由于柠檬酸根阴离子分解产生大量气体而导致的。另外Prakash[16]等依据燃烧法能产生大量气体的原理合成出多孔状Li4Ti5O12。因此,我们模拟出多孔Li3V2(PO4)3/C复合材料形成机理图,如图3所示。步骤Ⅰ:前驱体在高温煅烧时材料发生反应,产生大量气体,大量气体聚集在材料内部造成孔隙的形成。步骤Ⅱ:当材料内部气体排出后便形成了多孔状材料。
2.3 样品充放电性能
图4给出了不同烧结温度下所得Li3V2(PO4)3/C样品0.1 C首次充放电曲线图,充放电压范围为3.0~4.3 V。各个样品充放电曲线都表现出三个平台,分别对应Li3V2(PO4)3中两个锂离子的脱出,第一个锂离子脱出对应的3.6 V和3.7 V,第二个锂离子脱出对应的是4.1 V[17]。700、750、800℃和850℃烧结的Li3V2(PO4)3/C样品首次放电比容量分别为:108.8、122.7、130.0、126.6mAh/g。800℃温度下烧结的样品具有最高的首次放电比容量,而700℃样品首次放电比容量最低。造成这种差异的原因在于:烧结温度太低,容易造成杂相的产生,同时也影响材料的结晶度,这从XRD图可以容易看出;烧结温度过高,材料团聚严重,影响了多孔的形成,同时团聚的大颗粒不利于锂离子的扩散,在SEM图中850℃烧结的样品存在严重的团聚现象,孔隙明显减少。

下面进一步考察了各样品的循环性能和倍率性能,其结果如图5所示。在0.1 C时700、750、800℃和850℃烧结的Li3V2(PO4)3/C样品在循环20次后放电比容量分别为:102.2、117.0、124.9、119.1mAh/g,容量保持率依次为:93.9%,95.4%,96.1%,94.1%,在低倍率中800℃烧结的样品表现出最佳的循环性能。在高倍率下800℃烧结的样品仍具有最优的放电比容量及循环性能。其中在2C下,各样品首次放电比容量分别为:51.8、77.9、91.5、54.6mAh/g,50 次循环后它们的放电比容量保持率分别为:70.7%,81.9%,93.0%,80.6%。由图5不难发现随着烧结温度的升高,材料的放电比容量与循环性能都先提高后减小,这与形貌随温度的影响变化规律一致。

不同温度烧结的材料的电化学性能之间的差异与材料的形貌有密切关系,这一点可以通过材料与电解液接触模拟图6进行进一步解释:如图6(a)普通的块状材料体积大,比表面积小,电解液不易渗入到材料内部,这样就增加了锂离子的扩散距离,阻碍了锂离子的扩散;而在多孔材料中[图6(b)],多孔的结构有利于电解液的渗入,这样锂离子可以通过渗入的电解液进行扩散从而缩短了锂离子在固体材料内部的传输距离;另外多孔结构增大了材料的表面积,增加了材料与电解液的接触面,反应活性位点得到增多。

2.4 样品交流阻抗分析
为了进一步解释多孔材料电化学性能明显提高的原因,对不同温度下所得的样品进行了电化学阻抗测试。图7为不同温度下所得样品在3次循环后充电至4.3 V[即LixV2(PO4)3中x=1时]稳定三个小时后测得的Nyquist图及其等效电路图。等效电路图中R1表示欧姆电阻;并联电阻R2和电容CRE分别表示锂离子进入到正极材料界面内的电荷转移电阻和双电层电容,W1表示锂离子在固相正极材料内扩散Warbug阻抗,并将等效电路图所拟合的参数制成表1。


表 1 EIS 拟合数据表
表1直观的体现了R2,W1与温度的关系:电荷转移电阻R2随着温度的升高,先减小再增大,800℃烧结的样品具有最小的R2值,锂离子在材料中的扩散阻抗(W1)同样随着温度的升高,先减小再增大。这说明在800℃烧结的多孔Li3V2-(PO4)3/C材料最易发生电化学反应;与非多孔Li3V2(PO4)3/C材料相比,锂离子在800℃烧结的多孔Li3V2(PO4)3/C材料内部的脱/嵌最为容易。这进一步证实了均匀多孔Li3V2(PO4)3/C材料具有最佳的电化学性能。
3 结论
具有多孔结构的Li3V2(PO4)3/C材料可以由Li2CO3、NH4-H2PO4、V2O5、草酸及淀粉为原料采用高温固相法成功合成。当烧结温度为800℃时,Li3V2(PO4)3/C材料不仅具有纯相单斜结构,而且在3~4.3 V范围内,较其他温度烧结的样品表现出最优的电化学性能,具有最优的放电比容量和倍率性能。在0.1 C倍率下首次放电比容量为130.0mAh/g,经20次循环后,仍有124.9mAh/g。2 C倍率下经50次循环后放电比容量为85.1mAh/g保持率为93.0%。因此,800℃下烧结的多孔Li3V2(PO4)3/C材料是一种很有潜力的动力锂离子电池正极材料。
[1]SAÏDIMY,BARKER J,HUANGH,etal.Performance characteristicsof lithium vanadium phosphate asa cathodematerial for lithium ion batteries[J].JPower Sources,2003,119-121:266-2721.
[2]BARKER J,GOVER R K B,BURNSP,etal.The effectof A l substitution on the electrochem ical insertion propertiesof lithium vanadium phosphate,Li3V2(PO4)3[J].Journalof the Electrochemical Society,2007,154(4):A 307-A 3131.
[3]MORGAN D,CEDERG,SAÏDIMY,etal.Experimental and com putational study of the structure and electrochem ical properties of LixM2(PO4)3compounds w ith themonoclinic and rhombohedral[J].Chemistry ofMaterials,2002,14(11):4684-4693.
[4]JIANG T,WANG C Z,CHEN G,etal.Effectsof synthetic route on the structural,physical and electrochem ical propertiesof Li3V2(PO4)3cathodematerials[J].Solid State Ionics,2009,180(9/10):708-714.
[5]SAÏDIMY,BARKER J,HUANG H,et al.Electrochem ical properties of lithium vanadium phosphate as a cathode material for lithium-ion batteries[J].Electrochemical and Solid-State Letters,2002,5(7):A 149-A 151.
[6]WANG JW,LIU J,YANGG L,etal.Electrochemicalperformance of Li3V2(PO4)3/C cathodematerial using a novel carbon source[J].Electrochim ica Acta,2009,54(26):6451-6454.
[7]CHEN Y H,ZHAO Y M,AN X N,et al.Preparation and electrochem ical performance studies on Cr-doped Li3V2(PO4)3as cathode materials for lithium-ion batteries[J].Electrochim ica Acta,2009,54(25):5844-5850.
[8]LIY Z,ZHOU Z,REN MM,etal.Electrochem ical performance of nanocrystalline Li3V2(PO4)3/carbon composite material synthesized by a novel sol-gelmethod[J].Electrochimica Acta,2006,51(28):6498-6502.
[9]GABERSCEK M,DOMINKO R,BELE M,et al.Monodisperse Porous,carbon-decorated LiFePO4prepared by sol-gelmethod based on citric acid[J].Solid State Ionics,2005,176(19/22):1801-1805.
[10]FAN X Y,LIY,WANG J J,et al.synthesis and electrochem ical performance of porous Li2FeSiO4/C cathode material for long-life lithium-ion batteries[J].Journal of Alloys and Compounds,2010,493(1/2):77-80.
[11]SAÏDIMY,BARKER J,HUANG H,et al.Performance characteristics of lithium vanadium phosphate asa cathodematerial for lithium-ion batteries[J].JPower Sources,2003,119-121:266-272.
[12]刘素琴,李世彩,唐联兴,等.Li3V2(PO4)3的溶胶-凝胶法合成及其性能研究[J].无机化学学报,2006,22(4):645-650.
[13]刘素琴,唐联兴,黄可龙.碳热还原法合成正极材料Li3V2(PO4)3及其性能[J].电源技术,2006,30(6):473-476.
[14]ZHENG JC,LIX H,WANG Z X,et al.Li3V2(PO4)3cathode material synthesized by chemical reduction and lithiation method[J].Journalof Power Sources,2009,189(1):476-479.
[15]DOMINKOR,GOUPIL JM,BELEM,etal.Impactof LiFePO4/C composites porosity on their electrochem ical performance[J].Journalof the Electrochem ical Society,2005,152(5):A 858-A 863.
[16]PRAKASH A S,MANIKANDAN P,RAMESHA K,et al.Solutioncombustion synthesized nanocrystalline Li4Ti5O12ashigh-rateperformance li-ion battery anode[J].Chem istry of Materials,2010,22(9):2857-2863.
[17]郭炳焜,徐徽,王先友,等.锂离子电池[M].长沙:中南大学出版社,2002.
