功能胶原蛋白生物材料与组织再生
2012-02-06韩倩倩王春仁戴建武鲁葵岳瑞齐黄经春
韩倩倩 王春仁 戴建武 鲁葵 岳瑞齐 黄经春
1 中国食品药品检定研究院(北京100050)
2 中国科学院遗传与发育生物学研究所(北京100190)
3 国家食品药品监督管理局济南医疗器械监督检验中心(济南 250101)
1.功能生物材料概述
1.1 生物材料
生物材料通常指以医疗为目的,单独或与药物一起,用于组织或器官的治疗或替代以修复受损组织的材料。使用生物材料的目的是为组织细胞生长提供三维支架,在对损伤部位进行填充、替换的同时,促进细胞的粘附、增殖乃至分化,所以除了符合一般生物医学材料的要求外,理想的生物材料还需满足以下要求:(1)良好的生物相容性;(2)可降解性及合适的降解速率;(3)合适的孔径结构;(4)合适的表面理化性质和良好的细胞界面关系;(5)与植入部位组织的力学性能相匹配的结构强度;(6)便于加工成理想的二维或三维结构,可获得所需的组织或器官形状[2]。
1.2 胶原生物材料
胶原蛋白是细胞外基质的主要成分,作为细胞生长的依附与支架,能诱导上皮细胞等的增殖和分化。胶原蛋白为生物体提供了机械支撑作用,维护器官与组织的完整性,保障其正常功能的行使[3]。胶原在创伤修复中有十分重要的作用,是参与创伤愈合的主要结构蛋白,所以,我们选择胶原作为修复组织损伤的支架材料。
胶原在医学上的应用包括许多方面,包括创面的愈合和烧伤的修复、整形,神经损伤再生,以及血管瓣膜替代等。表1 总结了胶原在医疗上的用途。

表1.胶原材料在医疗上的应用
2.功能胶原生物材料的研究
功能生物材料是指能主动对机体的理化或生理过程产生影响的生物活性材料,它能够诱导细胞的长入,使材料细胞化,从而使得损伤部位形成新的组织。在这种情况下,生物材料不只是起物理机械支持作用,它还能够通过改变周围环境而改变再生的过程。目前,活化材料的生物活性分子有几种:(1)促细胞粘附分子,促进细胞在材料上的生长和分化;(2)生长因子,促进细胞增殖、存活及控制细胞表型;(3)特异表达活性分子的DNA,可以达到长期稳定的作用效果。三方面的研究目前都有很大的进展,我们更为关注生长因子的独特功能。
2.1 生长因子与胶原复合构成生物材料

图1.生长因子与材料简单吸附的生物材料
生长因子是通过细胞间信号传递影响细胞活动的一类多肽因子,可由多种细胞分泌,与靶细胞表面的特异性受体结合来发挥其作用,有促进或抑制细胞的增殖、迁移和基因表达的作用,在生物体的发育与损伤修复过程中发挥重要的作用[4]。
目前,用生长因子来活化胶原材料,并与胶原材料联合用于损伤修复的例子已经有很多。然而,根据目前的研究,生长因子与生物材料简单的复合作用是有限的,这是因为体内体液的浸润与流动,造成了生长因子的自由扩散,从而不能达到局部富集的目的。如图1 所示。这种扩散会有几方面的问题,一是扩散的生长因子为机体带来潜在的风险,二是扩散使细胞活动主要发生在材料的外部,导致修复效果有限,而为了加强修复效果,需要反复用药,这无疑增加了成本与患者的痛苦[5]。
2.2 利用带胶原结合区的生长因子与胶原材料复合构成功能胶原生物材料
如果通过特定的方式,将生长因子锚定在胶原支架材料上,限制生长因子的自由扩散,就能使生长因子在材料的原位发挥作用,促进细胞在材料内的增殖、迁移、分化。如图2 所示。由此我们可以预测:一方面,移植到体内后,生长因子的自由扩散可以得到限制,削弱生长因子的自由扩散对机体的潜在风险;另一方面,可以大大降低生长因子使用量,降低治疗成本,达到高效率利用生长因子的目的;最重要的一点是可以提高修复治疗效率,使得再生能够比较均匀,从而提高修复后组织的质量[5]。
为了增强生长因子与胶原材料的结合能力,采用基因工程的方法,在生长因子上融合能够特异结合胶原的多肽TKKTLRT(胶原结合区CBD),从而赋予生长因子更强的特异结合胶原蛋白的能力。其中,胶原结合区CBD 衍生于胶原酶中胶原结合区的一段7 肽,序列为TKKTLRT,具有特异的胶原结合能力。
针对不同的损伤,可以制备不同的胶原材料。对适于这种组织损伤修复的生长因子进行改造,使之带有胶原结合能力。具有胶原特异结合能力的生长因子和不同的胶原材料,构成适于不同组织损伤修复的功能胶原生物材料,并且在皮肤、骨、肌肉(膀胱肌肉,腹壁肌肉)、外周神经和中枢神经损伤修复中验证了胶原功能生物材料的作用。
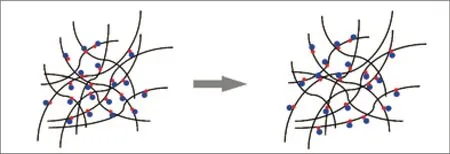
图 2.生长因子与材料定向结合的功能生物材料
3.胶原功能生物材料对不同组织损伤修复的作用
3.1 胶原功能生物材料在皮肤组织损伤修复中的作用
对于皮肤损伤修复,胶原膜(Collagen Membrane,CM)是一种合适的材料。胶原膜可以作为创面覆盖物,具有封闭创面、保湿、止血以及可吸收等特点(图3)。
选择PDGF-BB(血小板源性生长因子-BB)作为治疗皮肤损伤的活化因子。PDGF 参与了许多细胞活动,包括细胞增殖、细胞生长、迁移及细胞的生存凋亡等,对各种间充质及神经上皮来源的一些细胞是潜在的促分裂素。大量的动物实验表明,加入外源的PDGF 能够促进愈合过程。外源PDGF-BB 能够促进组织的新生、伤口的愈合,提高修复质量[6,7]。
对PDGF-BB 进行改造,将胶原结合区CBD融合入PDGF-BB 中,制备出带胶原结合区的PDGF-BB(称之为CBD-PDGF),同时也制备出天然形式的PDGF-BB,称之为NAT-PDGF。体外细胞实验的结果表明,NAT-PDGF 和CBD-PDGF具有相似的生物学活性,这说明胶原结合区CBD的融合,没有影响CBD-PDGF 的生物学活性[7]。体外胶原结合实验的结果显示,CBD-PDGF 具有特异结合胶原蛋白的能力,其胶原结合能力显著性优于NAT-BDNF[7]。
随后,用动物模型检验由胶原膜结合CBDPDGF 构成的功能胶原生物材料。采用的皮肤损伤模型是兔耳溃疡模型。共分为3 组:PBS 浸泡的胶原膜组(CM/PBS),胶原膜吸附NAT-PDGF组(CM/NAT-PDGF),胶原膜结合CBD-PDGF 组(CM/CBD-PDGF)。测量不同时间点,各个组的伤口愈合率,结果显示,由胶原膜结合CBD-PDGF构成的功能胶原生物材料组的愈合速度显著好于胶原膜吸附NAT-PDGF 组和对照组。手术后14 天,由胶原膜结合CBD-PDGF 构成的功能生物材料组的溃疡已经基本愈合。免疫组化观察血管新生和胶原沉积。血管新生将改变伤口处的血供,运输养分;而胶原沉积是皮肤愈合及重塑不可或缺的过程,胶原沉积的好坏往往反映了伤口愈合治疗的优劣。在这两个指标上,由胶原膜结合CBDPDGF 构成的功能胶原生物材料组也显著高于胶原膜吸附NAT-PDGF 组与对照组,显示了其在促进损伤修复,提高修复质量上的巨大作用[7]。

图3.胶原膜(CM)的结构(A)胶原膜(CM)的直观图(B)胶原膜(CM)电镜图

图4.DBM的结构(A)DBM直观图;(B)DBM电镜图。
3.2 胶原功能生物材料在骨组织损伤修复中的作用
选择脱钙骨基质(Demineral bone matrix,DBM)即骨胶原作为促进骨损伤修复的支架材料(图4)。DBM 保持了天然骨的小梁结构与有机成分(骨的主要成分),DBM 的胶原结构表面含有矿物沉积的位点,对矿物沉积有诱导作用,可有效引发和控制矿化过程,促进骨形成,因而是很好的骨填充材料[5,8]。
研究的另外一个方面是选择活化DBM 的因子,研究人员选择了骨形态发生蛋白-2(BMP-2)作为诱导骨形成的活性分子。同样,通过基因工程的方法在BMP-2 一端耦联CBD,制备出与胶原蛋白具有特异结合能力的CBD-BMP-2。且制备出天然的BMP-2(NAT-BMP-2)。体外细胞实验验证了NAT-BMP-2 与CBD-BMP-2 的生物学活性没有明显的差别,体外胶原结合实验的结果表明CBD-BMP-2 具有良好的胶原结合能力[5]。
为了研究这种功能胶原生物材料对原位骨缺损的修复作用,采用兔下颌骨缺损模型,即在兔的下颌骨部位制造一个自身无法修复的12mm×5mm×4mm 的缺损。随后用3 组不同材料填充,或不填充作为对照,即总共分为4 个组:不填充材料的空白组,填充PBS 浸泡的DBM 作为对照组(DBM/PBS),以及 DBM 吸附NAT-BMP-2组(DBM/NAT-BMP-2),DBM 结合CBD-BMP-2组(DBM/CBD-BMP-2)。对不同组的愈合情况进行X 光检查,通过侧面的X 光成像来分析伤口的愈合情况。结果表明由DBM 结合CBD-BMP-2 构成的功能胶原生物材料(DBM/CBD-BMP-2)显著加速了骨修复的能力,不仅外周成骨比较成熟,而且材料的内部的成骨作用也非常明显[5]。
3.3 功能胶原生物材料在肌肉组织损伤修复中的作用
3.3.1 膀胱肌肉损伤修复
用胶原膜CM 作为促进膀胱肌肉损伤修复的支架材料。选择人碱性成纤维生长因子bFGF 作为活化材料的因子。bFGF 是促进膀胱损伤后组织再生的重要因子。对bFGF 进行改造,将胶原结合区CBD 融合入bFGF 蛋白中,制备出能与胶原蛋白特异结合的CBD-bFGF,同时也制备出天然形式的bFGF(NAT-bFGF)。在大鼠膀胱肌肉损伤模型中,检验了由胶原膜结合CBD-bFGF构成的功能胶原生物材料的作用。共分为4 组:假手术组(sham-operated group);PBS 浸泡过的胶原膜组(CM/PBS);胶原膜吸附NAT-bFGF 组(CM/NAT-bFGF);胶原膜结合CBD-bFGF 组(CM/CBD-bFGF)[9]。
修复过程中的30 天和90 天两个时间点,H&E 染色观察各组损伤修复的直观情况。结果表明,由胶原膜结合CBD-bFGF 构成的功能胶原生物材料组的材料植入处细胞化明显高于其他治疗组,且90 天时,其损伤部位再生组织的形态与正常组织相似。损伤处平滑肌细胞的免疫组化染色结果也表明,由功能胶原生物材料组材料植入处平滑肌细胞的阳性率显著高于其他治疗组,说明它能够促进损伤部位肌肉损伤的修复。接着,进行尿动力学检测,观察各组膀胱功能的恢复情况。结果表明,功能胶原生物材料组的膀胱顺应性,即膀胱肌肉的弹性性能明显高于其他组,这说明由胶原膜结合CBD-bFGF 构成的功能胶原生物材料,显著促进了受损膀胱肌肉再生及膀胱功能的恢复[9]。
3.3.2 腹壁肌肉损伤修复
采用大鼠腹壁肌肉缺损模型检验了对膀胱肌肉损伤修复有效果的胶原膜结合CBD-bFGF 构成的功能胶原生物材料。腹壁肌肉缺损处用材料覆盖,共分为四组:经PBS 浸泡的胶原膜组(CM/PBS);胶原膜结合吸附NAT-BDNF 组(CM/NAT-BDNF);胶原膜结合CBD-BDNF 组(CM/CBD-BDNF);假手术组(sham)。恢复90 天后,腹壁损伤处H&E 染色和平滑肌细胞免疫组化染色的结果表明,collagen/CBD-bFGF 组损伤处平滑肌细胞阳性率显著高于其他治疗组。说明,这种由胶原膜结合CBD-bFGF 构成的功能胶原生物材料促进了腹壁肌肉缺损处的肌肉再生[10]。观察再生的腹壁肌肉组织的机械性能以评价再生腹壁肌肉组织的功能恢复,测定了再生腹壁肌肉的机械抗拉力性能。结果表明,collagen/CBD-bFGF组的最大弹性性能显著好于其他治疗组,说明由胶原膜结合CBD-bFGF 构成的功能胶原生物材料促进了再生肌肉的功能恢复[10]。
3.4 胶原功能生物材料在外周神经损伤修复中的作用
对于外周神经损伤的修复,选用胶原膜CM作为支架材料。同时,选用神经营养因子(NGF)作为活化胶原膜,促进外周神经再生的因子。NGF 的生物学效应广泛,主要通过促进神经细胞树状突发生、伸展和维持存活的作用,增加神经纤维在支配靶区的密度,并且促进神经细胞的分化,加快有丝分裂,使神经细胞数目增加,决定轴突的生长方向[11]。
对NGF 进行改造,使之带有胶原结合区CBD,制备出能与胶原特异结合的NGF(CBDNGF),同时制备出天然的NGF(NAT-NGF)。体外细胞活性实验表明CBD-NGF 和NAT-NGF 都具有神经营养活性,促使pc12 细胞生长出轴突。胶原结合实验也表明,CBD-NGF 具有特异的胶原结合能力。采用大鼠皮下包埋实验观察由胶原膜结合CBD-BDNF 构成的功能胶原生物材料促进外周神经再生的效果。共分为三组:PBS 浸泡胶原膜的对照组;胶原膜吸附NAT-NGF 组;胶原膜结合CBD-NGF 组。这三个组之间的神经纤维数目都具有显著性差异。其中由胶原膜结合CBD-NGF 构成的功能胶原生物材料组的神经纤维数目要明显高于另外两组。可以得出结论,由胶原膜结合CBD-NGF 构成的功能胶原生物材料能够有效促进外周神经再生[11]。
3.5 胶原功能生物材料在中枢神经损伤修复中的作用
脊髓损伤(spinal cord injury,SCI)是一类致残率很高的中枢神经损伤。其中比较严重的是脊髓断裂损伤,其损伤部位神经丝断开连接,受损脊髓组织甚至出现缺损。断裂伤后神经再生面临的障碍有:(1)损伤处缺乏促进轴突生长的因子;(2)轴突生长缺乏方向性,难以实现正确的突触连接,神经功能很难恢复。针对这些问题,需要设计一个综合的治疗策略,克服再生障碍。(1)要选择一种良好的神经生长引导材料;(2)对材料进行修饰,使之带有活性成分,促进轴突生长。
良好的轴突生长引导材料可以引导受损轴突的生长方向,使之形成正确的突触联接,促进神经功能恢复。采用有序胶原生物材料LOCS(图5)[12]。其次,选择脑源性神经营养因子(BDNF)作为活化LOCS,促进神经再生的因子。BDNF 能够促进神经元的存活与分化,常被用来治疗中枢神经损伤,包括帕金森症、抑郁症及脊髓损伤[13]。研究人员对BDNF 进行改造,将胶原蛋白结合区CBD 融合入BDNF 蛋白,制备出能与胶原材料特异结合的BDNF(CBD-BDNF),同时,还制备出天然形式的BDNF(NAT-BDNF)[12]。

图5.有序胶原材料LOCS的宏观照片(a)-(c)及电镜照片(d)
采用大鼠脊髓半横断损伤模型检验了由LOCS 结合CBD-BDNF 构成的功能胶原生物材料的作用。大鼠脊髓做6mm 长半横断损伤,材料纵向植入脊髓缺损处,分为四组:对照组,不植入材料;LOCS 组;LOCS 吸附NAT-BDNF 组;LOCS 结合CBD-BDNF 组。
BBB 行为学评分结果表明,LOCS 结合CBDBDNF 组的运动能力恢复显著好于其他组。免疫组化观察材料植入部位的神经再生情况:神经丝NF 染色结果表明,LOCS 结合CBD-BDNF 组的神经丝阳性率显著高于其他组,且轴突再生方向与其他组比较有更好的有序性。说明LOCS 结合CBD-BDNF 所构成的功能胶原生物材料不但能促进神经再生,而且能引导轴突沿LOCS 的方向有序生长,显著促进了脊髓损伤大鼠的运动能力恢复。
4.结论
针对不同的组织损伤,可以选用不同的胶原材料作为促进再生的支架材料:胶原膜CM 适用于皮肤、肌肉、外周神经的损伤修复;脱钙骨胶原DBM 适用于骨组织修复;有序胶原材料LOCS 适用于脊髓中枢神经损伤的修复。同时,用带胶原结合区的生长因子来活化胶原材料,构成功能胶原生物材料,促进不同组织损伤的再生:CBD-PDGF 用于活化胶原膜,促进皮肤损伤再生;CBD-BMP-2 用于活化脱钙骨胶原DBM,促进骨损伤修复;CBD-bFGF 用于活化胶原膜,促进肌肉损伤修复;CBD-NGF 用来活化胶原膜,用于外周神经损伤修复;CBD-BDNF 用来活化有序胶原材料LOCS,用于脊髓中枢神经损伤修复。采用不同的组织损伤大鼠模型检验了这些胶原功能生物材料促进相关组织损伤修复的作用。结果表明,通过限制生长因子在生物材料上的扩散可以有效提高生物材料引导组织再生的能力。
[1]Peppas NA,Langer R(1994)New challenges in biomaterials.Science 263:1715-1720.
[2]Langer R,Vacanti JP(1993)Tissue engineering.Science 260:920-926.
[3]Gelse K,Poschl E,Aigner T(2003)Collagens--structure,function,and biosynthesis.Adv Drug Deliv Rev 55:1531-1546.
[4]Macri L,Silverstein D,Clark RA(2007)Growth factor binding to the pericellular matrix and its importance in tissue engineering.Adv Drug Deliv Rev 59:1366-1381.
[5]Chen B,Lin H,Wang J,Zhao Y,Wang B,et al.(2007)Homogeneous osteogenesis and bone regeneration by demineralized bone matrix loading with collagen-targeting bone morphogenetic protein-2.Biomaterials 28:1027-1035.
[6]Heldin CH,Westermark B(1999)Mechanism of action and in vivo role of platelet-derived growth factor.Physiol Rev 79:1283-1316.
[7]Lin H,Chen B,Sun W,Zhao W,Zhao Y,et al.(2006)The effect of collagen-targeting platelet-derived growth factor on cellularization and vascularization of collagen scaffolds.Biomaterials 27:5708-5714.
[8]Chakkalakal DA,Strates BS,Garvin KL,Novak JR,Fritz ED,et al.(2001)Demineralized bone matrix as a biological scaffold for bone repair.Tissue Eng 7:161-177.
[9]Chen W,Shi C,Yi S,Chen B,Zhang W,et al.Bladder regeneration by collagen scaffolds with collagen binding human basic fibroblast growth factor.J Urol 183:2432-2439.
[10]Shi C,Chen W,Zhao Y,Chen B,Xiao Z,et al.Regeneration of full-thickness abdominal wall defects in rats using collagen scaffolds loaded with collagen-binding basic fibroblast growth factor.Biomaterials.
[11]Sun W,Lin H,Chen B,Zhao W,Zhao Y,et al.(2007)Promotion of peripheral nerve growth by collagen scaffolds loaded with collagen-targeting human nerve growth factor-beta.J Biomed Mater Res A 83:1054-1061.
[12]Han Q,Sun W,Lin H,Zhao W,Gao Y,et al.(2009)Linear ordered collagen scaffolds loaded with collagen-binding brainderived neurotrophic factor improve the recovery of spinal cord injury in rats.Tissue Eng Part A 15:2927-2935.
[13]Sharma HS,Nyberg F,Westman J,Alm P,Gordh T,et al.(1998)Brain derived neurotrophic factor and insulin like growth factor-1 attenuate upregulation of nitric oxide synthase and cell injury following trauma to the spinal cord.An immunohistochemical study in the rat.Amino Acids 14:121-129.
