SiW11O39Fe(Ⅲ)(H2O)5-的电化学性质及电催化还原过氧化氢*
2012-01-24华英杰王崇太刘希龙吴春燕毛彦超刘晓旸
华英杰,王崇太,刘希龙,吴春燕,周 方,毛彦超,刘晓旸
(1.海南师范大学化学与化工学院,海南 海口 571158;2.中山大学化学与化工学院,广东 广州 510275;3.吉林大学无机合成与制备国家重点实验室,吉林 长春 130012)
Keggin型过渡金属取代杂多阴离子XM11O39MTr(H2O)n-[X=Si、Ge,P、As 等;M=Mo(Ⅵ)、W(Ⅵ)等;MTr=过渡金属离子;n=4~6]在几何结构保持不变的情况下,其化学结构如组成杂离子X、多金属离子M以及取代金属离子MTr可任意改变,因而可通过改变X、M和MTr来调节XM11O39MTr(H2O)n-的氧化还原性质,以满足不同场合的需要。XM11O39MTr(H2O)n-的这种多样性使它在光催化、电催化、电化学传感器、绿色合成、医药、环境治理和能源等领域潜在着广泛的应用前景,一直备受各国研究者的关注,成为研究的热点[1-12]。
最近,Wang等[5-8]研究了 Keggin 型 Fe(Ⅲ)-取代磷钨杂多阴离子PW11O39Fe(Ⅲ)(H2O)4-的电化学性质和电催化性能,并应用于水体生物难降解有机污染物邻苯二甲酸二甲酯和硝基苯的电催化降解,取得了较好的效果。为了考察杂离子X改变时多阴离子XM11O39MTr(H2O)n-电化学性质和电催化性能的变化,拟将PW11O39Fe(Ⅲ)(H2O)4-中的P(Ⅴ)置换为Si(Ⅳ),然后用循环伏安、交流阻抗等方法研究SiW11O39Fe(Ⅲ)(H2O)5-的电化学性质及其对 H2O2还原的电催化作用。虽然Anson等[13-14]曾报道 SiW11O39Fe(Ⅲ)(H2O)5-在NaClO4等介质中的循环伏安行为及其对H2O2、NO-2还原的电催化作用,但缺乏系统和详细,本文不仅弥补这个不足,而且与PW11O39Fe(Ⅲ)(H2O)4-进行比较,从而为XM11O39MTr(H2O)n-电催化剂的分子水平设计提供实验依据。
1 实验
1.1 试剂
钨酸钠 (Na2WO4·2H2O):SCRC国药集团化学试剂有限公司;硅酸钠 (Na2SiO3·9H2O)、丙酮、硝酸、硫酸氢钠、氢氧化钠、过氧化氢:广州化学试剂厂;硝酸铁:天津福晨化学试剂厂;以上所用试剂均为分析纯,实验用水为二次蒸馏水。Keggin型缺位硅钨杂多酸盐Na8SiW11O39和铁取代硅钨杂多酸盐Na5SiW11O39Fe(Ⅲ)(H2O)分别按参考文献 [15-16]合成,并进行红外光谱、紫外光谱和循环伏安表征。
1.2 仪器和方法
所有电化学测试均在CHI电化学工作站(660b,上海辰华)上进行,使用单室电解池,GC为工作电极 (~0.07 cm2),Pt丝为辅助电极,Ag/AgCl(3 mol·L-1KCl)为参比电极。每次测试前,工作电极均用0.05 μm的Al2O3进行抛光,并超声清洗2 min。溶液用N2气赶氧10 min。除非指明,实验均在298 K下进行。
2 结果与讨论
2.1 SiW11Fe的循环伏安行为
图1是SiW11Fe的循环伏安扫描结果,为了比较,图中附加了PW11Fe的扫描结果 (曲线b)。从图中可以看到,和PW11Fe一样,SiW11Fe的循环伏安行为也表现出3对还原氧化波,位于-0.218/-0.098 V处的还原氧化波归属于 Fe(Ⅲ)/Fe(Ⅱ)电对的还原氧化反应;而位于 -0.649/-0.575 V和 -0.762/- 0.715 V 处的两对还原氧化波则归属于W-O骨架的还原氧化反应[13-14]。与PW11Fe相比较,SiW11Fe的3对还原氧化波的峰电位明显负移,例如Fe波的还原峰电位从0.029 V负移至-0.218 V,负移了247m V;氧化峰电位则从0.102 V负移至-0.098 V,负移了200 mV。这是因为SiW11Fe的负电荷密度比PW11Fe高,能级位于PW11Fe之上,因而施加的电位要更负电子才能从阴极注入SiW11Fe,使之还原;相反,氧化时不用很正的电位就能使之氧化,因此还原和氧化电位都发生了负移,即SiW11Fe比PW11Fe难还原,但还原后比PW11Fe易氧化。此外,从图中我们还可以看到,对于SiW11Fe,除了还原氧化峰电位负移之外,其Fe波的还原 (阴极)峰电位EPc与氧化 (阳极)峰电位EPa的差值明显比PW11Fe的大,例如,SiW11Fe的是120 mV,PW11Fe的是73 mV,表明SiW11Fe的Fe(Ⅲ)/Fe(Ⅱ)电对传递电子的可逆性明显比PW11Fe的差,因为EPc与EPa的差值是检测能斯特反应的判据[17]。

图 1 1.0 mmol·L-1SiW11Fe(a)和 PW11Fe(b)在0.1 mol·L-1NaHSO4+Na2SO4(pH 2.5)溶液中的循环伏安曲线,扫描速度为20 mV·s-1Fig.1 Cyclic voltammogram of 0.1 mol·L -1NaHSO4+Na2SO4(pH 2.5)solution containing 1.0 mmol·L -1 SiW11Fe(a)and PW11Fe(b),scan rate:20 mV·s-1
SiW11Fe的E~I响应从方波伏安实验中也可以观察到,图2 是1.0 mmol·L-1SiW11Fe在0.1 mol·L-1NaHSO4+Na2SO4(pH 2.5)溶液中的方波伏安曲线。由图可见,有3个波分别出现在-0.188、 -0.629和 -0.760 V 处,恰好对应于上述循环伏安图中的3对还原氧化波。

图 2 1.0 mmol·L-1SiW11Fe 在 0.1 mol·L-1NaHSO4+Na2SO4(pH 2.5)溶液中的方波伏安曲线,ΔE=25 mV;f=15 HzFig.2 Square wave voltammogram of 0.1 mol·L-1 NaHSO4+Na2SO4(pH 2.5)solution containing 1.0 mmol·L-1SiW11Fe,ΔE=25mV;f=15 Hz
在对SiW11O8-39的电化学性质研究中我们观察到SiW11O8-39两对W-O骨架波的峰电位和峰电流与溶液的pH有很大关系,即随着溶液pH的增大,峰电位负移,峰电流降低。这是由于电极过程有H+离子参与 (式1、2)的缘故,显然,溶液pH的增加 (H+浓度降低)不利于反应的进行,故峰电位负移,峰电流降低。
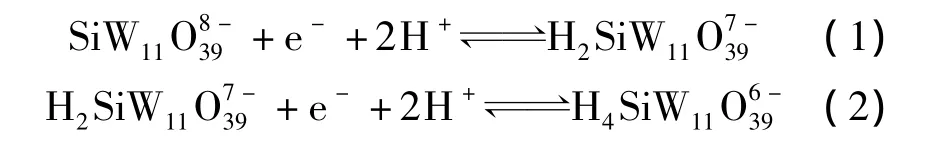

图3 1.0 mmol·L-1SiW11Fe在不同pH时的循环伏安曲线:(a)Fe(Ⅲ)/Fe(Ⅱ)波;(b)W-O骨架波支持电解质:0.1 mol·L-1NaHSO4+Na2SO4;扫描速度:10 mV·s-1Fig.3 Cyclic voltammograms of 1.0 mmol·L -1SiW11 Fe at different pH:(a)Fe(Ⅲ)/Fe(Ⅱ)wave;(b)W-O waves.Supporting electrolyte:0.1 mol·L -1NaHSO4+Na2SO4;scan rate:10 mV·s-1
当Fe(Ⅲ)接到SiW11O8-39的骨架形成SiW11Fe后,骨架波的这种性质依然保持,如图3(b)所示,当溶液的pH为4.31时,峰电流几乎为零。而对于Fe(Ⅲ)/Fe(Ⅱ)波,随着溶液pH的增大,峰电位也发生了负移 (图3a),这可能与下列的酸碱平衡有关[1]
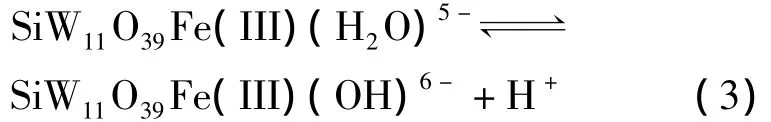
显然,SiPW11O39Fe(Ⅲ)(H2O)5-随着溶液pH的增加逐步转化为SiPW11O39Fe(Ⅲ)(OH)6-,而SiPW11O39Fe(Ⅲ)(OH)6-的负电荷密度比较大,能级位于SiPW11O39Fe(Ⅲ)(H2O)5-之上,因此Fe波还原氧化的峰电位负移。当pH>6.07时,Fe波的阴极峰电位和阳极峰电位拉得很宽 (峰电位差变大),这是因为当溶液的pH>6.0时,Fe(Ⅲ)的第六配位位置占据的全部是 OH-而不是H2O[13-14],因而电子传递的可逆性降低。
2.2 SiW11Fe对H2O2还原的电催化作用
前期的研究表明,PW11Fe对H2O2的还原具有显著的电催化作用[5],当其中的P(Ⅴ)用Si(Ⅳ)代替后,分子的几何结构并未改变,因而这种催化性质应被保持。为了证实这一点,我们进行了循环伏安实验,结果如图4所示。
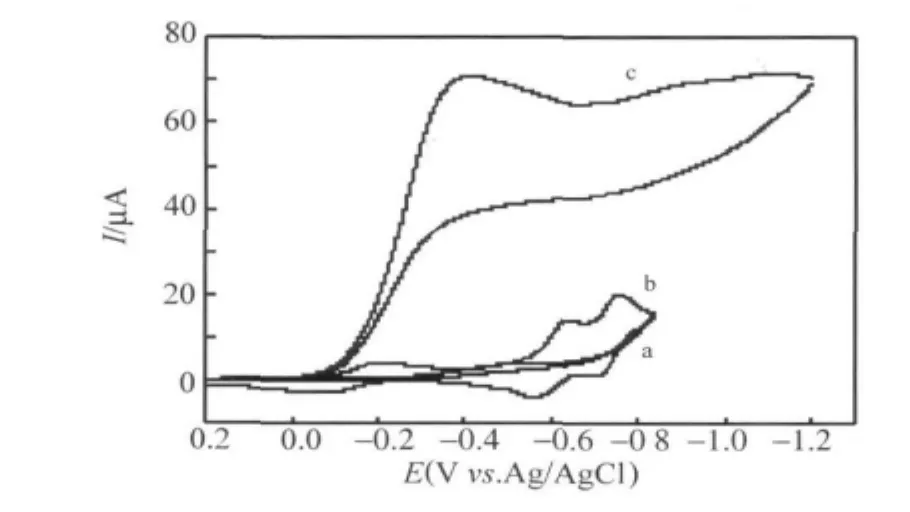
图4 SiW11Fe对H2O2还原的电催化作用:(a)底液+5 mmol·L-1H2O2;(b)底液 +1.0 mmol·L-1 SiW11Fe;(c)a+b底液:0.1 mol·L-1NaHSO4+Na2SO4(pH 2.5);扫描速度:20 mV·s-1Fig.4 Electrocatalysis of SiW11Fe towards H2O2reduction:(a)Background solution+5 mmol·L-1H2O2;(b)Background solution+1.0 mmol·L -1SiW11Fe;(c)a+b.Background solution:0.1 mol·L-1NaHSO4+Na2SO4(pH 2.5);scan rate:20 mV·s-1
由图4中可见,在SiW11Fe存在的情况下 (曲线c),H2O2还原的速率与它单独在电极上直接还原的速率 (曲线a)相比显著提高,表明SiW11Fe对H2O2的还原产生了间接电催化作用,这是SiW11Fe中的电对Fe(Ⅲ)/Fe(Ⅱ)发生可逆的还原氧化 (电子传递)所致 (曲线b)。因此,和PW11Fe一样,SiW11Fe对H2O2的还原也具有明显的电催化活性,只是催化电位更负。上述电催化过程用反应方程式表示为[6]
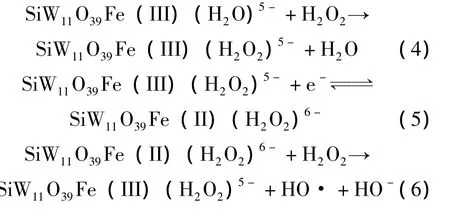
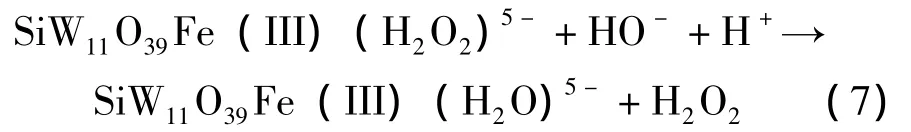
净反应为
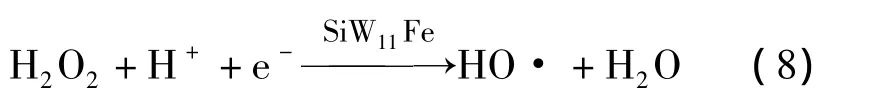
其中H2O2接受的电子并不是直接来自电极,而是来自SiW11Fe这一媒介,这就是SiW11Fe电催化作用的本质,因此,这类催化反应又称为媒介反应。显然,SiW11Fe传递电子的可逆性对于催化效率具有决定性的作用。
SiW11Fe对H2O2还原的间接电催化作用可以从电化学阻抗谱得到进一步理解。如图5所示,在没有H2O2存在的情况下,SiW11Fe的电化学阻抗谱 (EIS)由两部分组成 (曲线a),高频部分的半圆对应于电荷传递控制,低频部分的沃伯格直线对应于扩散控制,因此。在高频的情况下,Fe(Ⅲ)/Fe(Ⅱ)电对的电子传递受电荷传递阻力控制;而在低频的情况下则受扩散控制阻力控制。在H2O2存在的情况下,Fe(Ⅲ)/Fe(Ⅱ)电对的电子传递阻抗显著减小,由原来的13 750 Ω下降至3 475 Ω,表明SiW11Fe的催化作用是由于降低了电极反应活化能的缘故。
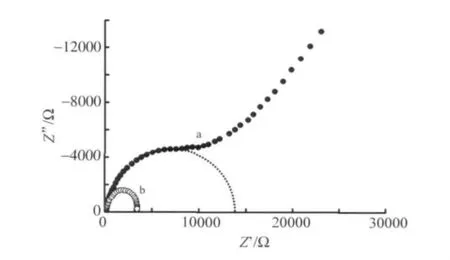
图5 1.0 mmol·L-1SiW11Fe溶液加入 H2O2前后的交流阻抗谱:(a)1.0 mmol·L-1SiW11Fe;(b)1.0 mmol·L-1 SiW11Fe+5 mmol·L -1H2O2 ΔE=5 mV;EP= -0.188 V;支持电解质:0.1 mol·L-1NaHSO4+Na2SO4(pH 2.5)Fig.5 EIS of 1.0 mmol·L -1SiW11Fe solution before and after addition of H2O2:(a)1.0 mmol·L-1SiW11Fe;(b)1.0 mmol·L -1SiW11Fe+5 mmol·L -1H2O2 ΔE=5 mV,EP= -0.188 V;supporting electrolyte:0.1 mol·L-1NaHSO4+Na2SO4(pH 2.5)
根据关系式 (9)[17-18]

估算加入H2O2前后Fe(Ⅲ)/Fe(Ⅱ)电对的交换电流密度分别为 1.9 ×10-6和 7.4 ×10-6A·cm-2。
2.3 H2O2浓度对催化反应速率的影响
图6显示了H2O2浓度对催化反应速率的影响。由图可见,催化峰电流随着H2O2浓度的增加而增大,直至H2O2浓度超过40 mmol·L-1以后,催化峰电流达到极限,因为此时H2O2使Fe(Ⅲ)在电极表面再生的速率达到了极限。
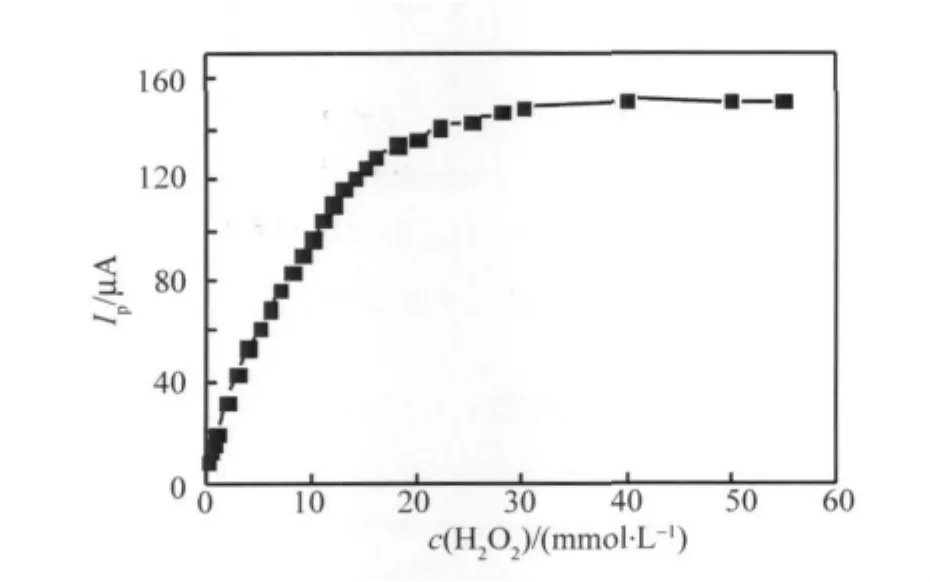
图6 H2O2浓度对催化峰电流的影响反应溶液 1.0 mmol·L-1SiW11Fe+0.1 mol·L-1 NaHSO4+Na2SO4(pH 2.5)Fig.6 Effect of the H2O2concentration on the catalyticpeak current The reaction solution:1.0 mmol·L-1 SiW11Fe+0.1 mol·L-1NaHSO4+Na2SO4(pH 2.5)
2.4 溶液pH对催化作用的影响
从上研究可知,溶液pH不仅影响SiW11Fe中W-O骨架波的还原氧化电位和电流,而且影响Fe(Ⅲ)/Fe(Ⅱ)电对的还原氧化电位和电子传递的可逆性,从而影响SiW11Fe电催化还原H2O2的效果,实验证实了这一点。如图7所示,随着溶液pH的增加,Fe波的催化峰电流明显减小。当pH>3.2时,Fe波的催化峰电流迅速下降,至pH=6.9时,该催化电流几乎为零,这是因为SiW11Fe此时以SiW11O39Fe(Ⅲ)(OH)6-的形式存在,导致Fe(Ⅲ)/Fe(Ⅱ)电对传递电子的可逆性降低,因而催化活性降低乃至消失。相反,SiW11Fe的第一个W-O骨架波却对H2O2的还原产生了电催化作用,而且在pH=4.3时效果最好,因为在这个pH下,正好能抑制Fe波的电催化作用,又能使骨架波可逆传递“单个电子”。W-O骨架波的间接电催化作用可用反应方程式表示如下
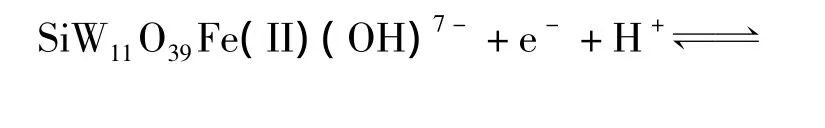


图 7 不同 pH 下 1.0 mmol·L-1SiW11Fe+5 mmol·L-1 H2O2溶液的线性扫描伏安曲线:(a)2.5;(b)3.2;(c)4.3;(d)5.5;(e)6.9扫描速率:20 mV·s-1;支持电解质:0.1 mol·L-1NaHSO4+Na2SO4Fig.7 LSV of 1.0 mmol·L -1SiW11Fe+5 mmol·L -1H2O2 solution at different pH of:(a)2.5;(b)3.2;(c)4.3;(d)5.5;(e)6.9 Scan rate:20 mV·s-1;supporting electrolyte:0.1 mol·L-1 NaHSO4+Na2SO4
W-O骨架波构成的催化循环与Fe波构成的催化循环区别在于,前者以“外球电子转移”的方式将电子传递给H2O2;后者则以“内球电子转移”的方式将电子传递给H2O2[6]。
3 结论
与PW11Fe类似,SiW11Fe在酸性溶液中也有3对还原氧化伏安响应,分别归属于 Fe(Ⅲ)/Fe(Ⅱ)电对和 W-O骨架的还原氧化反应。但SiW11Fe的3对还原氧化波的峰电位与PW11Fe相比明显负移,且均受溶液pH的影响。SiW11Fe中Fe(Ⅲ)/Fe(Ⅱ)电对传递电子的可逆性比PW11Fe的差,但同样对H2O2的还原具有明显的间接电催化作用,并受溶液pH的影响。随着溶液pH的增加,Fe波和W-O骨架波的还原氧化峰电位均负移,Fe波对H2O2还原的电催化活性降低甚至被完全抑制,相反,第一个W-O骨架波对H2O2的还原却有明显的电催化活性。
[1]RONG C Y,POPE M T.Lacunary polyoxometalate anions are .pi.-acceptor ligands.Characterization of some tungstoruthenate(Ⅱ,Ⅲ,Ⅳ,Ⅴ)heteropolyanions and their atom-transfer reactivity [J].J Am Chem Soc,1992,114(8):2932-2938.
[2]JORGENSEN K A.Transition-metal-catalyzed epoxidations[J].Chem Rev,1989,89(3):431 -458.
[3]JORGENSEN K A,SCHISTT B.Metallaoxetanes as intermediate in oxygen-transfer reactions-reality or fiction?[J].Chem Rev,1990,90(8):1483- 1506.
[4]Drago R S.Homogeneous metal-catalyzed oxidations by O2[J].Coord Chem Rev,1992,117(22):185 -213.
[5]WANG C T,HUA Y J,LI G R,et al.Indirect cathodic electrocatalytic degradation ofdimethylphthalate with PW11O39Fe(Ⅲ)(H2O)4-and H2O2in neutral aqueous medium[J].Electrochim Acta,2008,53(16):5100-5105.
[6]WANG C T,HUA Y J,TONG Y X.A novel electro-fenton-like system using PW11O39Fe(Ⅲ)(H2O)4-as an electrocatalyst for wastewater treatment[J].Electrochim Acta,2010,55(22):6755 -6760.
[7]HUA Y J,WANG C T,DUAN H,er al.Fabrication,characterization and electrocatalytic properties of a solid modified electrode based on PW11O39Fe(Ⅲ)(H2O)4-and chitosan [J].Electrochim Acta,2011,58:99 -104.
[8]华英杰,王崇太,童叶翔,等.Keggin型杂多阴离子PW11O39Fe(Ⅲ)(H2O)4-电催化降解硝基苯[J].化学学报,2009,67(23):2650-2654.
[9]王崇太,华英杰,李高仁,等.Cr(Ⅲ)-取代磷钨杂多配合物对4-甲基吡啶的电催化氧化作用[J].化学学报,2008,66(8):835-840.
[10]华英杰,王崇太,李天略,等.Keggin型铬取代杂多离子 PW11O39Cr(Ⅲ)(H2O)4-的电化学性质[J].中山大学学报:自然科学版,2011,50(3):68 -73.
[11]华英杰,茅舟,王崇太,等.缺位磷钨杂多阴离子PW11O397-电催化降解邻苯二甲酸二甲酯[J].中山大学学报:自然科学版,2011,50(5):71 -74.
[12]王崇太,华英杰,华淑艳,等.Keggin型铁取代杂多阴离子PW11O39Fe(Ⅲ)(H2O)4-光催化降解硝基苯[J].化学学报,2010,68(11):1037-1042.
[13]TOTH J E,ANSON F C.Electrocatalytic reduction of nitrite and nitric oxide to ammonia with iron-substituted polyoxotungstates[J].J Am Chem Soc,1989,111(7):2444-2451.
[14]TOTH J E,MELTON J D,CABELLI D,et al.Electrochemistry and redox chemistry of aquaferrotungstosilicate,H2OFe(Ⅲ)SiW11O5-39in the presence of hydrogen peroxide and hydroxyl[J].Inorg Chem,1990,29(10):1952-1957.
[15]BREVARD C,SCHIMPF R,TOURNé G,et al.Tungsten-183 NMR:A complete and unequivocal assignment of the tungsten-tungsten connectivities in heteropolytungstates via two-dimensional183W NMR techniques[J].J Am Chem Soc,1983,105(24):7059-7063.
[16]ZONNEVIJLLE F,TOURNÉ C M,TOURNÉ G F.Preparation and characterization of iron(Ⅲ)-and rhodium(Ⅲ)-containing heteropolytungstates.Identification of novel oxo-bridged iron(Ⅲ)dimmers [J].Inorg Chem,1982,21(7):2751-2757.
[17]A J巴德,L R福克纳.电化学方法原理及应用[M].北京:化学工业出版社,1986:253.
[18]王崇太,华英杰.简明电化学原理及其应用[M].海口:海南出版社,2008:91.
