更昔洛韦联合人免疫球蛋白治疗婴儿巨细胞病毒性肝炎22例疗效观察
2012-01-15熊克宫林彩文
熊克宫, 林彩文
更昔洛韦联合人免疫球蛋白治疗婴儿巨细胞病毒性肝炎22例疗效观察
熊克宫, 林彩文
目的 观察更昔洛韦(GCV)联合人免疫球蛋白(IVIG)治疗婴儿巨细胞病毒性肝炎的疗效及不良反应。方法 将临床诊断为婴儿巨细胞病毒性肝炎的85例患儿随机分成3组。GCV+IVIG组22例:常规保肝治疗基础上,加用GCV和IVIG;GCV组33例:常规保肝治疗基础上,加用GCV;对照组30例:常规保肝治疗;疗程均为28d,观察治疗前后肝功能、肾功能、血常规及肝脏大小等变化。结果 (1)3组患儿总胆红素(TBIL)、直接胆红素(DBIL)、丙氨酸转氨酶(ALT)、天门冬氨酸转氨酶(AST)、谷氨酰转肽酶(GGT)及肝脏大小治疗前后差异均有统计学意义(P<0.05);(2)3组患儿治疗后比较:对照组TBIL、DBIL、ALT、AST及GGT均高于GCV+IVIG组,除AST外亦均高于GCV组,差异有统计学意义(P<0.05)。但GCV+IVIG组、GCV组之间差异均无统计学意义(P>0.05),3组之间肝脏大小差异亦均无统计学意义(P>0.05);(3)GCV组患儿中性粒细胞减少发生率(33.3%)明显高于GCV+IVIG组、对照组(9.1%,1.0%)差异有统计学意义(P<0.05),3组血小板减少发生率差异无统计学意义(P>0.05),而3组均未发生血红蛋白(Hb)下降及肌酐(Cr)升高。结论 GCV治疗婴儿巨细胞病毒性肝炎疗效显著、安全,而联合IVIG不增加疗效。
肝炎; 更昔洛韦/治疗应用; 人免疫球蛋白/治疗应用; 巨细胞病毒感染; 婴儿
婴儿巨细胞病毒性肝炎是指在婴儿期发生,由人巨细胞病毒(human cytomegalo virus,HCMV)引起的以黄疸、肝脏肿大、肝功能损害为主要临床表现的肝脏疾病[1]。长期以来,对于婴儿巨细胞病毒性肝炎的治疗缺乏统一标准和完善的方案。本研究分析更昔洛韦(ganciclovir,GCV)联合人免疫球蛋白(human immunoglobulin,IVIG)治疗婴儿巨细胞病毒性肝炎的疗效及不良反应,探讨婴儿巨细胞病毒性肝炎的治疗方法。
1 资料与方法
1.1 临床资料 将2006-05/2011-05在福建医科大学附属传染病医院感染科住院临床诊断为婴儿巨细胞病毒性肝炎的85例患儿根据患儿家长意愿分为GCV+IVIG组、GCV组、对照组,GCV+IVIG组22例,其中男14例,女8例;年龄1~12个月。GCV组33例,其中男20例,女13例;年龄1~12个月。对照组30例,其中男18例,女12例;年龄1~12个月。3组患儿性别、年龄比较,差异无统计学意义(P>0.05),具有可比性。
1.2 诊断标准 诊断标准参照中华医学会儿科分会制定标准[2]。
1.3 纳入标准 (1)采用PCR法定量检测HCMV DNA载量均升高,且均为黄疸型或淤胆型肝炎,乙肝两对半及丙肝抗体均呈阴性者;(2)患儿家长签知情同意书。
1.4 排除标准 代谢性肝病、药物、中毒性肝炎和胆道闭锁等疾病患儿。
1.5 治疗方法 3组患儿均予复合辅酶、维生素C、茵栀黄等保肝治疗。在此基础上GCV+IVIG组加用GCV,每次5mg/kg,每隔12h静脉滴注1次,连用14d;给予IVIG每日1次,每次2.5g静脉滴注,连用5d。GCV组加用GCV,剂量及疗程同GCV+IVIG组;3组总疗程均为28d。
1.6 观察指标 每周复查肝功能:TBIL、DBIL、ALT、AST、GGT;治疗前后查肝脏B超。
1.7 统计学方法 应用SPSS 12.0统计软件包进行统计分析,计量资料采用t检验,组间比较采用方差分析,P<0.05为差异有统计学意义。
2 结果
2.1 3组患儿各项指标治疗前后比较 见表1。
表1 3组患儿各项指标治疗前后比较(±s)
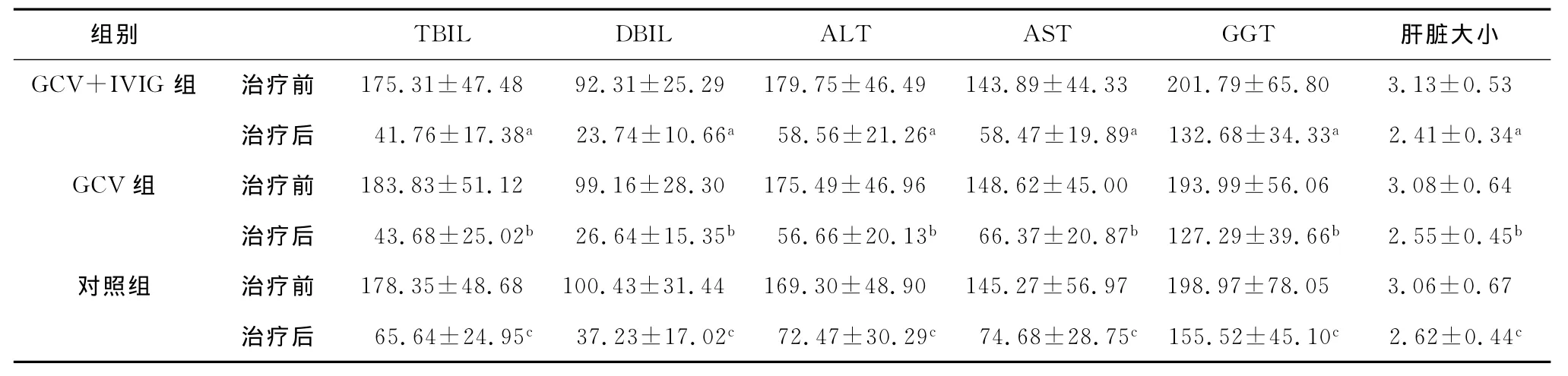
表1 3组患儿各项指标治疗前后比较(±s)
注:与治疗前比较,at=12.39、11.72、11.10、8.25、4.37、5.36,P<0.01;bt=14.15、12.94、13.36、9.94、5.65、3.91,P<0.01;ct=11.29、9.68、9.22、6.06、2.64、3.07,P<0.01。
肝脏大小GCV+IVIG组 治疗前 175.31±47.48 92.31±25.29 179.75±46.49 143.组别 TBIL DBIL ALT AST GGT 89±44.33 201.79±65.80 3.13±0.53治疗后 41.76±17.38a23.74±10.66a58.56±21.26a58.47±19.89a132.68±34.33a 2.41±0.34a GCV组 治疗前 183.83±51.12 99.16±28.30 175.49±46.96 148.62±45.00 193.99±56.06 3.08±0.64治疗后 43.68±25.02b 26.64±15.35b 56.66±20.13b 66.37±20.87b 127.29±39.66b 2.55±0.45b对照组 治疗前 178.35±48.68 100.43±31.44 169.30±48.90 145.27±56.97 198.97±78.05 3.06±0.67治疗后 65.64±24.95c 37.23±17.02c 72.47±30.29c 74.68±28.75c 155.52±45.10c 2.62±0.44c
表1结果显示,TBIL、DBIL、ALT、AST、GGT及肝脏大小差异均有统计学意义(P<0.05)。
2.2 3组患儿治疗后各项指标比较 GCV+IVIG组和GCV组TBIL、DBIL、ALT、GGT水平与对照组比较差异均有统计学意义,GCV+IVIG组AST水平与对照组比较差异有统计学意义(P<0.05),见表2。
表2 治疗后3组患儿各项指标比较(±s)

表2 治疗后3组患儿各项指标比较(±s)
肝脏大小GCV+IVIG 组 41.76±17.38 23.74±10.66 58.56±21.26 58.47±组别 TBIL DBIL ALT AST GGT 19.89 132.68±34.33 2.41±0.34 GCV 组 43.68±25.02 26.64±15.35 56.66±20.13 66.37±20.87 127.29±39.66 2.55±0.45对照组 65.64±24.95 37.23±17.02 72.47±30.29 74.68±28.75 155.52±45.10 2.62±0.44 F 4.743 4.149 3.668 3.391 4.153 0.280 P 0.011 0.019 0.030 0.038 0.019 0.757
2.3 3组患儿不良反应的比较 GCV+IVIG组、GCV组、对照组3组出现中性粒细胞减少分别为2例、11例和3例,GCV组明显高于GCV+IVIG组、对照组两组(χ2=7.439,P=0.024)。GCV+IVIG组、GCV组、对照组3组出现血小板减少分别为1例、5例和1例,3组之间差异均无统计学意义(P>0.05)。但中性粒细胞均未小于1.5×109/mL、血小板均未<50×109/mL,无特殊处理。所有患儿未发现血红蛋白下降、血清肌酐升高及神经系统症状。
3 讨论
CMV为疱疹病毒,自身有逆转录酶,能将RNA转变为DNA而得以繁殖,一旦侵入人体,不易被消灭,可长期甚至终生存在于体内。有文献报道[3],CMV是引起婴儿肝炎综合征最常见病原体,45.3%~85.5%婴儿肝炎综合征合并CMV感染,先天性婴儿巨细胞病毒性肝炎病死率高达20%。婴儿CMV感染临床表现较多,合并症较多,一般用药治疗效果不甚明显[4]。GCV是一种广谱抗DNA病毒药物,可通过双重作用来抑制病毒复制,不仅可竞争性抑制病毒DNA聚合酶,而且能直接渗入病毒DNA,终止病毒DNA链的延长,且GCV在感染细胞内的浓度为非感染细胞的100倍,因而对宿主正常细胞的毒性小[5]。目前,研究表明GCV在临床中治疗婴儿巨细胞病毒性肝炎是有效的[6],且少有发生严重不良反应[7]。本研究显示,GCV组患者肝功能指标及肝脏大小均有明显的改善,且肝功能指标较对照组改善更显著,提示GCV治疗婴儿巨细胞病毒性肝炎的疗效肯定。
IVIG含有大量的抗体,包括如腺病毒、柯萨奇病毒、CMV、流感病毒、麻疹及呼吸道合胞病毒等特异性抗体,能有效中和病毒抗原;还可封闭血液中的单核细胞、血小板或血管内皮细胞表面的fc受体,阻断异常免疫反应,减少CMV对机体的损害,提高机体对病毒的抵抗力。有研究表明,GCV联合IVIG可提高疗效及减少不良反应[8]。本研究显示,GCV+IVIG组患者肝功能指标及肝脏大小均有明显的改善,且肝功能指标较对照组改善显著,但与GCV组比较肝功能指标及肝脏大小均无差异,提示GCV加用IVIG不增加疗效,与上述研究不相符,分析原因可能为IVIG含有抗体可提高机体的特异性体液免疫,而不能增加抗CMV所依赖的特异性细胞免疫。且IVIG为血制品,可能给患儿带来潜在危险,增加治疗费用,故GCV不宜联合IVIG治疗婴儿巨细胞病毒性肝炎。
众所周知,GCV的主要副反应是骨髓抑制,即引起中性粒细胞和血小板减少,另极少数可出现血红蛋白下降及肌酐升高。本研究可以看出3组患儿在治疗过程中有少数病例出现中性粒细胞和血小板减少,GCV组出现中性粒细胞减少的现象明显高于GCV+IVIG组及对照组,3组血小板减少发生率在GCV组有升高趋势,但3组差异无统计学意义;治疗过程中中性粒细胞均未<1.5×109/mL及血小板均未<50×109/mL,无需特殊处理;3组均未出现血红蛋白下降及肌酐升高,提示IVIG可减少GCV在临床应用中出现骨髓抑制的发生率,其具体机制有待进一步研究。因此,GCV治婴儿疗巨细胞病毒性肝炎疗效显著、安全,而联合IVIG不增加疗效。
[1] Shibata Y,Kitajima N,Kawada J,et al.Association of cytomegalovirus with infantile hepatitis[J].Microbiol Immunol,2005,49(8):771-777.
[2] 中华医学会儿科学分会感染消化组.巨细胞病毒感染诊断方案[J].中华儿科杂志,1999,37(7):441.
[3] Griffiths PD,Walter S.Cytomegalovirus[J].Curr Opin Infect Dis,2005,18(3):241-245.
[4] Lombardi G,Stronati M.Congenital cytomegalovirus infection[J].Minerva Pediatr,2005,57(5):213-227.
[5] Halwachs-Baumann G.The congenital cytomegalovirus infection:virus-host interaction for defense and transmission[J].Curr Pharm Biotechnol,2006,7(4):303-312.
[6] Alarcón Allen A,Baquero-Artigao F.Review and guidelines on the prevention,diagnosis and treatment of post-natal cytomegalovirus infection[J].An Pediatr(Barc),2011,74(1):52.e1-52.e13.
[7] Tezer H,Secmeer G,Kara A,et al.Cytomegalovirus hepatitis and ganciclovir treatment in immunocompetent children[J].Turk J Pediatr,2008,50(3):228-234.
[8] 林少勇,王波,唐远平.更昔洛韦联合丙种球蛋白治疗婴儿巨细胞病毒性肝炎疗效观察[J].中华妇幼临床医学杂志(电子版),2010,06(3):182-184.
350021福州,福建医科大学附属传染病医院(福州市传染病医院)感染科
熊克宫(1982-),男,医师,医学硕士。研究方向:小儿感染性疾病的诊断与治疗,E-mail:510768115@qq.com。
林彩文,350021福州,福建医科大学附属传染病医院感染科。
10.3969/j.issn.1674-3865.2012.06.040
R512.6
B
1674-3865(2012)06-0563-03
2012-10-30)
张小冬)
临床研究
