磷灰石-硅灰石型生物玻璃粉体制备工艺的研究
2011-11-09彭文强徐旺生
杨 英,彭文强,徐旺生
(武汉工程大学化工与制药学院绿色化工过程省部共建教育部重点实验室,中国武汉430073)
磷灰石-硅灰石型生物玻璃粉体制备工艺的研究
杨 英,彭文强,徐旺生
(武汉工程大学化工与制药学院绿色化工过程省部共建教育部重点实验室,中国武汉430073)
采用溶胶-凝胶法制备磷灰石-硅灰石(AW)生物玻璃粉体,研究了加料方式、反应温度、pH对凝胶特性的影响。通过X射线衍射仪(XRD)、红外谱图分析(FT-IR)和扫描电镜(SEM)分析测试方法对产品的晶相组成及微观结构进行了分析。结果表明:凝胶形成的最佳工艺条件是加料方式为先让正硅酸乙酯乙醇溶液在硝酸催化作用下水解30 min后加入磷酸三乙酯,再以硝酸盐形式引入钙、镁元素,以氟化氢铵形式引入氟元素;反应温度为25℃;pH为1~2。烧结后的样品中主晶相为磷灰石和硅灰石,且颗粒大小均匀,形状规整,无明显团聚现象,孔结构规整,孔隙率为35%~40%。
磷灰石;硅灰石;生物活性
生物活性玻璃首先由L.L.Hench等[1]提出,这种材料在植入到体内后会与周围组织发生反应,使植入体与组织间形成生物结合,它因其致密的晶体结构,较低的溶解度,无毒副作用,与生物组织具有良好的相容性等特点而受青睐[2-3]。其中T.Kokubo等[4]用熔融法制备的磷灰石-硅灰石(AW)生物活性玻璃不仅具有良好骨诱导性和生物降解性,而且其机械性能非常出色,其表面弹性模量及断裂韧性都能与人体骨很好匹配,在生理环境下抵抗老化和疲劳性能也非常好,非常适合作为人体承重骨的替代和修复[5]。AW生物活性玻璃为CaO-MgOSiO2-P2O5-CaF2系统,磷灰石和硅灰石晶体质量分数分别为38%和34%,呈谷粒状均匀分布在玻璃基质中[6]。传统制备AW生物玻璃的方法为熔融法[7],但该法所需温度较高,容易引入杂质,且产品的化学成分均匀性较差[8]。而溶胶-凝胶法[9]具有条件易控制,能准确控制掺杂量,烧结温度低,避免坩埚污染,产品化学成分均一等优点[10]。笔者采用新型的溶胶-凝胶法制备AW生物活性玻璃粉体。
1 实验部分
1.1 实验原料、组成与仪器
本研究以CaO-MgO-SiO2-P2O5-CaF2系统生物玻璃粉体作为研究对象,其组成设计为: w(MgO)=4.6%,w(CaO)=44.9%,w(SiO2)= 34.2%,w(P2O5)=16.3%,w(CaF2)=0.5%[11]。
原料:正硅酸乙酯(TEOS)、磷酸三乙酯(TEP)、五氧化二磷、四水硝酸钙、无水氯化钙、六水硝酸镁、六水氯化镁、氟化铵、氟化氢铵、硝酸,均为分析纯;所用水为去离子水。
仪器:SHZ-D(Ⅲ)循环水式真空泵;501型超级恒温器;JJ-1增力电动搅拌器;ZK-82A型真空干燥器;SX-2.5-10箱式电阻炉;XD-5A型粉晶X射线衍射仪(XRD);JSM-5510LV型扫描电镜(SEM);Impact 420型傅里叶变换红外光谱仪(FTIR)。
1.2 实验步骤
将正硅酸乙酯溶于乙醇后缓慢加入含少量硝酸的水溶液中,TEOS、乙醇与蒸馏水的物质的量比为1∶4∶8,水解30 min后,加入磷源,混合搅拌20 min后形成磷硅酸盐网络结构,再加入含Ca、Mg和F的醇盐溶液,继续水解缩聚3 h后形成溶胶,溶胶在60℃下陈化3 h后形成整体凝胶,Ca2+、Mg2+在凝胶中主要存在于Si—O四面体之间。凝胶用蒸馏水洗涤后放入120℃烘箱内干燥12 h,干燥后得到均匀、分散干凝胶粉,将干凝胶粉在马弗炉中升温至800℃后保温1 h,得到前驱体粉末,让其随炉冷却后再升温至1 150℃保温4 h后随炉冷却,最终得到生物玻璃粉体。
2 结果与讨论
2.1 原料选择对凝胶特性的影响
原料的选择及加料方式对凝胶的性质有较大的影响,表1列举了不同原料及加料方式。由表1可知,以P2O5为磷源时,水解速率太快,直接形成白色沉淀,无法得到凝胶;以氯化盐形式引入Ca、Mg元素时,Cl-在后续过程中无法除去,使煅烧后的产品呈灰色;在引入F元素时,由于NH4HF2酸性较NH4F强,能加速水解反应的进行,从而缩短凝胶形成时间;TEOS水解速率最慢,所以最佳的加料方式为:先让TEOS乙醇溶液在HNO3催化作用下水解30 min后加入TEP,再以硝酸盐形式引入Ca、Mg元素,以NH4HF2形式引入F元素。

表1 原料选择对凝胶特性的影响
2.2 反应温度对凝胶特性的影响
采用最佳原料及加料顺序,考察反应温度对凝胶特性的影响,结果如表2所示。由表2可知,随着反应温度的升高,凝胶形成的时间缩短,凝胶的质量变差。由于正硅酸乙酯水解活性较低,当体系温度太低时,水解反应进行十分缓慢,胶凝时间太长;而体系温度升高后,体系中分子平均动能增加,分子运动速率提高,提高了分子间碰撞的几率,更多的分子成为活化分子,从而提高了正硅酸乙酯分子的水解活性,促进水解反应的进行,最终使体系的胶凝时间缩短;但随温度升高,溶剂挥发加快,醇盐不能完全溶解,水解反应进行不充分,从而形成的凝胶不稳定,降低了凝胶质量,因此该实验的最佳反应温度为25℃。

表2 反应温度对凝胶特性的影响
2.3 pH对凝胶特性的影响
采用最佳原料及加料方式,反应温度为25℃,分别讨论加入氨水、不加外来电解质、加入HNO3调节反应体系pH对凝胶的影响,结果如表3所示。由表3可知,当体系呈碱性时,难以形成凝胶;呈中性时形成凝胶质量较好,但凝胶形成时间较长;以HNO3调节体系pH为1~2时可在短时间内形成均匀、清澈的凝胶。这是因为用酸催化时,醇盐水解由H3O+的亲电机理引起,水解速度快,但随水解进行,醇盐水解活性因其分子上—OR基团数量减少而下降,因而很难形成Si(OH)4,其缩聚反应在完全水解前,即Si(OR)4完全转变为Si(OH)4前已开始,因而缩聚反应速率远大于水解反应速率,形成凝胶时间短;而用碱催化时,水解由—OH的亲核取代引起,水解速率大于缩聚反应速率,颗粒聚集较酸催化慢,因而碱催化时凝胶形成时间长。

表3 pH对凝胶特性的影响
2.4 XRD谱图分析
干凝胶粉在800℃下预煅烧后得到的前驱体粉末的X射线衍射谱图如图1所示,由图1可看出,预煅烧后前驱体粉末为非晶态结构,无明显晶体峰值出现,且稳定性较好。
图2为前驱体粉末在1 150℃下煅烧4 h的XRD谱图,由图2可知,样品晶化较好,峰形尖锐,将该谱图与标准JCPDF卡片对照后,确定主晶相为磷灰石和硅灰石,并有少量二氧化硅晶相。

2.5 红外谱图分析
烧结后AW玻璃粉体的FT-IR谱图如图3所示。在图3中,3 448.23 cm-1处为—OH的特征振动峰;1 074.62 cm-1、1 020.20 cm-1处为PO34-的非对称伸缩振动峰;977.43 cm-1处为PO34-对称伸缩振动峰,从而可确定组成中存在羟基磷灰石形式的磷灰石。在850~1 100 cm-1强吸收范围内出现6个吸收带,1 074.62 cm-1和1 020.20 cm-1吸收带是由Si—O—Si非对称伸缩振动引起,977.43 cm-1吸收带是由O—Si—O(非桥氧)对称伸缩振动引起,938.60 cm-1和 902.57 cm-1吸收带是由O—Si—O(非桥氧)非对称伸缩振动产生的(此吸收带与磷灰石吸收带部分重合);在600~750 cm-1范围内出现由 Si—O—Si对称伸缩振动引起的690.40 cm-1和 644.12 cm-1两个吸收带;300~600 cm-1弱吸收区内有3个吸收带,547.69 cm-1和512.98 cm-1吸收带是Si—O(非桥氧)弯曲振动吸收的结果,455.12 cm-1吸收带是由Ca—O伸缩振动产生的。由上述FT-IR分析结果进一步确认所制备的生物活性玻璃粉体主晶相为磷灰石和硅灰石。
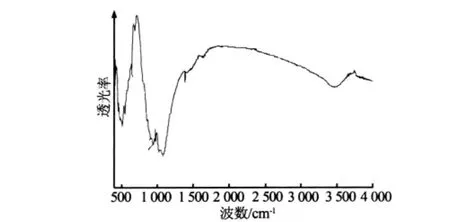
图3 生物玻璃粉末FT-IR谱图
2.6 SEM照片
图4为玻璃粉体的扫描电镜照片,从图4可看出产品颗粒大小比较均匀,无明显团聚现象,晶粒形状规整,有丰富的大孔及微孔结构,便于组织、生长因子等长入。

图4 生物玻璃粉末SEM图
3 结论
1)采用溶胶-凝胶法制备出化学性能稳定的前驱体粉末,确定出凝胶的优化工艺条件:加料方式为先让TEOS乙醇溶液在HNO3催化作用下水解30 min后加入TEP,再以硝酸盐形式引入Ca、Mg元素,以NH4HF2形式引入F元素,反应温度为25℃,pH为1~2。2)前驱体粉末在800℃下预煅烧后再经1 150℃烧结可制备出以磷灰石和硅灰石为主晶相的生物玻璃粉体材料。3)所制得的生物玻璃粉体颗粒大小均匀,形状规整,无明显团聚现象,孔结构规整,孔隙率为35%~40%。
[1]Hench L L,Splinter R J,Allen W C,et al.Bonding mechanisms at the interface of ceramic prosthetic materials[J].J.Biomed.Mater. Res.,1971,2(1):117-141.
[2]苗鸿雁,孙正球,谈国强.溶胶-凝胶法制备生物微晶玻璃的研究进展[J].材料导报,2006,20(1):54-56.
[3]Chen Q Z,Rezwan K,Boccaccini A R,et al.The surface functionalization of 45S5 Bioglass-based glass ceramic scaffolds and its impact on bioactivity[J].J.Mater.Sci.-Mater.Med.,2006,17(11):979-987.
[4]Kokubo T,Shigematsu M,Ito S,et al.Fatigue and life-time of bioactive glass-ceramic A-W containing apatite and wollastonite[J].Journal of Materials Science,1987,22(11):4067-4070.
[5]Singh R K,Srinivasan A,Kothiyal G P.Evaluation of CaOSiO2-P2O5-Na2O-Fe2O3bioglass-ceramics for hyperthermia application[J].J.Mater.Sci.-Mater.Med.,2009,20(1): 147-151.
[6]Saravanapavan P,Jones J R,Pryce R S,et al.Bioactivity of gelglass powders in the CaO-SiO2system:acomparison with ternary (CaO-P2O5-SiO2)and quaternary glasses(SiO2-CaOP2O5-Na2O)[J].J.Biomed.Mater.Res.A,2003,66(1):110-119.
[7]Yoshihara S,Kokubo T,Nishimura N,et al.Effects of glass composition on compressive strength of bioactive cement based on CaOSiO2-P2O5glass powders[J].Journal of Materials Science,1994,5(3):123-129.
[8]杨为中,周大利,尹光福,等.溶胶-凝胶法制备AW生物活性玻璃陶瓷的研究[J].硅酸盐学报,2004,32(2):171-176.
[9]Abiraman S,Varma H K,Kumari T V,et al.Preliminary in vitro characterization of a sol-gel derived bioactive glass-ceramic system[J].Bull.Mater.Sci.,2002,25(5):419-429.
[10]薛明,冯丹歌,李大光,等.有机泡沫浸渍法制备多孔磷灰石-硅灰石(AW)生物活性玻璃陶瓷研究[J].无机化学学报,2007,23(4):708-709.
[11]Kokubo T,Ito S,Huang Z T,et al.Ca,P-rich layer formed on high-strength bioactive glass-ceramic A-W[J].Journal of Biomedical Materials Research,1990,24(3):331-343.
Study on preparation technology of apatite-wollastonite bioactive glass powder
Yang Ying,Peng Wenqiang,Xu Wangsheng
(Key Laboratory for Green Chemical Process of Ministry of Education,School of Chemical Engineering&Pharmacy,Wuhan Institute of Technology,Wuhan 430073,China)
Apatite-wollastonite(AW)bioactive glass powder was prepared by sol-gel process.Effects of feeding way,reaction temperature,and pH on the property of gel were researched.Phase composition and microstructure of the materials were analyzed by X-ray diffraction,Fourier transform-infrared reflection spectroscopy,and electron scanning microscopy. Results showed that the property of gel was the best under the following conditions:the feeding way was adding triethylphosphate after the hydrolysis of tetraethoxysilane ethanol solution for 30 min with HNO3as catalyst,and then introducing Ca and Mg in the form of nitrate,introducing F in the form of NH4HF2;the reaction temperature was 25℃;and pH was at 1~2. Main crystalline phases of the sintered glass powder were apatite and wollastonite.Particles whose sizes and shapes were uniform did not make any apparent agglomeration.Porosity was at 35%~40%.
apatite;wollastonite;bioactivity
TQ174.7
A
1006-4990(2011)07-0036-03
2011-01-25
杨英(1986— ),女,硕士研究生,主要从事无机精细化工方向研究。
联 系 人:徐旺生
联系方式:yangying860711@126.com
