滇池底泥制备的生物炭对菲的吸附-解吸*
2011-11-08陈会会王震宇宋秀丽
陈 宁 吴 敏** 许 菲 陈会会 王震宇宋秀丽 张 迪 宁 平 潘 波
(1.昆明理工大学环境科学与工程学院,昆明,650093 2.中国海洋大学环境科学与工程学院,青岛,266100)
滇池底泥制备的生物炭对菲的吸附-解吸*
陈 宁1吴 敏1**许 菲1陈会会1王震宇2宋秀丽2张 迪1宁 平1潘 波1
(1.昆明理工大学环境科学与工程学院,昆明,650093 2.中国海洋大学环境科学与工程学院,青岛,266100)
将滇池草海底泥在不同烧制温度下制成生物炭,并用元素分析法表征其元素组成,溴化钾压片法表征其红外光谱,CO2和N2法表征其比表面积、孔体积、孔径.以菲作为模型化合物来研究有机污染物在生物炭上的吸附-解吸行为,以此深入了解生物炭施用中对有机污染物环境行为和风险的影响.结果表明,生物炭随烧制温度升高,芳香性升高、亲水性降低、极性降低.生物炭随烧制温度升高,对水中菲的吸附能力不断增强.解吸滞后效应随生物炭烧制温度升高而不断增强,这与分配作用和孔隙填充作用有关.
生物炭,多环芳烃,土壤改良,解吸滞后,非线性吸附.
生物炭是生物质经过热解后形成的具有多孔特性的木炭,它在土壤改良中的应用不仅可以提高土壤的pH,增加总氮和总磷,促进植物根系的生长,利于真菌类和微生物的生长[1],而且能够提升营养物质的保留和水分储蓄能力[2].这些特性使生物炭作为潜在的土壤改良剂而在荒漠化治理和改观干旱农业等方面发挥重要作用[3-4].此外,生物炭在减缓全球环境恶化方面的作用也显得越来越重要[5].生物炭可以作为CO2、CH4等气体的吸收汇而将其固化在土壤中,这不仅可以改良土壤水文特性,为植物提供广泛的C源,而且可以降低温室气体对全球变暖的贡献.研究表明,环境中普遍存在的生物质[6]如木材、城市垃圾、家畜禽遗体、粪便,都可以作为制备生物炭的材料,这些材料来源广泛、价格低廉,因此生物炭的低成本和可持续性预示它将是未来主要的环保能源.生物炭作为一种新型的炭材料,具有非常重要的应用价值.滇池草海底泥的有机质含量高(50%以上),所以具有制备生物炭的潜在可行性;而且,滇池的环境污染日益严重,其底泥的处理也是一个亟待解决的问题.若能将底泥制备的生物炭应用于实际生产,则既解决了相关的环境问题,又为社会创造价值.
生物炭作为土壤改良剂施用,一个重要问题是这个过程会改变各种污染物的环境行为.多环芳烃(PAHs)包括了大量的有机污染物,具有基因诱变、致癌作用,而且在低浓度就呈现了环境毒性.多环芳烃在土壤中的吸附-解吸研究已是当今热点,但是关于生物炭对于有机污染物环境行为影响的研究却鲜为人知.
在对多环芳烃的研究中,关于菲的环境行为模拟研究具有最好的数据储备.因此,本文以菲作为多环芳烃的模型化合物来研究有机污染物在生物炭上的吸附-解吸行为,以此深入了解生物炭施用中对有机污染物环境行为和风险的影响.本研究用滇池草海沉积物制备生物炭,探讨菲在其中的吸附机理及生物炭理化特征对菲吸附的影响,为生物炭环境效应的准确评价和合理使用提供重要的理论依据.
1 材料与方法
1.1 吸附剂的制备
实验采用滇池草海底泥作为生物质代表,手工剔除底泥杂物,冷冻干燥,然后经研磨粉碎,过60目筛.在氮气保护下,分别于200℃、300℃、400℃和500℃在马弗炉中灼烧4 h,冷却至室温后取出装于棕色瓶中,待用.制得的样品标记为T0、T200、T300、T400和T500,数字表示相应烧制温度(T0为原沉积物).
1.2 吸附剂的表征
本实验采用溴化钾压片法[7]对所制备的生物炭进行傅立叶红外光谱(Varian 640-IR)表征.红外光谱为在4000—400 cm-1波数范围内以8 cm-1精度扫描20次获得的光谱[8].
生物炭用元素分析仪(Elementar MicroCube)分析其C、H和N含量,并用该设备的专用模式分析O含量.用BET方法分别在CO2和N2作为介质的条件下,测定生物炭的比表面积、孔体积和孔径.
1.3 吸附-解吸实验步骤
将菲(Acros Organics,分析纯,97%)在甲醇中配制成 1200 mg·L-1储备液待用;称取 2.00 mg固体样品于8 mL的样品瓶中,并分别加入不同浓度的菲溶液.菲溶液由储备液在背景溶液(0.01 mol·L-1CaCl2和200 mg·L-1NaN3)中逐级稀释为0.10—1.20 mg·L-1的 7 个浓度点,每个浓度点有两个重复;背景溶液中的CaCl2用来絮凝固体颗粒以保持其完整性;NaN3用于灭菌,防止菲的生物降解.样品瓶在25℃下避光,60 r·min-1旋转振荡7 d;预备试验表明吸附平衡在7 d完成.吸附平衡后,以2000 r·min-1的速度离心15 min;取6.00 mL上清液,加入8.00 mL正己烷萃取,激烈振摇至出现完全乳化现象,静置分层后再振摇一次,清晰分层以后,用荧光分光光度计(PerkinElmer,LS55)测定正己烷相中菲的浓度,并绘制吸附等温线.向原吸附实验的样品瓶中加入6.00 mL背景液,用同样的分析方法和平衡时间,测定解吸平衡后菲的浓度.文中吸附曲线由SigmaPlot 10.0拟合.
1.4 数据处理
根据实验数据绘制等温吸附曲线,并分别用Freundlich和双模式模型对吸附数据进行拟合.

其中,Qe(mg·kg-1)为固相浓度,Ce(mg·L-1)为液相浓度,KF[(mg·kg-1)/(mg·L-1)N]为 Freundlich 吸附系数,N(无量纲)为非线性指数.单点吸附系数计算为 Kd=Qe/Ce=KFCN-1e.双模式模型中公式S(D)是线性吸附形式,Kp(L·kg-1)是分配平衡常数;S(H)是Langmuir非线性吸附形式,S0i(mg·kg-1)是Langmuir吸附容量,bi(L·mg-1)是吸附结合能系数;C是液相浓度(mg·L-1);n取1.
标准可决系数r2受到数据点个数和拟合参数的影响,所以拟合效果用可调可决系数r2adj进行比较,综合度量回归模型对样本观测值的拟合优度.

其中,m是拟合曲线中数据点的个数,n是拟合方程中的参数个数[10].
同时,计算了以下描述菲解吸特征的参数:

其中,Q'e(mg·kg-1)和C'e(mg·L-1)分别为解吸平衡时的固相浓度和液相浓度.
2 结果与讨论
2.1 生物炭的性质
随着烧制温度升高,生物炭的C含量变化不明显,但是H含量随烧制温度呈递减趋势;C/H原子比随烧制温度的升高而不断增大,说明生物炭在烧制过程中,形成了较多的芳香环结构,生物炭由此变得非常紧凑.Chen[11]等人用橘子皮、花生壳等制备的生物炭中,C含量随着烧制温度的升高而增大,认为这是生物炭从软碳向硬碳变化的过程.这一结果与本研究不太一致,但需要指出,本研究用于烧制生物炭的是沉积物颗粒,约有一半质量的颗粒是无机矿物.有机质与无机矿物形成致密的复合体,O、N、H、S等元素更容易被保留下来.
本文采用N2吸附和CO2吸附法对生物炭的表面特征进行了分析.两种方法都显示,比表面积和孔体积随烧制温度升高而逐渐增大.CO2测定的孔径没有明显的变化,但是N2测定的孔径显示了随烧制温度的升高而降低的现象.虽然N2与CO2分子大小相当,但是从数值上看,两种方法的测定结果相差很大.CO2测定的比表面积普遍比N2测定的比面积高3倍以上,而其测定的孔体积只是N2测定值的1/3.两种方法测定的孔径最大差别到50倍以上.需要指出,CO2和N2方法测定比表面积的操作温度差别非常大,N2为-80℃,而CO2为-4℃.研究认为,N2测定时,由于温度太低,有机质固化,很多内部的小孔隙N2无法进入[12];因此,N2测定的结果可能只能反映相对比较大的孔隙的特征,比如从孔径上看,直径在100 Å以上的孔隙.但是,CO2则不会受到温度的影响,能够得出相对客观全面的结果.对两个测定结果的比较,可能对生物炭内部结构有更加准确的认识.N2测定的孔径随烧制温度增大而降低,而CO2测定的小孔直径变化不大,这一变化与比表面积和孔体积的增大相伴发生,表明沉积物颗粒中相对大的孔隙在烧制过程中被破坏,可能分离成若干直径较小的孔隙;同时,由于烧制过程中,沉积物颗粒进一步被玻璃态化,形成更多新的小孔隙.这些孔隙对生物炭发挥重要的环境功效起到了重要的作用.

表1 生物炭的元素质量组成、灰分含量、比表面积、孔体积、孔径Table 1 Elemental compositions,ash contents,specific surface areas,total pore volumes and pore diameters of the bio-adsorbents
用红外光谱分析不同烧制温度的生物炭,得到图1的结果.红外结果显示,—OH(3436 cm-1)、C ==O(1634 cm-1)[13]、以及 C—O—C(1031 cm-1)[14]随烧制温度的变化不明显,但是—CH2—(2927 cm-1和2856 cm-1)[15]和—CH3(1085 cm-1)随烧制温度升高而减少,与元素分析的结果一致.2360 cm-1处的峰为检测时进入的CO2而产生的,不代表生物炭性质的变化.
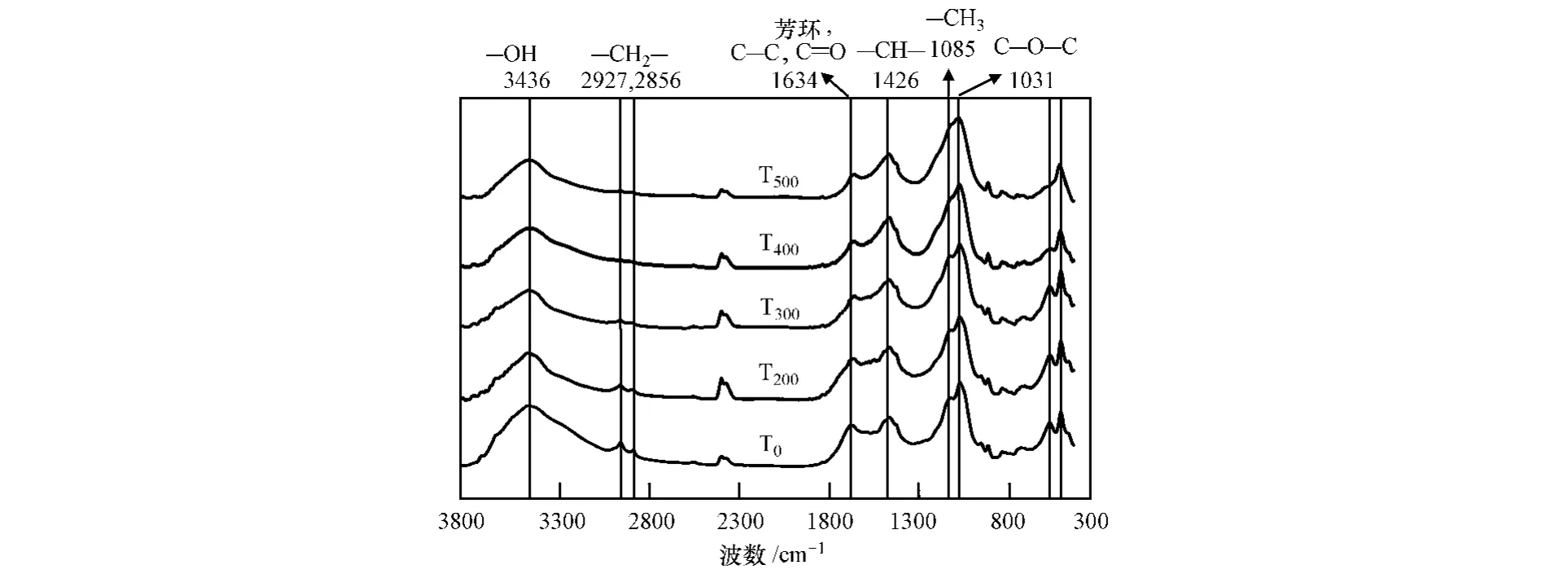
图1 生物炭的红外谱图Fig.1 Infrared spectra of bio-adsorbents
2.2 生物炭对菲的吸附
尝试了Freundlich和双模式模型对吸附等温线的拟合,结果列于表2.从可调可决系数r2adj看,对同一条吸附等温线,双模式模型的r2adj整体上高于Freundlich模型,表现了其较好的拟合优度.但是,曲线拟合中一个普遍存在的问题是,参数越多,模型的不稳定性越大.从本拟合来看,双模式模型对本研究中吸附等温线的拟合非常不稳定,表现为拟合参数较大的误差,比如样品T0、T200和T500的Kp值,T0、T200和T300的S0值,以及T0、T200和T500的b-1值,在这样的拟合结果下,不管是对拟合参数的比较和讨论,还是对双模式模型反应出来的分配过程和吸附过程的分离计算,都有非常大的不确定性,因此,对本研究结果的讨论,主要集中于Freundlich模型的拟合结果.

图2 菲的吸附等温线(a)Freundlich模型;(b)双模式模型Fig.2 The adsorption isotherms of phenanthrene
随着烧制温度的升高,生物炭对菲的吸附逐渐增强.对沉积物(T0)样品,Freundlich吸附等温线的非线性指数N在0.05显著性水平下与1没有显著差别(0.978±0.040,表2),但随着烧制温度升高,N逐渐降低,非线性程度逐渐增加,当烧制温度升高到500℃时,N值降低到0.325.前期研究指出,有机质的紧凑程度越高,憎水性有机污染物在其中的吸附由孔隙填充贡献的比例越高,表观吸附表现为更强的非线性特征[16].这一吸附现象与生物炭的理化性质随烧制温度的变化一致,表明非线性程度是可以通过吸附剂的性质来预测的.从吸附系数KF或者KOC来看,烧制温度达到300℃以上后,生物炭对菲的吸附比普通土壤高1—2个数量级[17],表现了生物炭对菲非常强的吸附性能.因此,在开放环境大量使用生物炭会对以菲为代表的憎水性有机污染物大量滞留而影响其环境迁移行为及其风险特征.

表2 水中菲在生物炭上的等温吸附曲线的回归参数Table 2 Fitting results of phenanthrene sorption isotherms
2.3 被生物炭吸附菲的解吸
被生物炭吸附的菲的解吸率随着烧制温度升高而降低(图3a).对于T0,被吸附的菲的释放率[18]在30%—40%;而T200释放率急剧下降至10%—20%,T300—T500释放率已降至10%以下;在较高烧制温度下释放率极低(5%以下),这说明菲更倾向于滞留在生物炭上,而不是重新回到水中.同时,随着菲的固相浓度升高,释放率略微上升,这可能与分配作用和孔隙填充作用在表观吸附中所占的比例不同有关.研究表明,随着固相浓度的增大,孔隙填充作用在表观吸附中的贡献降低,而分配作用在其中的贡献增大[19].分配作用可逆的吸附-解吸行为使释放率增大.本研究中计算的滞后系数((Qe-Q'e)/Q'e)[20]与释放率有类似的数学关系,两者表现了一致性.
解吸过程中的单点吸附系数K'd与固相浓度的关系显示于图3c中.T0的K'd随固相浓度变化不明显,从另外一个角度证实了T0对菲吸附的理想线性特征.而T300—T500样的K'd表现了随菲的固相浓度升高K'd降低的规律,而且随着烧制温度的升高,K'd降低的斜率也越来越快,这一现象与吸附的非线性特征一致.为有效比较不同生物炭的解吸滞后特征,本研究中计算了相对滞后率(Kd/K'd,图3d).在T0时,Kd/K'd≈1,说明滞后效应不明显,但随烧制温度升高,Kd/K'd不断下降,即滞后越来越明显.值得注意的是,用CO2测定的孔径随烧制温度的变化不明显,显然可以排除直径在5 Å左右的孔隙对解吸滞后的影响.N2测定的孔径分布随烧制温度有非常明显的变化,孔径在300 Å左右(T0和T200)的固体颗粒解吸滞后不明显,但是孔径在100 Å及以下时,生物炭表现了非常强的滞后性(图3d).

图3 菲的解吸特性释放率(a)和滞后系数(b)是针对固相浓度在解吸过程中的变化计算的,而K'd(c)与Kd/Kd'(d)是针对吸附和解吸的比较Fig.3 Desorption characteristics of phenanthrene
3 结论
生物炭随烧制温度增加,芳香性升高、亲水性降低、极性降低.生物炭随烧制温度的升高,对水中菲的吸附能力不断增强.解吸释放率、滞后系数随生物炭烧制温度升高而降低.随着菲的固相浓度升高,释放率略微上升,这可能与分配作用和孔隙填充作用在表观吸附中所占的比例不同有关.相对原始沉积物而言,烧制后的生物炭对菲的吸附更高,解吸滞后更强,表明生物炭可能极大地降低了菲的迁移性,从而消弱其环境风险.这个结果可能对其它的憎水性有机物都有重要的参照.然而,还需要有更多的毒性和生物积累试验以及更大尺度的污染物环境行为研究进行系统的论证.
[1]Tenenbaum D J.Biochar:Carbon mitigation from the ground up[J].Environ Health Perspect,2009,117:A70-A73
[2]Glaser B,Lehmann J,Zech W,et al.Ameliorating physical and chemical properties of highly weathered soils in the tropi cs with charcoal —a review[J].Biol Fert Soils,2002,35:219-230
[3]Mbagwu J S C,Piccolo A.Effect of humic substances from oxidized coal on soil chemical properties and maize yield//Drozd J,Gonet S S,Senesi N,et al.The Role of Humic Substances in Ecosystems and in the Environmental Protection[M],Poland:Wroclaw,1997:921-925
[4]Glaser B,Balashov E,Haumaier L,et al.Black carbon in density fractions of anthropogenic soils of the Brazilian Amazon region[J].Org Geochem,2000,31(7/8):669-678
[5]Guo L P,Lin E.Carbon sink in cropland soils and the emission of greenhouse gases from paddy soils:a review of work in China[J].Chemosphere-Glabal Change Science,2001,3(4):413-418
[6]Jacobson M Z.Strong radiative heating due to the mixing state of black carbon in atmospheric aerosols[J].Nature,2001,409(6821):695-697
[7]翁诗甫.傅里叶变换红外光谱仪[M].北京:化学工业出版社,2005,5:83-87
[8]Hou J,Pan B,Niu X K,et al.Sulfamethoxazole sorption by sediment fractions in comparison to pyrene and bisphenol A[J].Environ Pollut,2010,158(9):2826-2832
[9]Xing B S,Pignatello J J.Dual-mode sorption of low-polarity compounds in glassy poly(vinyl chloride)and soil organic matter[J].Environ Sci Technol,1997,31(3):792
[10]Wang Z Y,Yu X D,Pan B,et al.Norfloxacin sorption and its thermodynamics on surface-modified carbon nanotubes[J].Environ Sci Technol,2010,44(3):978-984
[11]Chen B L,Chen Z M.Sorption of naphthalene and 1-naphthol by biochars of orange peels with different pyrolytic temperatures[J].Chemosphere,2009,76(1):127-133
[12]Pignatello J J.Soil organic matter as a nanoporous sorbent of organic pollutants[J].Adv Colloid Interface Sci,1998,77:445-467
[13]Yu J,Wang N,Ma X,et al.Fabrication and characterization of poly(lactic acid)/acetyl tributyl citrate/carbon black as conductive polymer composites[J].Biomacromolecules,2008,9(3):1050-1057
[14]Kang S H,Xing B S.Phenanthrene sorption to sequentially extracted soil humic acids and humins[J].Environ Sci Technol,2005,39:134-140
[15]Wen B,Zhang J J,Zhang S Z,et al.Phenanthrene sorption to soil humic acid and different humin fractions[J].Environ Sci Technol,2007,41(9):3165-3171
[16]Pan B,Xing B S,Liu W X,et al.Distribution of sorbed phenanthrene and pyrene in different humic fractions of soils and importance of humin[J].Environ Pollut,2006,143(1):24-33.
[17]潘波,刘文新,林秀梅,等.水溶性有机碳对菲吸附系数测定的影响[J].环境科学,2005,26(03):162-166
[18]潘波.土壤有机质的存在形式及对菲的吸附特征[D].北京:北京大学博士学位论文,2005
[19]陈宝梁,周丹丹,朱利中,等.生物炭质吸附剂对水中有机污染物的吸附作用及机理[J].中国科学 B辑:化学,2008,38(6):530-537
[20]Huang W,Weber W J Jr.A distributed reactivity model for sorption by soil and sediments.11.Slow concentration-dependent sorption rates[J].Environ Sci Technol,1998,33:3549-3555
SORPTION AND DESORPTION OF PHENANTHRENE IN THE BIOCHAR DERIVED FROM DIANCHI SEDIMENT
CHEN Ning1WU Min1XU Fei1CHEN Huihui1WANG Zhenyu2SONG Xiuli2ZHANG Di1NING Ping1PAN Bo1
(1.Faculty of Environmental Science and Engineering,Kunming University of Science& Technology,Kunming,650093,China;2.College of Environmental Science and Engineering,Ocean University of China,Qingdao,266100,China)
As a new carbon-based material,biochar has attracted great research attention.In this study,biochars were derived at different temperatures from Dianchi Lake sediment which consists of more than 50%organic matter.These biochars were characterized for their elemental composition,functional groups,surface area,pore volume,pore diameter and sorption/desorption properties with phenanthrene.The C content in the biochars did not vary significantly with pyrolyzing temperatures,probably because the complexation of organic matter and inorganic mineral particles and the loss of other elements(such as O,N,H,and S)was not dramatic.Increased surface areas were observed for biochars with increasing pyrolysis temperature.FTIR characterization showed decreasing—CH2— and—CH3contents with increasing temperature,but—OH,C==O ,and C—O—C did not show obvious change.Biochar sorption with phenanthrene increased and desorption hysteresis increased with pyrolyzing temperature.The sorption isotherms were fitted well with Freundlich and dual mode models.But the dual mode model showed significant variation for the parameters and thus could not be applied to illustrate sorption mechanisms.The results from Freundlich model were the main discussion focus.The sorption nonlinearity increased with pyrolyzing temperature,which could be well explained by biochar properties.Phenanthrene sorption in biochars was 1—2 orders of magnitude higher than that in natural soils/sediments.The high sorption and strong desorption hysteresis of the biochar could reduce the environmental risks of phenanthrene.
biochar,polyromatic hydrocarbons,soil remediation,hysteresis,nonlinear sorption.
2011年3月26日收稿.
*昆明理工大学学生课外学术科技创新基金课题(2010BA160);国家自然科学基金(40973081,40803034);教育部留学回国人员启动基金;云南省学术带头人后备人才项目资助.
**通讯联系人,Tel:+86-871-5102829;E-mail:kustless@gmail.com
