肝素杂化材料的制备及抗凝血性质的初步研究
2011-09-29宋玉民李清萍张玉梅马新贤王怡云
宋玉民 缐 萍 李清萍 张玉梅 马新贤 张 强 王怡云
(1西北师范大学化学化工学院,兰州 730070)(2甘肃省肿瘤医院,兰州 730050)
肝素杂化材料的制备及抗凝血性质的初步研究
宋玉民*,1缐 萍1李清萍1张玉梅1马新贤1张 强2王怡云2
(1西北师范大学化学化工学院,兰州 730070)(2甘肃省肿瘤医院,兰州 730050)
以甲苯二异氰酸酯(TDI)中的-NCO基与纳米金属氧化物表面的羟基发生反应,得到改性纳米金属氧化物,并使其与肝素钠(Heparin)进行接枝反应生成肝素杂化材料,结合红外、热重、扫描电镜(SEM)等表征方法,确定纳米金属氧化物确实接枝到了肝素钠的表面。通过对体外凝血时间和复钙时间的测定,来初步研究肝素杂化材料的抗凝血性质。结果表明:肝素杂化材料的抗凝血时间和复钙时间均比肝素钠的要短,表明它的抗凝血性比肝素钠的抗凝血性要弱一些;但比纳米金属氧化物和空白组的抗凝血时间和复钙时间要长,说明肝素杂化材料的抗凝血性与其相比则有明显的提高。
TDI;纳米金属氧化物;肝素;复钙时间;抗凝血性
肝素是一类常用的抗凝血药物,它是因从动物的肝脏中提取而得名的,肝素是一种多糖,作为预防和治疗血栓的药物,它应用于临床已经有70多年了[1-4]。肝素的抗凝血作用主要是通过与抗凝血酶Ⅲ(AT-Ⅲ)相结合来完成的,它可以用于心导管检查、体外循环、血液透析与器官移植等方面,也可用来防治血栓栓塞性疾病[5]。由于肝素研究的较早,经Niers等[6]临床试验研究表明:肝素不仅在抗凝血方面有良好的作用而且肝素以及肝素衍生物在治疗癌症方面也有着积极的治疗作用,将肝素用于癌症初期病人可以对肿瘤的扩散起到抑制作用。
近年来血栓栓塞性疾病发病形式多样,广泛发生在人体的动脉和静脉系统,严重威胁着人类的健康。针对肝素在用药过程中可引起自发性出血、骨质疏松症、血小板减少症和注射部位轻度血肿和坏死等症状[7],其它多种多样的抗凝血物质的研究也应用而生[8]。经李潮[9]、鲁险锋[10]等研究纳米氧化锌等物质由于表面具有羟基的缘故也具有一定的抗凝血性,鉴于肝素和纳米金属氧化物在临床方面广泛的应用性和潜在的生物医学效应,同时为克服肝素抗凝血效果较强而导致自发性出血等副作用和纳米金属氧化物抗凝血时间短的缺陷,本文报道了利用纳米氧化锌和纳米氧化钛表面具有羟基的特点,分步用TDI与纳米金属氧化物和肝素进行反应生成接枝杂化材料,并研究了肝素杂化材料的抗凝血性质。结果表明,在相同条件下,杂化材料的抗凝血时间相较之肝素钠要短一些(约为其1/2),但较之纳米金属氧化物抗凝血时间要长(约为其3倍)。初步达到了通过制备杂化材料改善二者抗凝血性的预期目标。目前抗凝血材料在医学上的应用较为广泛,例如人造血管,心血管造影导管,生物医学薄膜[11]等,这些材料都要求要与人体血液有良好的相容性,即抗凝血性能要好,因此本研究结果对通过接枝反应生成的杂化材料在临床应用和生物医用材料应用方面有较大的参考价值。
1 实验部分
1.1 原料与仪器
肝素钠(上海山浦化工有限公司);过硫酸铵(天津市百世化工有限公司);甲苯 2,4-二异氰酸酯(TDI,国药集团化学试剂有限公司);硬脂酸(上海康达氨基酸厂);二丁基二月桂酸锡(上海试剂一厂);丙酮,四氢呋喃(天津市光复精细化工研究所);纳米氧化钛,纳米氧化锌(自制);人体血液:取自健康成人;实验用水为二次蒸馏水,其余均为分析纯试剂。
电镜S-4800(日本日立公司);800型电动离心沉淀器;DZF-6020型真空干燥箱(上海一恒科技有限公司);KQ-100M超声波清洗器(东莞市科桥超声波设备有限公司);DG/DTA-6300型热重-差热分析仪 (美国PE公司);FTS-3000型红外光谱仪(美国PE公司)。
1.2 实验方法
1.2.1 纳米金属氧化物的表面修饰
纳米金属氧化物用硬脂酸法制得[12]。称取5 g纳米氧化锌或纳米氧化钛在120℃下真空干燥7 h。分别将干燥后的纳米金属氧化物5 g,100 mL无水丙酮和5 g TDI加入三口烧瓶,在氮气保护下室温超声处理2 h后,加入0.3 mL二丁基二月桂酸锡,80℃下超声反应2 h。反应后经离心,洗涤,真空干燥,得纳米金属氧化物-TDI。
1.2.2 纳米金属氧化物表面与肝素的接枝
各称取纳米金属氧化物-TDI 0.2 g加入到装有50 mL THF的圆底烧瓶中,超声分散1 h,随后加入0.2 g肝素钠和0.1 g的过硫酸铵,在氮气保护下常温搅拌6 h。离心,洗涤得固体,在50℃下真空干燥15 h。 分别记为:ZnO-TDI-Heparin和 TiO2-TDIHeparin。
1.2.3 反应机理
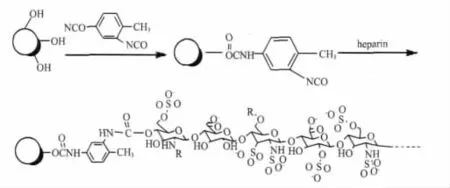
1.2.4 溶液的配制
分别称取0.1 g肝素钠,肝素杂化材料及与其相对应的纳米金属氧化物溶于10 mL二次蒸馏水中。其中肝素钠易溶于水,直接进行配制,而杂化材料微溶于水,纳米金属氧化物难溶于水,故在其溶液中加入2滴1%的吐温-80水溶液进行乳化,常温搅拌5 h,得到溶液浓度均为0.01 g·mL-1,室温保存备用,待需用时再进行稀释。对照组为1%的吐温-80水乳化液。
1.2.5 全凝血时间(CT)的测定
取洁净的玻璃试管,将其分为6组,每组3个平行样。第 1 组为空白对照,第 2、3、4、5、6 组中分别加入肝素、纳米氧化锌、纳米氧化钛、ZnO-TDI-Heparin和TiO2-TDI-Heparin杂化材料溶液(加入的溶液浓度均为 0.1 mg·mL-1,体积为 0.1 mL),同时将加好样品的6组试管放在37℃水浴中恒温5 min,然后沿试管壁缓慢加入1 mL人体血液,3 min后每隔30 s倾斜试管进行观察,直到血液凝固不再流动为止,记为全血凝血时间[13-14]。
1.2.6 复钙时间(RT)的测定
取9 mL人体血液,迅速加入装有1 mL(38 mg·mL-1)枸橼酸钠的试管中,在1 000 r·min-1的条件下离心分离10 min,将分离出的血浆置冰水浴中保存备用[15]。
取6组玻璃试管,每组3支,每支试管中加入经过上述处理后的血浆0.1 mL,第1组为生理盐水对照组,第2、3、4、5、6组中分别加入肝素、纳米氧化锌、纳米氧化钛、ZnO-TDI-Heparin和 TiO2-TDIHeparin杂化材料溶液(加入的溶液浓度均为0.1 mg·mL-1,体积为 0.1 mL)。 同时将加好样品的 6组试管放在37℃水浴中恒温3 min,随后在各试管中加入 0.1 mL 氯化钙溶液(cCaCl2=0.025 mol·L-1)仍让其处于37℃恒温水浴中,然后开启秒表进行计时,直到试管底部出现纤维状细丝且纤维蛋白凝固时则计时结束[16],记为复钙时间。
2 结果与讨论
2.1 红外光谱分析
图1,图2分别是纳米氧化锌和纳米氧化钛的系列红外谱图。图1中纳米ZnO的红外吸收曲线在1 622和3 435 cm-1处的吸收峰表明了纳米氧化锌表面存在有羟基[17],与纳米氧化锌相比,纳米ZnOTDI的红外吸收曲线在1645和1539cm-1处新出现的峰则为氨基甲酸酯的吸收峰[18-19]。而据文献报道2 270 cm-1处的振动吸收峰是-NCO基团的吸收峰[20],其原因是TDI第2位和第4位的-NCO基团活性存在差异,使得活性高的第4位-NCO充分反应而第2位-NCO大多没有反应,所以-NCO基团的特征吸收峰得以保留。由此说明TDI确实与纳米金属氧化物表面的羟基发生了反应,使纳米氧化锌得到了改性。而ZnO-TDI-Heparin的红外吸收曲线与ZnO-TDI的曲线相比,2 270 cm-1处-NCO的特征吸收峰消失,3344 cm-1处出现的一宽峰则是肝素分子中的各种基团如-COOH、-OH、-NH2综合效应的结果,这进一步说明TDI改性的纳米氧化锌接枝到了肝素分子上。纳米氧化钛的系列红外图谱与纳米氧化锌的类似,只是图2中的TiO2-TDI-Heparin红外吸收曲线与ZnO-TDI-Heparin相比-NCO的吸收峰稍有保留,这可能是由于氧化钛表面接枝的TDI太多致使TiO2-TDI未与肝素钠完全反应所致。

图1 纳米 ZnO,纳米 ZnO-TDI,ZnO-TDI-Heparin红外谱图Fig.1 FTIR spectra of nano-ZnO before and after the grafting

图2 纳米 TiO2,纳米 TiO2-TDI,TiO2-TDI-Heparin红外谱图Fig.2 FTIR spectra of nano-TiO2before and after the grafting
2.2 热重分析
图3是纳米氧化锌,纳米ZnO-TDI,ZnO-TDIHeparin的TGA图,图4是纳米氧化钛,纳米TiO2-TDI,TiO2-TDI-Heparin的 TGA 图。
从图3和图4的TGA曲线中可以看出,纳米氧化锌和纳米氧化钛在100~300℃之间出现失重现象,失重率大约为1.5%,这主要是由于吸附在纳米粒子表面的水分以及少量有机溶剂引起的,在300℃之后,大约2%的失重是纳米金属氧化物表面的羟基以及相邻羟基间脱水的结果。TDI改性后的纳米氧化锌和纳米氧化钛的热重曲线显示100℃左右有略微的失重,是由纳米金属氧化物-TDI表面的吸附水引起的;250℃左右失重现象较为明显,则是由反应接枝到纳米金属氧化物表面的TDI热分解造成的。由纳米金属氧化物-TDI-Heparin杂化材料的热重曲线可知,200℃开始出现失重是由于接枝到纳米金属氧化物表面的肝素及TDI热分解造成的。由热重曲线可以得知氧化钛和氧化锌的接枝率[21-22]分别为 36.9%,47.02%。

图3 纳米 ZnO,纳米 ZnO-TDI,ZnO-TDI-Heparin热重图Fig.3 TGA curves of nano-ZnO before and after the grafting

图4 纳米 TiO2,纳米 TiO2-TDI,TiO2-TDI-Heparin热重图Fig.4 TGA curves of nano-TiO2before and after the grafting
2.3 电镜分析
从图中可以看到,杂化材料分别为层状和纳米纤维状结构的固体,长度在50~400 nm不等,但看不到纳米金属氧化物粒子,这表明在纳米氧化物表面成功的发生了接枝反应,肝素已将氧化物粒子进行包覆。进一步说明各纳米氧化物均被TDI改性,并反应接枝。

图5 纳米ZnO的扫描电镜图Fig.5 SEM image of nano-ZnO

图6 ZnO-TDI-Heparin的扫描电镜图Fig.6 SEM image of ZnO-TDI-Heparin

图7 纳米TiO2的扫描电镜图Fig.7 SEM image of nano-TiO2

图8 TiO2-TDI-Heparin的扫描电镜图Fig.8 SEM image of TiO2-TDI-Heparin
2.4 凝血时间
表1为空白组,肝素钠,纳米氧化锌,纳米氧化钛,ZnO-TDI-Heparin,TiO2-TDI-Heparin 的全血凝血时间测定结果。在相同浓度的条件下肝素钠的抗凝效果较好持续的时间也最长,纳米氧化锌和纳米氧化钛的抗凝时间稍长于血液的正常凝固时间,但经过接枝后的ZnO-TDI-Heparin和TiO2-TDI-Heparin的凝血时间则明显长于各对应的金属氧化物,但相对于肝素钠抗凝血时间则要短一些。根据文献[23]肝素分子中含有五糖的特殊序列,肝素中的该五糖序列可提供与抗凝血酶(ATⅢ)相结合的位点,使其形成三元复合物,从而使得ATⅢ能有效灭活凝血酶,达到抗凝血的作用。在本实验中杂化材料的凝血时间较肝素短,可能是由于通过杂化反应后,肝素的五糖序列结构有所改变,使得抗凝血酶(ATⅢ)难以找到与肝素杂化材料相结合的位点,影响了杂化材料对凝血过程的作用,从而使得肝素杂化材料的抗凝作用弱于肝素但强于相对应的金属氧化物。
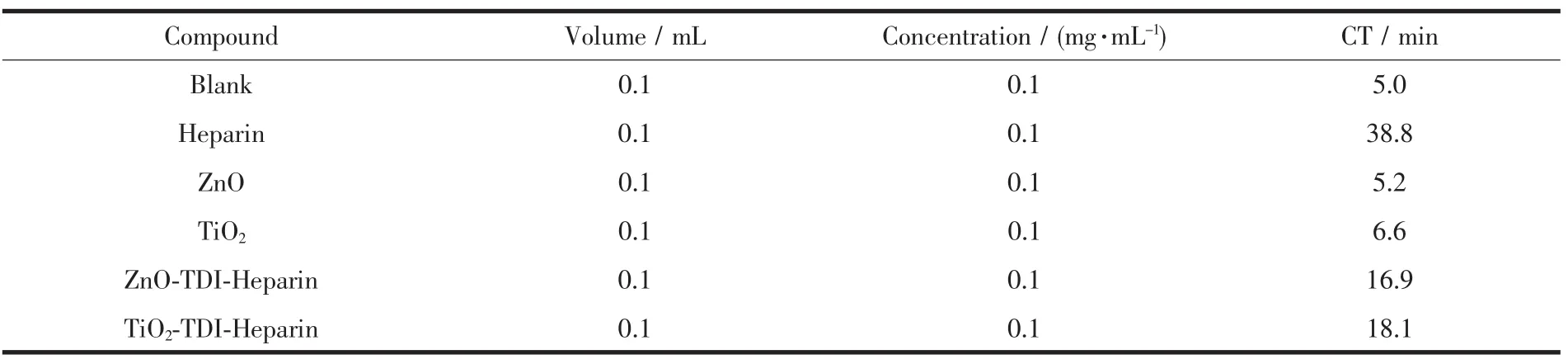
表1 杂化材料对人体体外血液凝固时间的影响Tabble 1 Eeffect of hybrid materials on the coagulation time(CT)in human
2.5 浓度对凝血时间的影响
为了测定杂化材料的凝血时间与其浓度之间的关系,选定ZnO-TDI-Heparin杂化材料为实验对象,配制了不同浓度的ZnO杂化材料进行测试。结果见表2,从表2的数据可以看到:随着杂化材料浓度的不断增加,全凝血时间也在逐渐变长,即抗凝血性能越来越好。这一现象说明凝血时间与物质的浓度之间存在着一定的量效关系,也就是说可以根据临床不同程度的要求,调节杂化材料的浓度来治疗血栓疾病,或者用于医用材料方面,使其达到物尽其用的效果。

表2 不同浓度杂化材料对人体体外血液凝固时间的影响Table 2 Effect of Hybrid materials with different concentrations on the coagulation time(CT)in human
2.6 对复钙时间的影响
表3是各物质复钙时间的测定结果。从表3中可以看出:肝素钠的复钙时间最长,在2 h内未出现纤维丝状物。而ZnO-TDI-Heparin,TiO2-TDI-Heparin杂化材料的复钙时间与生理盐水对照组和相应的纳米金属氧化物组相比均得到了延长,但与肝素钠的复钙时间相比则要小一些。这一结果说明了杂化材料可延长凝血酶所致纤维蛋白的凝固时间而具有一定的抗凝血作用[24],这一实验结果与上述的抗凝血实验得到了相互印证。
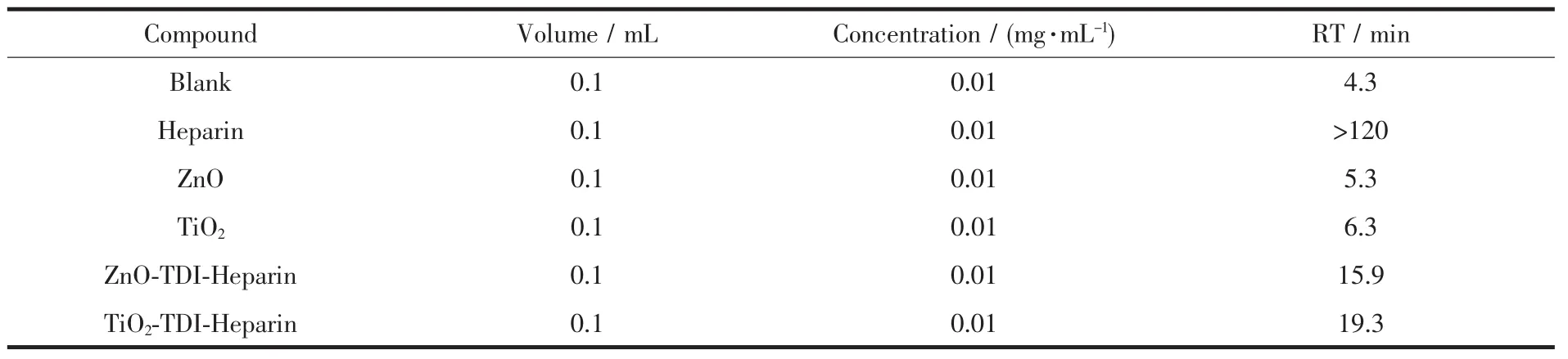
表3 杂化材料对人体体外血液复钙时间的影响Table 3 Effect of hybrid materials on the recalcification time(RT)in human
3 结 论
正常生理情况下,人体的凝血系统与抗凝血系统之间维持着动态平衡,如果此平衡遭到破坏,就会导致凝血或者抗凝血过程的发生[25]。该过程一般是由多种凝血因子参与的复杂生化反应过程,而肝素普遍被人们认为是通过与ATⅢ结合阻断Xa和Ⅱa因子来完成抗凝血过程的[26-27]。本实验通过接枝反应生成了肝素氧化锌、肝素氧化钛杂化材料,经全凝血时间和复钙时间的测定,表明均具有良好的抗凝血性质且凝血时间与杂化材料的浓度之间存在着一定的量效关系,在相同的条件下,杂化材料的抗凝血时间比肝素钠短(约为其1/2),但比对应的纳米金属氧化物抗凝血时间要长(约为其3倍),初步达到了通过制备杂化材料改善二者抗凝血性的预期目标。新合成的杂化材料既克服了肝素抗凝血效果较强而导致自发性出血等副作用和纳米金属氧化物抗凝血时间短的缺陷,同时又具有较好的抗凝血性质。
[1]Young E.Thromb.Res.,2008,122:743-752
[2]Boneu B.Thromb.Res.,2000,100:113-120
[3]Young E,Venner T,Ribau J,et al.Thromb.Res.,1999,96:373-381
[4]Li B,Suwan J,Martin J G,et al.Biochem.Pharm.,2009,78:292-300
[5]WANG Tian-Ling(王天玲),DING Hai-Jun(丁海军),WANG Wei-Gang(王维刚),et al.Pharmacology and Therapeutics(药理与药物治疗学).Xi′an:The Fourth Military Medical University Press,2006.
[6]Niers T M H,Klerk C P W,DiNisio M,et al.Crit.Rev.Oncol.Hemat.,2007,61:195-207
[7]ZHANG Qing-Mei(张青梅),WANG Jia-Xing(王甲兴).Chin.J.Pract.Tradit.Chin.Med.(Zhonghua Shiyong Zhongxiyi Zazhi),2005,18(15):616-617
[8]JIANGZhen-Ju(蒋珍菊),WANGZhou-Yu(王周玉),etal.Chem.Biol.Eng.(Huaxue Yu Shengwu Gongcheng),2008,12(25):57-59
[9]LIChao(李潮),HUGuo-Dong(胡国栋),HEYan-Hua(何艳花).Chin.J.Proc.Eng.(Guocheng Gongcheng Xuebao),2003,3(1):34-36
[10]LU Xian-Feng(鲁险锋),ZHAO Guo-Liang(赵国樑),GAO Yang(高 扬).China Synth.Fiber Ind.(Hecheng Xianwei Gongye),2005,28(3):13-15
[11]HOU Rui-Xia(侯瑞霞),WENG Ya-Jun(翁亚军),WANG Jin(王 进 ),et al.J.Inorg.Mater.(Wuji Cailiao Xuebao),2007,22(5):996-1000
[12]WANG Xin(汪信),LU Lu-De(陆路德).Chinese J.Inorg.Chem.(Wuji Huaxue Xuebao),2000,16(2):213-217
[13]SHI Hai-Tao(石海涛),MO Xiu-Mei(莫秀梅),HE Chuang-Long(何创龙),et al.J.Clinic.Rehabil.Tissue Eng.Res.(Zhongguo Zuzhi Gongcheng Yanjiu Yu Linchuang Kangfu),2008,12(1):10-14
[14]Osoniyi O,Onajobi F.J.Ethnopharm.,2003,89:101-105
[15]HE Hong(何红),CHE Qing-Ming(车庆明),SUN Qi-Shi(孙启时).Chin.Tradit.Herbal Drugs(Zhongcaoyao),2007,38(5):733-735
[16]ZHONG Shan(钟山),CUI Zheng(崔征),WANG Dong(王东),et al.J.Shenyang Pharm.Univ.(Shengyang Yaoke Daxue Xuebao),2006,23(7):456-458
[17]Tang E J,Cheng G X,Ma X L.Powder Technol.,2006,161:209-214
[18]FAN Niu-Ben(范牛奔),QIAN Yi-Qing(钱翼清),MENG Hai-Bing(孟海兵).J.Nanjing Univ.Chem.Technol.(Nanjing Huagong Daxue Xuebao),2001,23(3):10-13
[19]ZHENG Yu-Ying(郑玉婴),FU Ming-Lian(傅明连),WANG Can-Yao(王灿耀),etal.Spectrosc.Spectr.Anal.(Guangpuxue Yu Guangpu Fenxi),2005,25(11):1810-1812
[20]YUAN Xiao-Fang(袁晓芳),LÜ Zhi-Pin(吕 志 平),LI Fu-Xiang(李福祥),et al.J.Taiyuan Univ.Technol.(Taiyuan Ligong Daxue Xuebao),2002,33(6):660-662
[21]Lei X P,Su Z X.Polym.Adv.Technol.2007,18:472-476
[22]Wang K J,Li H X,Song Y M,et al.Biopolymers,2010,93(10):887-892
[23]SHI Feng(石峰),JI Sheng-Li(姬胜利),CHI Yan-Qing(迟延青),et al.Chin.J.Biochem.Pharm.(Zhongguo Shenghua Yaowu Zazhi),2003,24(2):101-104
[24]KOU Jun-Ping(寇俊萍),LI Jing-Feng(李景峰),YAN Jin(闫瑾),et al.J.China Pharm.Univ.(Zhongguo Yaoke Daxue Xuebao),2003,34(3):257-260
[25]SUN Hai-Yan(孙海燕),CAO Yong-Xiao(曹永孝),LIU Jing(刘静).Chin.J.New Drugs(Zhongguo Xinyao Zazhi),2005,14(8):1001-1003
[26]CAO Ping(曹苹),ZHANG Lin-Sheng(张麟生).Chin.Hosp.Pharm.J.(Zhongguo Yiyuan Yaoxue Zazhi),2001,21(5):280-300
[27]NIE Sheng-Gang(聂升刚),ZUO Li(左丽),SAHO Shi-Chuan(邵世川).Chin.Hosp.Pharm.J.(Zhongguo Yiyuan Yaoxue Zazhi),2002,22(10):639-639
Preparation and Preliminary Study of Anticoagulant Properties of Heparin Hybrid Materials
SONG Yu-Min*,1XIAN Ping1LI Qing-Ping1ZHANG Yu-Mei1MA Xin-Xian1ZHANG Qiang2WANG Yi-Yun2
(1College of Chemistry and Chemical Engineering,Northwest Normal University,Lanzhou 730070,China)(2Gansu Tumer Hospital,Lanzhou 730050,China)
Heparin hybrid materials were obtained by the grafting reaction of heparin and modified metal oxide nanoparticles,which were synthsized by the reaction between the TDIs NCO group and the hydroxyl group on the surface of nano metal oxides,and characterized by infrared spectra,thermogravimetry,scanning electron microscopy (SEM).The anticoagulant effect of hybrid materials were studied by the measurements of coagulation time(CT)and recalcification time (RT).The results showed that nano metal oxides were indeed grafted on the heparin.Compared to heparin,the coagulation time and recalcification time of heparin hybrid materials is shorter,but longer than the corresponding nano metal oxides and control group.In conclusion,the heparin hybrid materials were successfully prepared,and can shorten anti-coagulation time of heparin,prolong anti-coagulation time of nano metal oxides.
TDI;nano metal oxides;heparin;recalcification time;anticoagulant
O614.121;O614.81
:A
:1001-4861(2011)04-0631-06
2010-11-08。收修改稿日期:2010-12-08。
甘肃省自然科学基金(No.0710JRZA108)和甘肃省高分子材料重点实验室资助项目。
*通讯联系人。 E-mail:songym@nwnu.edu.cn,Tel:0931-6169896;会员登记号:S06N8225M1006。
