Aldol缩合反应的立体化学
——Zimmerman-Traxler过渡态
2011-09-26何广武张振琴刘莳姜慧君
何广武 张振琴 刘莳 姜慧君
(南京医科大学药学院 江苏南京 210029)
Aldol缩合反应(即羟醛缩合反应)是一类重要的有机化学反应,由于该反应生成的产物大多是有机合成的重要中间体,因此,一直是有机合成化学的研究热点。Aldol反应除形成新的碳-碳键外,产物中还常常会出现新的手性中心。例如,乙醛在稀碱溶液中发生羟醛缩合反应后,形成一个新的碳-碳键,生成β-羟基丁醛,同时在产物的β-位产生一个手性中心(图1)。
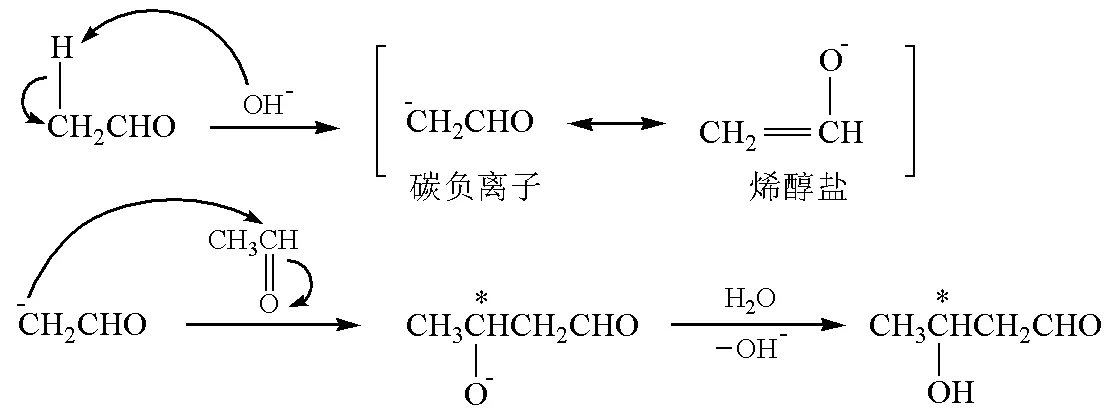
图1 乙醛在稀碱溶液中进行的Aldol缩合反应
在国内现行的有机化学教材中,对Aldol缩合反应中的烯醇盐和羰基的亲核加成反应机理及该反应在有机合成中的应用描述较多,而对Aldol缩合反应中的立体选择性几乎未加以讨论。事实上,当醛的碳原子数≥3时,形成的烯醇盐有Z和E两种不同构型,当它们再与羰基加成后,生成的产物中含有两个手性中心,理论上有4种产物(图2)。
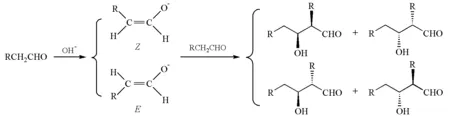
图2 3个碳以上的醛在碱作用下进行的Aldol缩合反应
本文将对上述Aldol缩合反应的立体选择性以及如何控制缩合反应的条件以减少次要产物的生成进行探讨。
1 Zimmerman-Traxler过渡态模型
1957年,美国西北大学的Zimmerman和Traxler为了解释由格式试剂介导的Ivannov及Reformmatsky反应中优势产物的立体化学问题,首先提出了著名的椅式构象的六元环过渡态模型,即后人常称的Zimmerman-Traxler模型[1]。该模型首次从立体化学的角度对Aldol缩合反应进行了剖析,指出烯醇盐构型与产物立体化学之间的对应关系,较好地解释了产物的立体化学特征。随后Dubois[2]、Heathcock[3]、Evans[4]等先后对Aldol缩合反应的立体化学进行了更加深入细致的研究,进一步完善了Aldol缩合反应的立体化学控制技术,实现了高度非对映选择性地合成Aldol缩合产物。
Zimmerman-Traxler 模型如图3所示(能量相等的对映体的过渡态未在图中显示)。当烯醇盐与羰基进行亲核加成时,羰基从垂直角度接近烯醇盐,与烯醇氧键合的金属M(M为碱带入的金属离子)与羰基氧配位,于是两化合物形成了椅式六元环结构的过渡态。若将过渡态中的羰基碳标记为1,烯醇盐的两个碳标记为2和3,则烯醇盐的氧在4位,M在5位,羰基氧在6位;图3中2、3之间原为烯醇盐碳-碳双键,1、6之间原为碳-氧双键。在此过渡态中,有空阻作用的取代基应尽可能采取平伏键状态,这样有利于碳-碳键的生成。
在碱作用下形成的烯醇盐有Z、E两种不同构型,Z型烯醇盐上的R1和R2同时处于六元环过渡态中的竖键,而E型烯醇盐上的R1和R2则是一个位于竖键,一个位于平伏键;对羰基而言,其R可以在竖键上或在平伏键上。在形成的4种环状过渡态中(图3(1)~(4)),过渡态(2)和(4)由于R1和R之间存在着较强的1,3-竖键相互作用,能量较高,不稳定;相比较而言,过渡态(1)和(3)能量较低,容易形成,从而导致相应的立体构型的产物占优势。即E型烯醇盐倾向于生成反式产物,而Z型烯醇盐倾向于生成顺式产物,也就是说烯醇盐的几何构型决定了Aldol缩合产物的立体选择性。

图3 Aldol缩合的Zimmerman-Traxler过渡态模型M为碱带入的金属离子
后来的许多研究表明,Zimmerman-Traxler模型非常成功,根据模型做出的实验设计很好地得到了预期的立体化学结果,成为Aldol缩合反应历史上的第一个理论突破,与后来发现的Mukaiyama羟醛缩合反应和Evans羟醛缩合反应成为控制羟醛缩合反应立体选择性的3大方向之一,在不对称合成中广泛应用。
2 金属离子的影响
在Zimmerman-Traxler 模型中,烯醇盐中的金属阳离子M显著影响着反应的特异性,常见的M可以是Li、K、Mg、Zn、Al、Ti、B、Sn等。反应产物的立体选择性与金属的性质、体积大小密切相关,一般来说,锂和硼,特别是硼,能更好地遵循Zimmerman-Traxler模型。这主要是由于它们的键长明显短于其他金属,如B—C键长为1.4~1.5Å,B—O 键长为1.5~1.6Å,而一般金属—碳键长为1.9~2.2Å,金属—氧键长为2.0~2.2Å。较短的M—O键长使形成的椅式六元环状过渡态结构更加紧密,在图3的过渡态(2)和(4)中,1,3-竖键上的相互空间排斥作用加剧,内能升高,不易生成;而过渡态(1)和(3)相对比较稳定,使Z或E型烯醇盐生成的顺式或反式产物的选择性增大。表1的实验事实也表明,当选用硼化物代替不同结构Z型烯醇盐中的其他金属离子时,Aldol缩合反应有更高的立体选择性,顺式产物的比例明显高于锂[4]。另外,与金属配位的配体L的体积大小及反应条件与产物的立体选择性也密切相关。
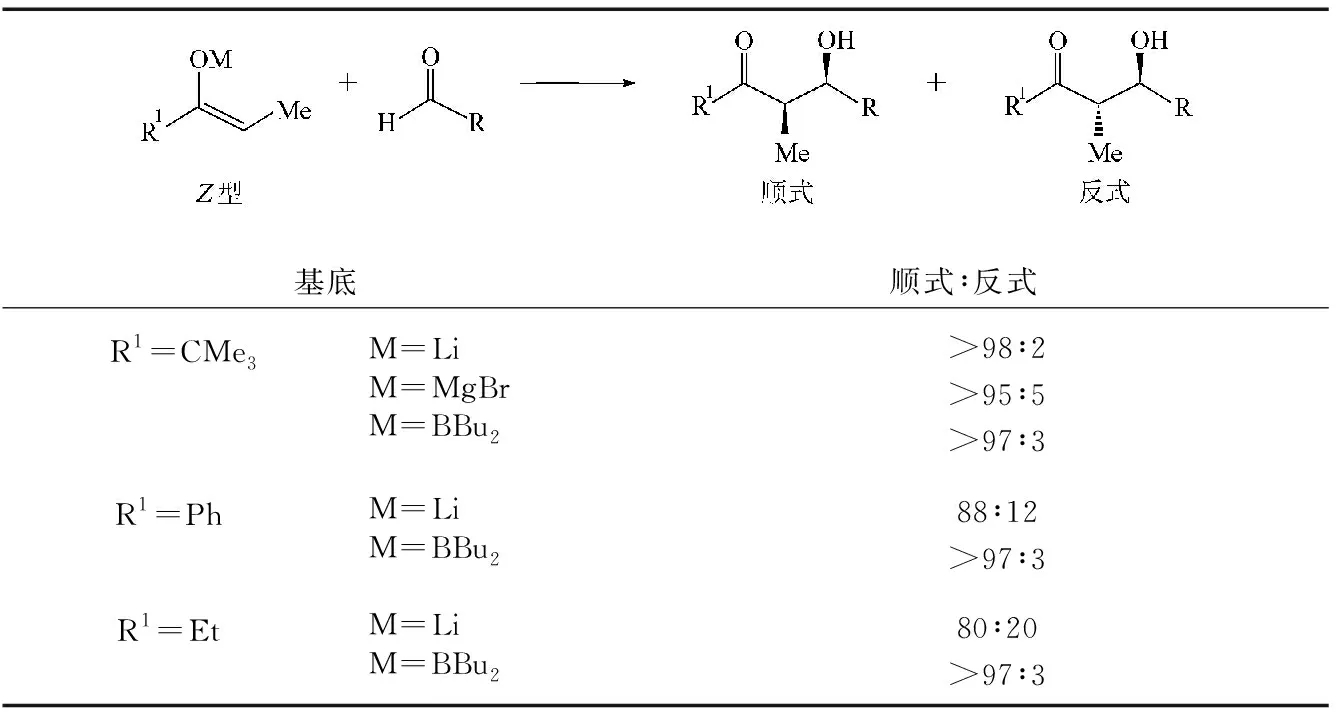
表1 Z型烯醇盐中的金属离子对反应特异性的影响
3 影响烯醇盐Z/E构型的因素
在Aldol缩合反应中,除金属离子的影响外,烯醇盐的顺反异构对羟醛产物的立体化学也有直接的影响,对烯醇盐的结构进行控制,可以获得特定构型的烯醇盐以增加反应的立体选择性。例如,对于酮形成的烯醇锂盐来说,影响其几何构型的因素主要是R1基团的大小,由于空间位阻等作用,大基团有利于形成Z构型的烯醇盐。在表2中,当R1为叔丁基时,过渡态(a)中的R1基团与甲基之间有较强的空间排斥作用;相比较而言,过渡态(b)中的甲基和LDA中的异丙基之间的空间排斥作用较(a)小,因而主要为Z型烯醇盐(约99%),由此主要生成相应的顺式缩合产物。当R1为较小的基团时,过渡态(a)和(b)能量相差不大,得到的烯醇盐为Z、E型混合物,且R1基团越小,所得的E型烯醇盐比例越大[5-6]。当使用较弱的碱如芳香氨基锂(LiNHAr)时,Z型烯醇盐比例较大;而使用空间位阻大的碱(LiTMSNtBu)时,E型烯醇盐比例较大[7]。
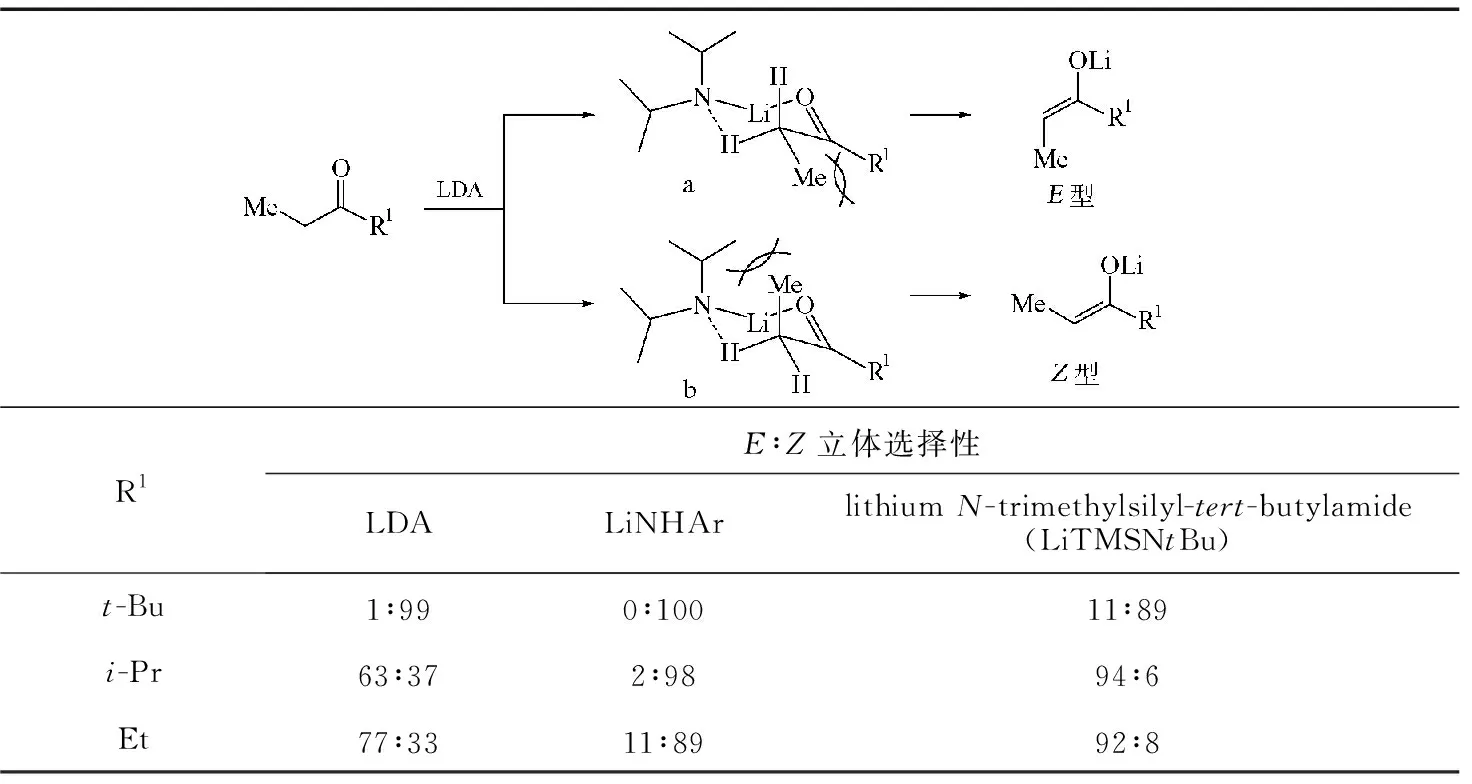
表2 羰基所连基团大小及碱对烯醇盐Z/E构型的影响
对于环己酮,其烯醇盐由于成环的因素只可能为E构型,所以当其与苯甲醛发生Aldol缩合时,得到的主产物为反式产物[7](图4)。

图4 环己酮烯醇盐与苯甲醛进行的Aldol缩合
综上所述,在Aldol缩合中以Zimmerman-Traxler过渡态进行的反应,其立体化学特点为:E型烯醇盐倾向于生成反式产物,而Z型烯醇盐倾向于生成顺式产物。影响Zimmerman-Traxler过渡态模型的主要因素有:①金属烯醇盐的Z/E构型;②烯醇盐与羰基亲核加成中过渡态的空间结构。通过调控烯醇盐的几何构型、金属离子的种类、羰基所连烃基、溶剂及反应条件等,可以提高羟醛缩合反应的立体选择性,拓展Aldol缩合在手性合成中的应用。
[1] Zimmerman H E,Traxler M D.JAmChemSoc,1957,79:1920
[2] Dubois J E,Fellmann P.TetrahedronLett,1975,14:1225
[3] Heathcock C H,Buse C T,Kleschick W A,etal.JOrgChem,1980,45:1066
[4] Evans D A,Nelson J V,Vogel E,etal.JAmChemSoc,1981,103:3099
[5] Narula A S.TetrahedronLett,1981,22:4119
[6] Kleschick W A,Buse C T,Heathcock C H.JAmChemSoc,1977,99:247
[7] Carey F A,Sundberg R J.Advanced Organic Chemistry.Part A:Structure and Mechanisms.5th ed.New York:Springer,2007
