以脱铁蛋白为模板控制合成CoO纳米颗粒*
2011-09-24周金华武小娟安玉良
周金华,袁 霞,武小娟,安玉良
(沈阳理工大学 材料学院 高分子材料研究所,辽宁 沈阳 110168)
以脱铁蛋白为模板控制合成CoO纳米颗粒*
周金华,袁 霞,武小娟,安玉良**
(沈阳理工大学 材料学院 高分子材料研究所,辽宁 沈阳 110168)
提出利用生物模拟化学原位合成纳米颗粒的方法。利用马脾铁蛋白作为限制性反应器控制金属Co离子水解、氧化还原等反应组装成单分散的CoO纳米粒子。在碱性条件下脱铁铁蛋白限制性合成磁性CoO纳米颗粒,通过透射电子显微镜(TEM)和元素分析(EDX)对产品的结构和组成分析表征,颗粒尺寸在3~8nm范围。此外,采用紫外、可见吸收光谱分析对蛋白组装过程进行了实验研究。对基于生物矿化的纳米材料形成机理进行了讨论。
CoO纳米材料;脱铁蛋白;生物矿化组装
Abstract:A novel route was presented for preparing nanoparticles by biosimulation chemical in-situ method.The monodisperse CoO nanoparticles were bio-mineralized by controlling the hydrolysis of metal Co ion and oxidation and reduction reaction with using horse spleen ferritin as controlled reactor.The magnetic CoO nanoparticles were obtained with apoferritin under the condition of alkalescence.The structure and compositions of the products were characterized by TEM and EDX,the particle size was 3~8 nm.In additional,the research on the mineralization process was carried out by UV spectrum.Furthermore,the formation mechanism of nanomaterials based on bio-mineralization was discussed briefly.
Key words:CoO nanoparticles;apoferritin;bio-mineralization
前 言
磁性是物质的基本属性,磁性材料是古老而用途十分广泛的功能材料。纳米磁性材料是20世纪70年代后逐步产生、发展、壮大而成为最富有生命力与宽广应用前景的新型磁性材料[1]。纳米磁性材料的特性不同于常规的磁性材料,其原因是关联于与磁相关的特征物理长度恰好处于纳米量级,例如:磁单畴尺寸、超顺磁性临界尺寸、交换作用长度以及电子平均自由路程等大致处于1~100nm量级,当磁性体的尺寸与这些特征物理长度相当时,就会呈现反常的磁学性质。这些特性使纳米磁性材料在磁流体、靶向药物以及电子器件等领域有着巨大应用潜力[2]。最近人们对于纳米磁性材料CoO的研究兴趣越来越大,有很多方法可以用来合成纳米磁性材料。比较常用的方法有溶胶凝胶法[3]、聚合物还原法[4]、模板法[5]、气相沉积法[6]以及仿生法如硅藻限制性合成纳米硅球[7]等。其中仿生法是一种可靠的、环境友好的纳米材料的合成方法,也是未来纳米技术重要发展方向[8]。在自然界中许多生物组织能够合成纳米材料,如一些特殊植物病毒蛋白分子作为反应模板合成纳米金属材料[9]。
本课题组以生物蛋白超分子为纳米限制性反应器对可控合成无机纳米材料进行了探索性研究。通过模拟生物矿化过程,以脱铁铁蛋白分子成功合成了MnO2纳米材料[10]。本文进一步采用此方法原位合成均一的CoO纳米材料。并通过紫外可见吸收光谱对其矿化过程进行研究。
1 实验部分
1.1 实验用蛋白原料和试剂
实验用蛋白分子为马脾脱铁蛋白(Apoferritin fromhorse spleen in 0.1MNaCl,SIGMA公司);其他所用试剂均为分析纯。
1.2 钴的蛋白矿化组装
取脱铁蛋白 100μL(10-5mmol),加到 5.0mL pH为8.50的Na2B4O7(0.02M)缓冲溶液中,然后加入25 μL Co(NO3)2溶液(0.1M) 和 23μL H2O2溶液(3%),并间隔10 min加入上述当量溶液,如此循环8次,Co/AF(物质的量比)约为2000。上述反应于恒温震荡器中进行,温度为25℃,并保持12h。
1.3 测试分析
采用透射电子显微镜(TEM)对矿化蛋白材料进行观察、分析。将样品溶液直接滴在覆有碳膜的铜网上,晾干后进行电镜分析和EDX(Energy Dispersive X-ray)元素分析。研究所用 TEM为 JEM 2000EX,工作电压100kV;采用紫外、可见(UV-7500)来表征金属离子的蛋白矿化样品,将样品溶液在石英比色皿中进行分析。
2 结果与讨论
在模拟生物条件下,将金属粒子的前驱体材料组装到脱铁蛋白的孔腔内部从而形成粒度均一的纳米粒子,这个过程亦称之为脱铁蛋白的生物模拟矿化。在钴的矿化反应中,加入双氧水后,溶液颜色很快发生变化,经9次循环后,反应溶液由无色转变成褐黄色;有时在实验中会观察到微量絮状沉淀产生,可能是发生非蛋白矿化反应而导致沉淀的生成。TEM研究发现,钴矿化脱铁蛋白的核心是粒度比较均匀的纳米粒子(见图1),从图2颗粒尺寸分布图可以看出多数颗粒介于5~7nm,这一粒度尺寸与蛋白分子的内径相比略小。说明钴的前驱体材料被填充到蛋白材料的内部孔腔中。EDX元素分析证实了锰元素的存在(见图3),说明锰的前驱体材料被填充到蛋白材料的内部孔腔中。
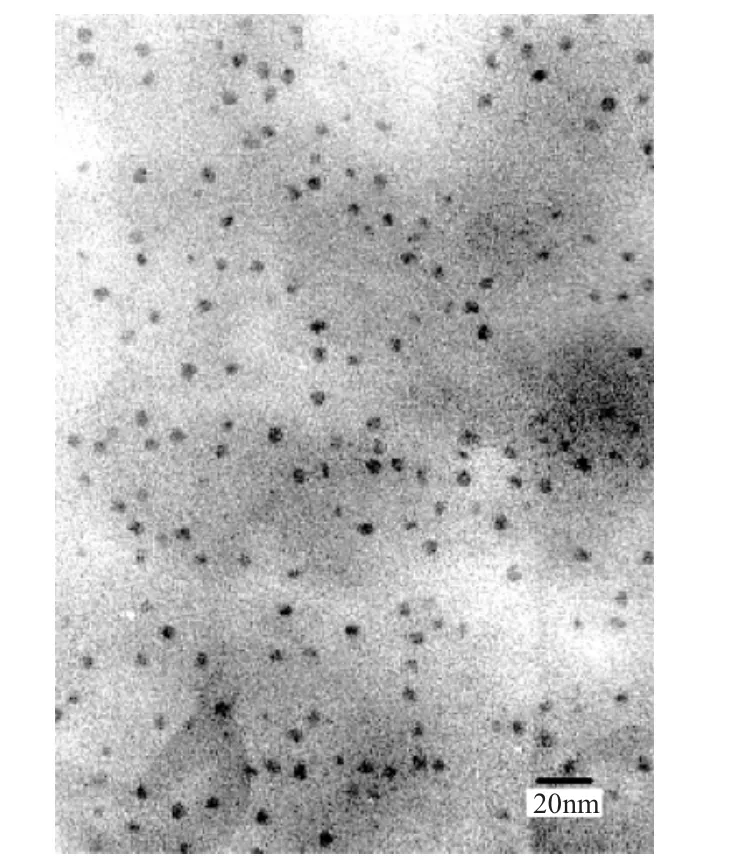
图1 钴矿化脱铁蛋白所得到纳米颗粒的TEM照片Fig.1 TEM images of mineralized apoferritin with cobalt cores
脱铁蛋白矿化组装过程是一种复杂的生物无机化学反应过程,其矿化反应的各种因素控制对其金属离子的组装效果有很大影响。为了考察各个反应因素对蛋白矿化反应的影响,实验中采用紫外可见吸收光谱对其进行分析。由于金属粒子在蛋白内部形成的纳米粒子是以一种水合金属化合物的形式存在,所以在紫外、可见波段会有特种吸收。通过光谱分析,钴的蛋白矿化样品在350nm处有特征吸收。通过考察矿化反应过程中在此特征吸收波长处的吸收度的变化,来评价反应条件的改变对矿化反应的影响。实验通过紫外、可见光谱考察金属离子与蛋白分子物质的量对反应过程的影响。图4是金属钴与脱铁蛋白的物质的量的改变对其紫外可见光吸收的影响。从图中可以看出,随着加入金属物质的量的增加,溶液的的吸光度也随着增加,但当金属/蛋白的物质的量比增加到2000时,溶液的特征吸光度增加程度开始减小,当金属/蛋白的物质的量比达到2200时,溶液的吸收值几乎没有太大的变化。结果表明当金属离子对蛋白分子的物质的量比达到2200时,矿化反应已经达到平衡,生成氧化钴的量已经达到最大量,再加入金属离子没有必要,这个结果和文献中所述的脱铁蛋白所容纳的金属钴的量是一致的[11]。

图2 CoO纳米颗粒的尺寸分布图Fig.2 Size distribution of CoO nanoparticles

图3 钴矿化AF样品的EDX元素分析谱图Fig.3 EDX of Co mineralized apoferritin sample

图4 吸光度随钴物质的量的变化关系Fig.4 The variety of absorbance with molar ratio of Co/AF
金属离子的蛋白矿化组装反应是一种特殊的生物矿化过程。脱铁蛋白是由24个亚单元组成的一种蛋白质分子,是一种结构十分稳定的储存铁的蛋白材料,这些由多肽所组成的亚单元构成了内径为8nm左右的球状空腔结构,能够容纳数千金属原子[12]。在蛋白的矿化组装反应过程中,Co2+是通过蛋白分子之外壳上的孔道进入蛋白分子的空腔内。连接蛋白内侧与外侧的通道有两种,即三重叠通道和四重叠通道。四重叠通道排列有疏水残基,而三重叠通道排列有亲水性的残基,这些贯穿蛋白壳体的亲水性孔道为Co2+的进出提供了通道[13]。在这些孔道内,存在一些活性基,Co2+可与这些活性基进行络合,同时这些活性基进一步将Co2+转移到蛋白空腔内。最后,Co2+和蛋白内部的残基相互作用成核于其空腔内部。蛋白壳体内侧排列有大量的亲水残基,这些内部残基对于络合、氧化和聚集金属离子有决定性的作用。在生物矿化反应过程中,脱铁蛋白内表面的残基组成高密度电荷区和Co2+产生电子静电作用促进矿化核种的形成,之后,Co2+进一步在核种上聚集、成长,直至形成如图1所示的、具有一定大小的纳米粒子。脱铁蛋白的矿化反应是个自催化过程;脱铁蛋白通过内表面的成核基补充静电,这个过程促进Co2+氧化水解反应;这个过程和金属Fe、Mn离子的矿化过程相似,其区别在于矿化过程发生的在不同成核基上。因此,在Co2+的整个矿化组装过程中,蛋白的壳体起到了决定性的作用,整个过程是通过蛋白壳体上有关单元上的各种残基的协同作用完成的[14]。
3 结论
超分子蛋白—脱铁蛋白是一种理想的合成CoO纳米材料的限制性反应的生物模板,蛋白内表面的高电荷密度基为CoO粒子的聚集成核提供前提。透射电镜证实所得到的CoO纳米颗粒尺寸分布与蛋白内径相当;元素分析所得CoO纳米粒子为金属氧化物。超分子蛋白是一种理想的合成无机纳米材料限制反应器,所制备的CoO纳米颗粒具有良好的形状和粒度分布使其在高密度磁盘、磁性共振成像等领域有着广泛的应用。
[1]SASTRY MURALI,AHMAD ABSAR,ISLAM KHAN M,et al.Biosynthesis of metal nanoparticles using fungi and actinomycete[J].Current Scient,2003,85(2):162~170.
[2]GRADY J K,SHAO J,AROSIO P,et al.Vanadyl(IV)binding to mammalian ferritins.An EPR study aided by site-directed mutagenesis[J].J.Inorg.Biochem,2000,80:107.
[3]LIU C,ZHOU B,RODINONE A J,et al.Sol-Gel syntheis of freestanding ferroelectric lead zirconate titanade nanoparticles[J].J.Am.Chem.Sco.,2001,123:4344~4345.
[4]SCOTT D BUNGE,TIMOTHY J BOYLE,THOMAS J Headley.Synthesis of coinage metal nanoparticles from mesityl precursors[J].Nano Letters,2003,3(7):901~905.
[5]RICARDO B AZEVEDO.Synthesis of magnetite nanoparticles in mesoporous copolymer template:a model system for mass loading control[J].Chem.Mater.,2003,15(13):2485~2487.
[6]FLAHAUT E,AGNOLI F,SLOAN J.Connor CO,GreenMLH,CCVD synthesis and Characterization of cobalt-encapsulated nanoparticles[J].Chem.Mater,2002,14:2553~2558.
[7]NILS KROGER,FAINER DEUTZMANN,MANFRED SUMPER.Polycationic Peptides from Diatom Biosilica that direct silica nanosphere formation[J].Science,1999,286:1129~1133.
[8]AHMAD ABSAR,MUKHERJEE PRIYABRATA,SENAPATI SATYAJYOTI,et al.Extracellular biosynthesis of silver nanoparticles using the fungus Fusarium Oxysporum [J].Colloids and Surfaces B:Biointerfaces,2003,28:313~318.
[9]DOUGLAS TREVOR,STRABLE ERICA,WILLITS DBORAH,et al.Protein engineering of a viral cage for constrained nanomaterials synthesis[J].Advanced Materials,2002,14(6):415~418.
[10]张学萍,安玉良,袁霞,等.以生物蛋白为模板控制合成MnO2纳米颗粒[J].化学与黏合,2010,32(2):1~3.
[11]ALLEN M,WILLITS D,YOUNG M,et al.Constrained Synthesis of Cobalt Oxide Nano-Materials In the 12-subunit Protein Cage From Listeria innocua[J].Inorg.Chem.,2003,42:6300~6305.
[12]MELDRUM F C,WADE V J,MANN S.Synthesis of inorganic nanophase materials in supramolecular protein cages[J].Nature,1991,349:684~687.
[13]WARDESKA J G,VIGLIONE B,CHASTEEN N D.Metal ion complexes of apoferritin[J].The Journal of Biological Chemistry,1985,261:6677~6683.
[14]MELDRUM F C,DOUGLAS T,MANN S,et al.Study of the iron content in ferritin,the iron-storage protein[J].Journal of inorganic biochemistry,1995,58:59~68.
Controlled Synthesis of CoO Nano-materials with Using Apoferritin as Template
ZHOU Jin-hua,YUAN Xia,WU Xiao-Juan and AN Yu-liang
(College of Material Science and Engineering,Shenyang Ligong University,Shenyang 110168,China)
TQ 710.6
A
1001-0017(2011)01-0012-03
2010-08-05 *基金项目:辽宁省教育厅青年计划基金(编号:2009A615)和辽宁科技攻关计划(编号:2009222006)。
周金华(1967-),女,吉林省长春人,工程师,研究方向:材料化学及纳米材料研究。
