戊二酸二甲酯水解工艺的研究❋
2011-09-11李秀华
李秀华,范 欣
(华南理工大学化学与化工学院,广东 广州 510641)
0 引 言
戊二酸是一种非常重要的化工原料,广泛运用于化学、建筑、医药、农业等方面,目前市场售价已超过 72000元 /t.目前,商品化戊二酸主要是通过己二酸的产业化生产的副产物混合二元酸经过反复的重结晶工艺获得,工艺复杂,成本高,产品纯度偏低.关于戊二酸制备的研究,目前已有报道的文献有戊二腈碱解酸化法[1],戊二醇催化氧化法[2],环戊烯钨酸催化选择氧化法[3]等.关于戊二酸二甲酯水解制备戊二酸的报道很少,戊二酸二甲酯碱解酸解法制备工艺涉及强酸和强碱,污染严重[4].戊二酸二甲酯的树脂催化水解目前还未见有报道.
目前,在脂肪酯类水解研究报道中较多的是醋酸甲酯水解工艺,具体包括碱解法、酸解法和阳离子交换树脂法.前两种方法由于腐蚀性大、对环境污染大、收率低而较少采用,现在一般是采用阳离子交换树脂法.离子交换树脂具有高效的催化活性和良好的再生性,具有易分离回收,便于化工连续操作,腐蚀性小等优点[5].阳离子交换树脂有 Amberlyst15,SK-1A,GT-175,001×7(732)等,目前已有一些关于离子交换树脂催化水解反应的报导[6-10],其中 001×7(732)阳离子交换树脂因具有交换容量大、廉价等特点而得到广泛的应用[6].本文考察了 001×7型阳离子交换树脂催化水解戊二酸二甲酯制取戊二酸工艺,讨论了各工艺因素对戊二酸水解过程的影响及其规律,并进行了工艺重复性实验,考察了树脂催化剂的寿命,为该技术的工程化、控制过程的优化提供了基础数据.二元酸酯(DBE)是由 3种二价酸酯组成的混合物,包括琥珀酸二甲酯,戊二酸二甲酯和已二酸二甲酯,利用现代精馏技术,DBE可以很容易地得到高纯度的琥珀酸二甲酯、戊二酸二甲酯和已二酸二甲酯等产品.利用本文的技术,可以利用价廉的二元酸酯得到高附加值的戊二酸,不仅无环境污染,而且重复性好,具有良好的应用推广价值.
1 实验部分
1.1 实验试剂及仪器
甲醇,分析纯,广州市东红化工公司;甲苯,分析纯,广东省化学试剂工程技术研究开发中心;乙醇,分析纯,天津市富宇精细化工有限公司;氢氧化钠,分析纯,天津市大茂化学试剂厂;盐酸,纯度36%~ 38%,广东省化学试剂工程技术研究开发中心;001×7强酸性苯乙烯系阳离子交换树脂,广州晶玉水处理材料有限公司;戊二酸二甲酯,工业级,上海嘉辰化工有限公司;DMSO-d6,北京大学大北公司.
上海精密科学仪器有限公司 X-40024758显微熔点仪;日本 HIT ACHI公司 TENSOR 27傅里叶变换红外光谱仪,Bruker Avance 400超导核磁共振仪.
1.2 实验操作
1.2.1 001×7强酸性苯乙烯系阳离子交换树脂的活化
使用前将树脂浸泡在 HCl溶液(4%~ 5%)中,体积比为 1∶1,浸泡时间为 30 min,重复 3次.使用时将树脂转移至去离子水中,树脂与去离子水的体积比为 1∶1,搅拌 1 min后除去水分,重复此过程3次,用滤纸除去表面水份.
1.2.2 戊二酸的制备
反应方程式

根据实验需要准确量取一定体积的去离子水,0.05 mol戊二酸二甲酯和一定量活化后的 001×7强酸性苯乙烯系阳离子交换树脂,置于配有搅拌器和分馏柱的单口圆底烧瓶中.启动搅拌器和油浴锅,并设定油浴温度和转速,当油浴的温度达到指定温度后,记录起始反应时间,同时在反应过程中利用分馏柱不断将甲醇分出;反应进行一定的时间后,停止实验,静置冷却,然后过滤分离树脂.对产品进行滴定分析,并计算反应产率.
1.3 分析方法
采用酸碱滴定法,指示剂为酚酞,通过测量戊二酸的量来计算反应的转化率.将去除树脂的反应产物摇匀后,取一定量的反应产物于 10 mL的容量瓶中,稀释定容.每次用移液管移取 1 mL,加入酚酞指示剂,用氢氧化钠标准溶液滴定至粉红色,15 s内不褪去.记录消耗的碱的体积,并计算得到戊二酸的转化率a. 计算公式如式( 1) 所示.

式中:M为反应产物的总质量,g;m为反应产物取样的质量,g;V为消耗的标准碱液的体积,mL;C为标准碱的摩尔浓度,mol/L;mDMG为戊二酸二甲酯的质量,g;MDM G为戊二酸二甲酯的摩尔质量,g/mol.
1.4 产物的后处理
剩余的溶液经旋转蒸发以除去过量的水.将产品溶于 10 mL乙醇中(55℃时戊二酸在乙醇中溶解度为 262.18 g/L),冷却到 28℃(28.85℃时戊二酸在乙醇中溶解度为 65.38 g/L)[11].由于戊二酸在乙醇中的溶解度随温度的变化较大,因此采用重结晶工艺提纯并干燥后可得纯度较高的戊二酸晶体.
2 实验结果与讨论
2.1 产品结构表征
图1和图 2分别给出了采用本文工艺所得戊二酸的红外和核磁谱图.
由图 1可知,3000~ 3600 cm-1为羧基的 -OH伸缩振动峰,2984 cm-1处为 C-H伸缩振动峰,1700 cm-1处为羧基 C=O的强吸收峰,1411 cm-1处为 -CH2-的弯曲振动强吸收峰,与戊二酸的标准谱图(NIST谱图库 COBLENTZ NO.10164)完全一致.
图2为1H NMR(DM SO-d6,400 M Hz),W:1.66(m,2H,CH2),W:2.24(t,4H,CH2COOH),W:12.08(s,2H,COOH),在W:2.52和W:3.42处分别是溶剂峰和水峰,无其他杂质峰.1H NMR测试结果与戊二酸的结构非常吻合,且所得戊二酸的纯度非常高.本文工艺所得戊二酸的 m.p.97~98℃,融程很窄,进一步说明戊二酸的纯度非常高.

图1 戊二酸红外谱图Fig.1 IR spectrum of glutaric acid
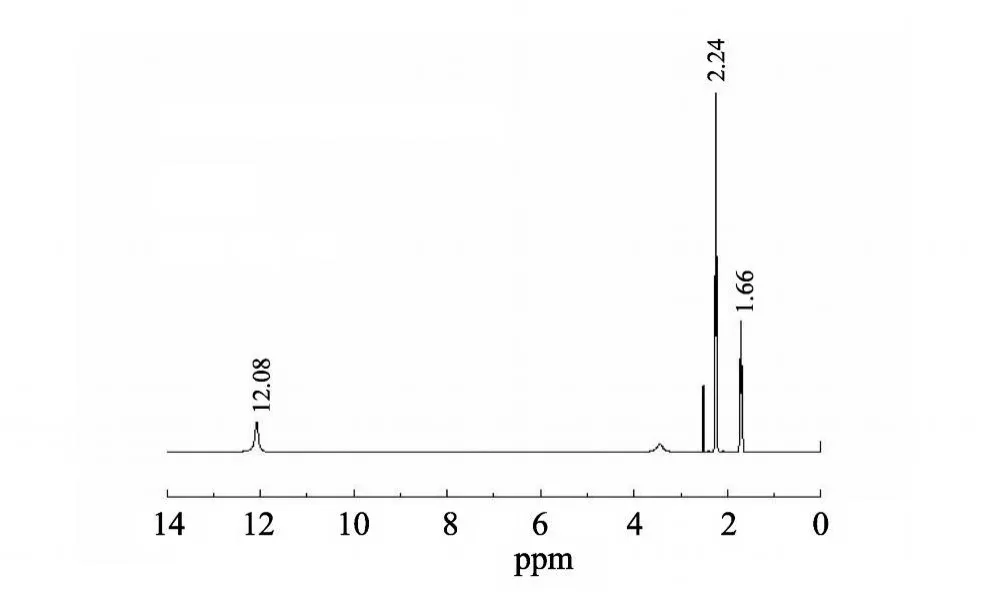
图2 戊二酸核磁谱图Fig.2 1HNM R spectrum of glutaric acid
2.2.1 正交试验设计及结果分析
戊二酸收率是衡量本论文水解工艺的重要参数.影响水解反应的因素主要有树脂浓度(A)、反应温度(B)、反应时间(C)和水酯比(D).本文利用 L9(34)正交表设计了 001×7型阳离子交换树脂催化水解戊二酸二甲酯制取戊二酸的正交试验,表1给出了各反应因素的水平参数,正交试验结果列入表 2.参照文献 [12]对戊二酸的收率利用软件进行极差分析,得到4个因素不同水平对应的产率均值,产率均值越大,该因素水平越有利.选出各因素对应的最佳水平,将其结合在一起,得到全体水平组合中关于戊二酸收率的可能的最佳水平组合.表 2最下一行的列极差是各因素对反应的影响程度,极差大的因素是较重要的因素,极差小的因素则对戊二酸的产率影响较小.很显然,对本文的工艺而言,反应温度对产率的影响作用是最大的,其次是反应时间,再次是水酯比,最后是树脂浓度.在此基础上进一步优化了各因素的反应条件.
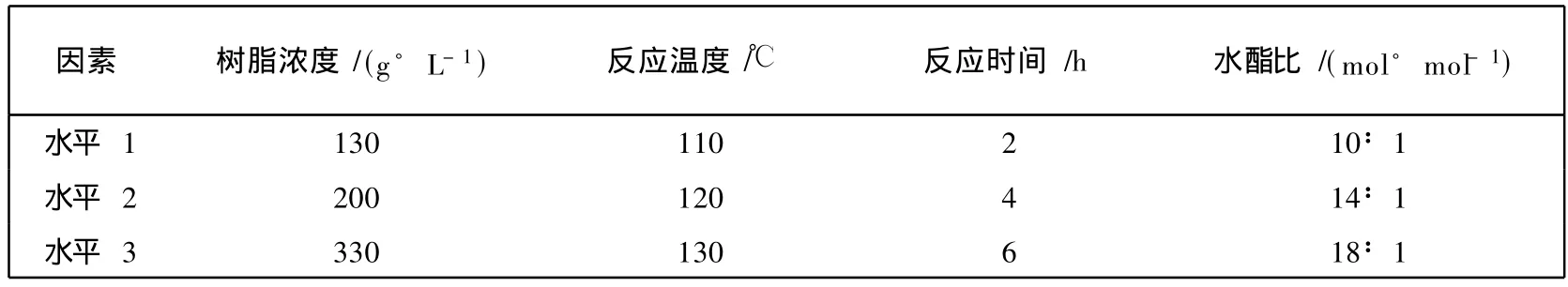
表1 正交试验因素水平表Tab.1 Factor levels of designed o rthogonal test
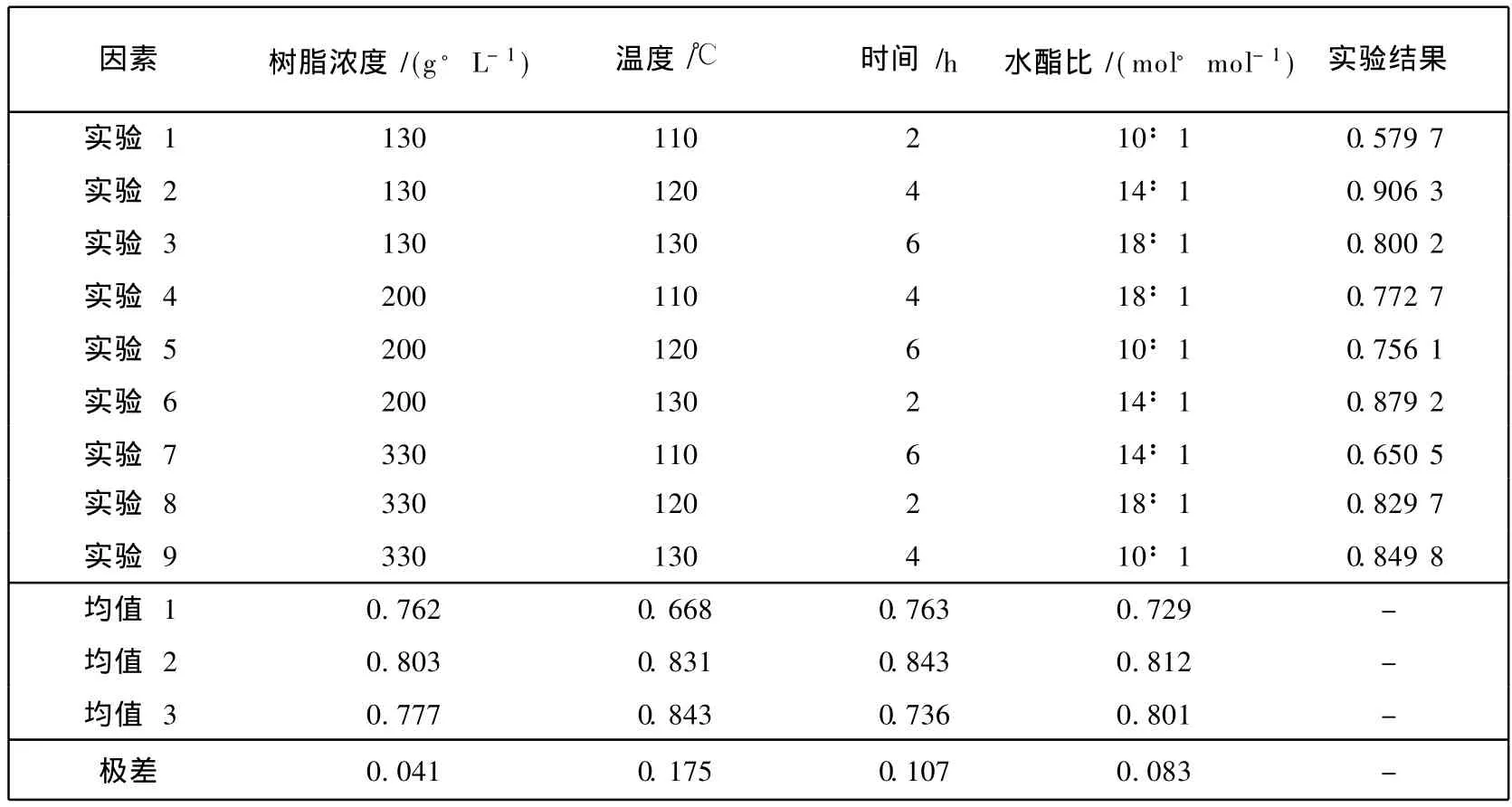
表2 L9(34)正交试验结果Tab.2 Results of designed L9(34)orthogonal test
2.2.2 温度的选择
戊二酸二甲酯的水解反应是一个吸热的可逆反应,反应温度的升高有利于提高反应程度和反应速率,因此酯的水解反应通常在较高的温度下进行.但由于阳离子交换树脂对温度非常敏感,特别是温度超过 107℃时,磺酸基团较易从树脂上脱离,导致催化剂变性.依据 001×7强酸性苯乙烯系阳离子交换树脂的性能指标,其最高使用温度为 100℃.考虑到本反应体系是采用分流回流的方式不断去除反应生成的甲醇,促使反应向正反应方向进行,故必须有足够的热能来保证反应的速度和程度.本文采用正交试验考察了 110~ 130℃这 3个环境温度,正交试验结果证明温度越高,试验收率越高.据此在保持其他因素为水平 2的情形下,本文将环境油浴温度升至 140℃,结果表明:虽然戊二酸的收率可以达到88.2%,但是此时反应体系的温度为 110℃,超过了 001×7强酸性苯乙烯系阳离子交换树脂的最高使用温度,造成树脂破损严重.而当油浴温度为 130℃时,反应液达到恒沸且回流稳定,用温度计测量反应体系的温度为 100℃,符合 001×7强酸性苯乙烯系阳离子交换树脂长期使用的温度要求.所以油浴温度选择 130℃是最为合适的.
2.2.3 反应时间对产率的影响
本文在油浴温度为 130℃,树脂浓度为 200 g/L,水酯比为 14∶1的条件下了探索戊二酸产率随反应时间的变化情况,研究结果如图 3所示.很显然,在反应时间为 2h时,戊二酸的产率达到最高,反应时间太短和过长都不利于戊二酸产率的提高.由于戊二酸二甲酯的水解反应是可逆反应,虽然分馏出的副产物甲醇已尽可能地提高正反应,但反应时间太短,戊二酸二甲酯不能够充分水解,戊二酸产率不理想,随着时间的增长,产率达到最高点;在反应后期,由于反应已进行到一定程度后,生成的甲醇较少,难以通过分馏柱从体系中完全分离出来,而且前期生成的戊二酸的积累达到了一定的浓度,这两个因素使得反应向逆反应方向进行,使戊二酸产率随着反应时间的延长出现先升高、而后降低的趋势.

图3 戊二酸收率随反应时间的变化曲线图Fig.3 Relationship of g lutaric acid yield and reaction time
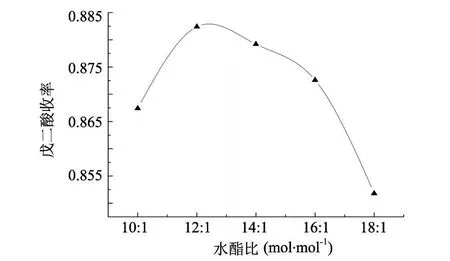
图4 戊二酸收率随水酯比的变化曲线图Fig.4 Relationship of glutaric acid yield and molar ratio of water to dimethyl glutarate
2.2.4 水酯比对产率的影响
对于可逆反应来说,增大其中一种反应物的浓度,就会使得单位体积内反应物分子互相碰撞的机会增多,就可以促使反应向正反应方向进行.在油浴温度为 130℃,树脂浓度为 200 g/L,时间为 2 h的情况下,本文研究了戊二酸产率随水酯比的变化情况,研究结果如图 4所示.由图 4可知,戊二酸产率随水酯比的增大出现先升高、后降低的趋势,当水酯比为 12∶1时,戊二酸产率为最高.其原因在于在水酯比较大时,水很容易吸附在树脂活性部位[13],随着水量的增加,催化活性降低.另外,随着水酯比的增大,后续分离工艺耗能高、花费大,在工业应用中,应考虑使用最佳的水酯比.
2.2.5 树脂浓度对产率的影响
在油浴温度为 130℃,水酯比为 12∶1,时间为 2 h的情况下,本文研究了戊二酸产率随树脂浓度的变化情况,研究结果如图 5所示.由图 5可知,随着树脂浓度的增加,收率开始呈上升趋势,当催化剂的浓度为 170 g/L时,收率最高,达 88.84%;再增加催化剂的浓度,收率反而会下降.这主要是因为当催化剂浓度较低时,单位体积内的活化分子数目较少,导致反应速率低,不能完全催化水解;当催化剂浓度较高时,在同等搅拌强度下,非均相体系随着固含量的增大,搅拌的效果变差,使得反应介质和催化剂的有效接触机会减少,导致收率下降.

图5 戊二酸收率随树脂浓度的变化曲线图Fig.5 Relationship of g lutaric acid yield and varying catalyst loadings
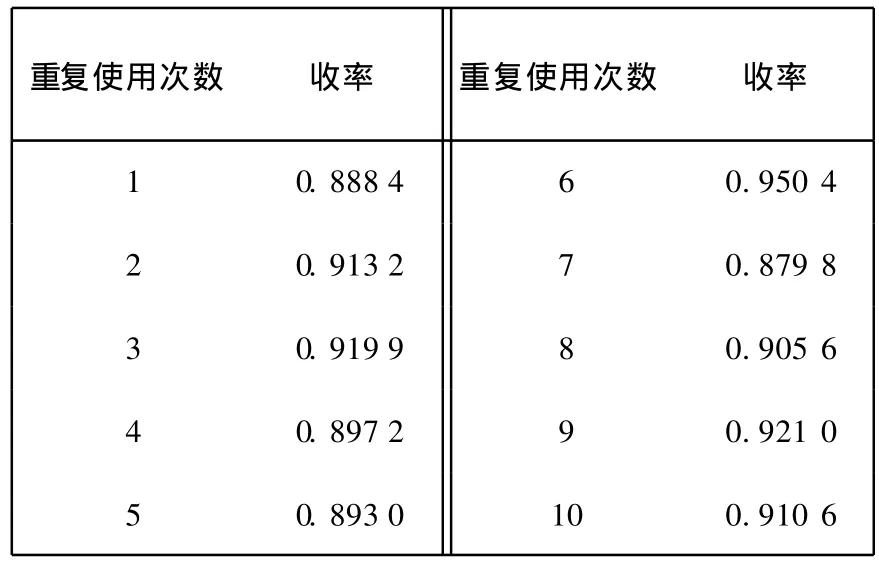
表3 重复使用催化剂实验结果Tab.3 Repeated tests of reuse catalyst
2.2.6 催化剂的重复使用
根据以上实验,筛选出的 001×7型阳离子交换树脂催化水解戊二酸二甲酯制取戊二酸的最佳工艺条件如下:油浴温度为 130℃,水酯比为 12∶1,时间为 2 h,催化剂浓度为 170 g/L.为验证阳离子树脂催化剂的充分利用稳定性,在同等的实验条件下用同一催化剂进行了重复实验 10次,实验结果如表 3所示.从表 3可以看出,戊二酸的产率在 87%~ 95% 之间,且催化剂破损不多,可以应用在工业大规模生产中.
3 结论与展望
1)反应温度是影响戊二酸二甲酯水解工艺的重要因素,温度太高树脂容易失活,粉末化;而温度太低不利于甲醇从体系中分离出来.
2)戊二酸二甲酯水解工艺制备戊二酸的最佳工艺条件为:温度为 130℃,水酯比为 12∶1,时间为2 h,催化剂浓度为 170 g/L.此时收率最高,可达到 88.84%.
3)催化剂 001×7树脂在本文筛选的工艺条件下可以多次使用,催化性能及物质形态稳定,具有良好的重复性.本文工艺路线简单,重复性好,对环境无污染,而且原料价格低廉,有望应用在大规模工业生产中.
[1]Poldy Jacqueline,Peakall Rod,BarrowRussell A.Pheromones and analogs from Neozeleboria wasps and the orchids that seduce them:A versatile synthesis of2,5-dialkylated1,3-cyclohexanediones[J].Tetrahedron Letters,2008,49(15):2446-2449.
[2]Chen Hui,Dai Weilin,Gao Ruihua,et al.New green catalytic manufacture of glutaric acid from the oxidation of cyclopentane-1,2-diol with aqueous hydrogen peroxide[J].Applied Catalysis,A:General,2007,328(2):226-236.
[3]戴维林,曹勇,范康年.环境友好催化氧化环戊烯大规模合成戊二酸的方法:中国,CN20061903823[P],2007-01-31.
[4]Niwayama Satomi,Rimkus Audrius.Effects of counter cations in selective monohydrolyses of symmetric diesters[J].Bulletin of the Chemical Society of Japan,2005,78(3):498-500.
[5]张红梅,魏文珑,常宏宏.阳离子交换树脂催化水解法制备丙二酸工艺的研究[J].应用化工,2007(7):653-655.Zhang Hongmei,Wei Wenlong,Chang Honghong.Study on the preparation process of malonic acid catalyzing by cation exchange resin[J].Applied Chemical Industry,2007(7):653-655.(in Chinese)
[6]刘跃进,朱福勇,韩路长,等.001×7(732)阳离子交换树脂催化醋酸甲酯水解反应过程模拟与优化[J].化工学报,2007(10):2513-2516. Liu Yuejin,Zhu Fuyong,Han Luchang,et al.Simulation and optimization of methyl acetate catalytic hydrolysis with 001× 7(732)cation-exchange resin[J].Journal of Chemical Industry and Engineering,2007(10):2513-2516.(in Chinese)
[7]李菊梅,夏代宽.阳离子交换树脂催化水解乙酸甲酯的动力学研究[J].石化技术与应用,2002,20(6):378-381.Li Jumei,Xia Daikuan.Kinetie model for the hydrolysis of Methyl acetate in the Presence of cation-exchange resin[J].Petrochemical Technology&Application,2002,20(6):378-381.(in Chinese)
[8]权霞,陈晓晖,魏可镁.NKC-9离子交换树脂催化醋酸甲酯水解动力学研究[J].工业催化,2006,14(10):31-35.Quan Xia,Chen Xiahui,Wei Kemei.Kinetics of the hydrolysis of methyl acetate catalyzed by NKC-9cationexchange resin[J].Industrial Catalysis,2006,14(10):31-35.(in Chinese)
[9]陈海波,吴巍,叶岗,等.醋酸甲酯水解的反应动力学[J].工业催化,2005,13(9):36-40.Chen Haibo,Wu Wei,Ye Gang,et al.The kinetics for hydrolysis of methyl acetate over ammonium heteropoly acids[J].Industrial Catalysis,2005,13(9):36-40.(in Chinese)
[10]Delgado P,Sanz M,Beltr′an S.Kinetic study for esterification of lactic acid with ethanol and hydrolysis of ethyl lactate using an ion-exchange resin catalyst[J].Chemical Engineering Journal,2007,126:111-118.
[11]孙晓波,任珂,毛治博,等.戊二酸溶解度的测定与关联 [J].华东理工大学学报(自然科学版),2007,33(5):629-632.Sun Xiaobo,Ren Ke,Mao Zhibo,et al.Measurement and correlation of solubilities of glutaric acid in different solvents[J].Journal of East China University of Science and Technology(Natural Science Edition),2007,33(5):629-632.(in Chinese)
[12]吴有炜.实验设计与数据处理[M].苏州:苏州大学出版社,2002:87-92.
[13]Zhang Y,Ma L,Yang J C.Kinetics of esterification of lactic acid with ethanol catalyzed by cation-exchange resins[J].Reactive&Functional Polymers,2004,61:101-114.
