I2/KI溶液同时脱硫脱硝的试验研究
2011-06-23韩粉女
韩粉女, 钟 秦
(1.南京理工大学化工学院,南京210094;2.盐城工学院化学与生物工程学院,盐城224051)
我国是世界上少数几个以煤为主要能源的大 国.全世界一次能源消费结构中煤炭仅占26.7%,而我国燃煤量在一次能源消费中占70%左右,到2050年亦将占60%左右[1].煤炭燃烧产生的SO2和NOx是形成“酸雨”和“酸雾”的主要原因之一.我国目前的烟气污染控制主要集中在SO2的排放控制上,随着环境污染的加重以及空气质量要求的提高,NOx的控制和治理已被提上日程.
湿法烟气脱硫是最有效的脱硫技术,与其他脱硫技术相比,其成本低、操作简单且脱硫效率高,因此湿法烟气脱硫技术被广泛应用.尽管目前单独脱硫脱硝的商业应用很成功,但考虑到成本投入、操作费用以及设备占地面积等,人们开始将研究重点放在一个设备装置同时脱硫脱硝上[2-3],因此开发与湿法脱硫相结合的湿法协同脱硝技术具有广阔的工业应用前景.当前,国内外已有大量的采用氧化吸收法同时脱硫脱硝的研究报道[4-5],但同时脱硫脱硝技术大多数在研究阶段,尚未得到大规模工业应用.碘在酸性条件下有很强的氧化性,能够将NO氧化成,且I—可以通过电解生成,实现的回收利用,同时降低吸收液的二次污染.
综合上述原因,笔者应用I2/KI溶液对模拟烟气中SO2和NO进行了同时脱硫脱硝的试验研究.
1 试验部分
1.1 试验流程
将压缩氧气、压缩高纯氮、压缩NO及压缩SO2气体通过减压阀后,按一定量配比混合,使NO以及以一定配比制成模拟烟气,并用加热带保证烟气温度为55~60℃.试验反应装置见图1.气体从钢瓶经减压阀送出,由气体调节阀控制流量,反应温度由恒温水浴锅控制.吸收液的pH值通过0.1 mol/L的NaOH或柠檬酸进行调节,模拟烟气通过装有吸收剂的鼓泡反应器后经尾气吸收瓶吸收后排放.烟气吸收系统主要由鼓泡反应器和恒温水浴锅组成:自行设计鼓泡反应器体积为500 mL,吸收液量为250 mL,进气管插入反应器底部,其下部装有直径为10cm的玻砂板,以保证气泡稳定均匀,出气管位于液面上方.
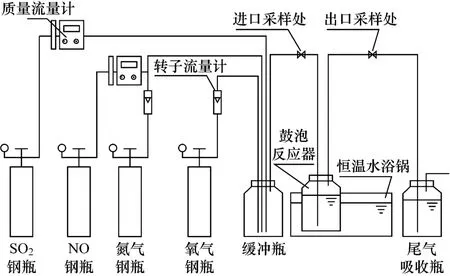
图1 试验装置示意图Fig.1 Schematic diagram of the experimental apparatus
1.2 仪器和装置
试验中所使用的试剂全部为分析纯,O2、N2以及SO2的纯度均为99.99%;NO体积分数为5%(其余为N2).主要仪器和装置有:鼓泡反应器,NOVA 2000烟气分析仪,ICS-90离子色谱仪.
1.3 分析方法
待系统稳定运行后,在总的反应时间25 min内,每隔5 min用烟气分析仪测定试验中每组进出口烟气的SO2和NO体积分数.SO2和NO的去除率即脱硫率(DS)、脱硝率(DN)的计算如下:
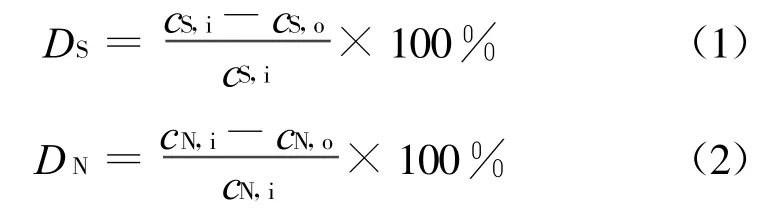
2 试验结果与讨论
2.1 I2浓度对脱硫脱硝率的影响
常压条件下,模拟烟气的气体流量为1 L/min,气相中 φ(O2)为 6%,φ(SO2)为0.09%,φ(NO)为0.08%,反应温度为25℃,考察不同I2物质的量浓度对脱硫脱硝率的影响.试验结果见图2.
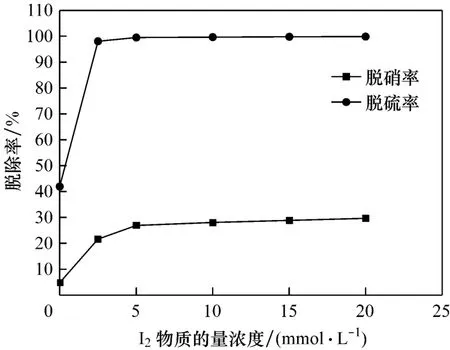
图2 I2物质的量浓度对脱除率的影响Fig.2 Effect of I2concentration on the removal efficiency
从图2中可以看出,随着I2物质的量浓度增大,脱硫脱硝率逐渐增大.这是由于氧化剂I2可以氧化SO2和NO,I2对SO2和NO的氧化方程式为:
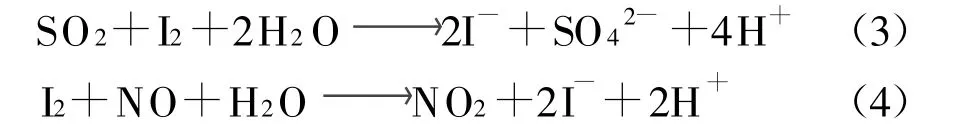
生成的NO2可以继续转变为其他易溶于水的氮氧化合物[6]:
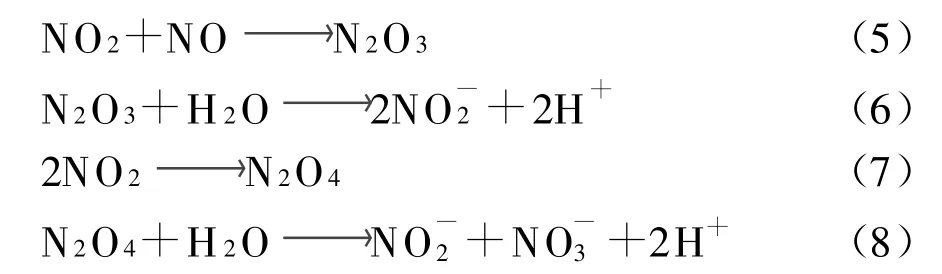
从而增大了脱硫脱硝率.而当I2物质的量浓度达到5 mmol/L时,继续增大c(I2),脱硫脱硝率只是略微增长.这可能是由于在25 min的反应时间内最多需要 1.3 mmol的 I2,当c(I2)达到 5 mmol/L后,氧化剂开始过量,对于SO2和NO的氧化促进作用就变小了.
2.2 Fe3+物质的量浓度对脱硫脱硝率的影响
常压条件下,模拟烟气的气体流量为1 L/min,气相中 φ(O2)为 6%,φ(SO2)为 0.09%,φ(NO)为0.08%,c(I2)为5 mmol/L,反应温度为25℃时,考察不同Fe3+(硫酸铁)物质的量浓度对脱硫脱硝率的影响,试验结果见图3.
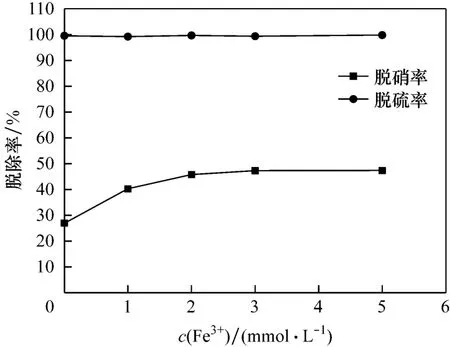
图3 Fe3+物质的量浓度对脱除率的影响Fig.3 Effect of Fe3+concentration on the removal efficiency
由图3中可以看出,随着c(Fe3+)增大,脱硫率变化不明显.这是因为在无催化剂的情况下脱硫率已经达到 99%以上,不能明显看出脱硫率的再提高,但有研究表明Fe3+可以提高脱硫率[7].随着c(Fe3+)增大,脱硝率快速升高,但当c(Fe3+)超过2 mmol/L时,脱硝率增长速度减缓.这表明Fe3+的存在能够促进NO的氧化和吸收,Christian等[8]的研究表明Fe3+本身也是一种氧化剂,它有利于NO的氧化,从而促进NO的吸收.
2.3 吸收溶液初始pH值对脱硫脱硝率的影响
常压条件下,模拟烟气的气体流量为1 L/min,气相中 φ(O2)为 6%,φ(SO2)为 0.09%,φ(NO)为0.08%,c(I2)为5 mmol/L,c(Fe3+)为 2 mmol/L,反应温度为25℃时,用NaOH调节pH值,考察不同pH值对脱硫脱硝率的影响,试验结果见图4.
由图4可见,初始pH值的变化对脱硫率脱硝率的影响并不是所预想的随着pH值增大,脱硫脱硝率升高.这是因为pH值的增大有利于SO2及NOx的吸收,但同时pH值增大会降低 I2的氧化性,两者同时作用使得pH值的变化对脱硫率脱硝率的影响并不显著.
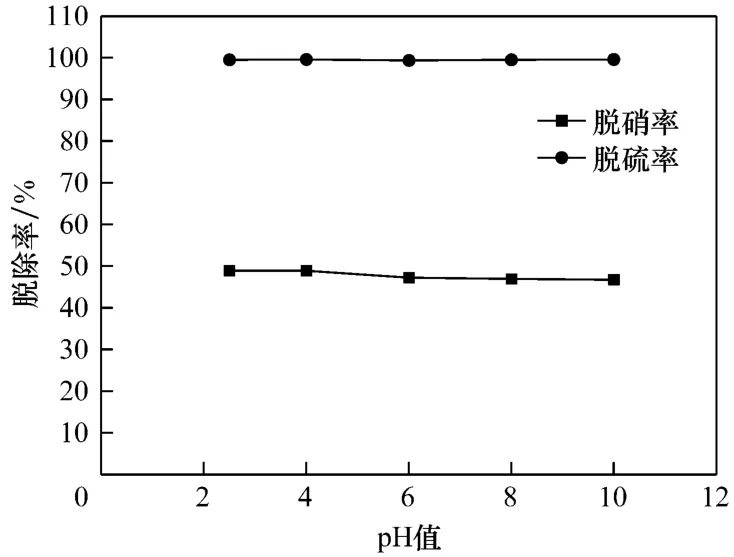
图4 初始pH值对脱除效率的影响Fig.4 Effect of initial pH value of absorbent solution on the removal efficiency
2.4 反应温度对脱硫脱硝率的影响
在常压条件下,模拟烟气气体流量为1 L/min,气相中 φ(O2)为 6%,φ(SO2)为0.09%,φ(NO)为0.08%,I2物质的量浓度为5mmol/L,Fe3+物质的量浓度为2 mmol/L时,考察不同反应温度对脱硫脱硝率的影响,试验结果见图5.
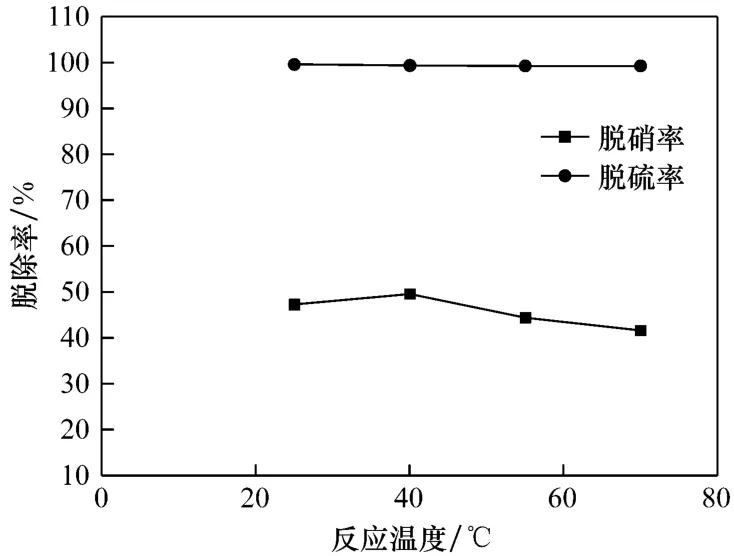
图5 反应温度对脱除率的影响Fig.5 Effect of reaction temperature on the removal efficiency
由图5可知,在试验温度范围内,随着温度升高,SO2吸收率基本不变.但在25~40℃时,NO的脱除率随着温度升高而增加,40℃时出现拐点,温度大于40℃后,NO的脱除率随着温度升高而略微降低.这种现象可以解释为,反应温度的升高可提高I2溶液的氧化活性,使NO的氧化率增大,从而增大了脱硝率;但另一方面温度继续升高对气体的吸收不利.温度升高的双重作用使得脱硝率在40℃出现一个最大值.
2.5 气相中O2体积分数对脱硫脱硝率的影响
在常压条件下,模拟烟气气体流量为1 L/min,φ(SO2)为 0.09%,φ(NO)为 0.08%,c(I2)为 5 mmol/L,c(Fe3+)为2 mmol/L,反应温度为40℃时,考察O2体积分数对脱硫脱硝率的影响,试验结果见图6.
由图6可以看出,烟气中 φ(O2)对脱硫率几乎没有影响.这是由于虽然氧气会和烟气中SO2发生氧化反应但由于在无氧情况下脱硫率已经超过99%,因而增加φ(O2)对脱硫率的提高作用不是很明显.但烟气中φ(O2)对脱硝率的影响比较大,当烟气中不存在O2时,脱硝率非常低;在有O2存在的条件下,脱硝率明显增大,且随着 φ(O2)增大,脱硝率缓慢增大.这是因为在无O2的情况下,NO的氧化仅仅靠氧化剂I2;当有O2存在时,O2可以氧化部分NO:2NO+增大了NO的氧化率,进而提高了脱硝率.但 φ(O2)为 3%时已过量,继续增大 φ(O2)对NO氧化率的影响不是太大.
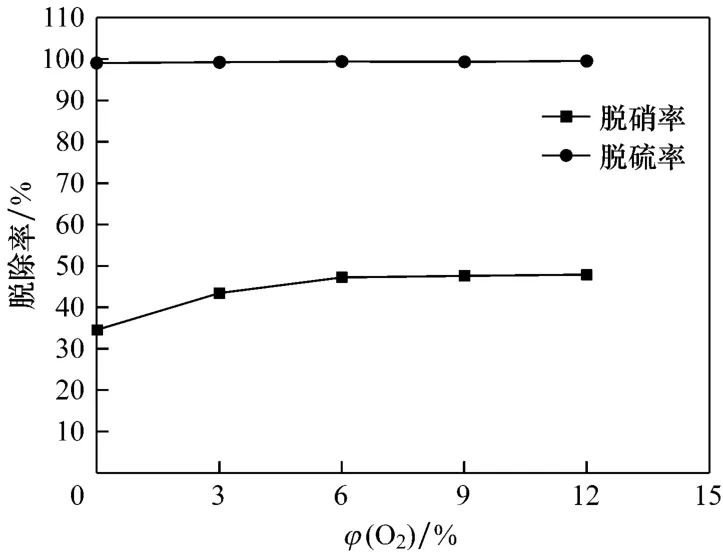
图6 烟气中O2体积分数对脱除率的影响Fig.6 Effect of O2concentration on the removal efficiency
2.6 NO体积分数对脱硫脱硝率的影响
在常压条件下,模拟烟气气体流量为1 L/min,气相中 φ(O2)为 6%,φ(SO2)为0.09%,I2物质的量浓度为5 mmol/L,Fe3+物质的量浓度为2 mmol/L,反应温度为40℃时,考察不同NO体积分数对脱硫脱硝率的影响,试验结果见图7.
从图7可以看出,在本试验中NO体积分数增大对脱硫率的提高不是很明显.这是由于高φ(NO)的吸收降低了吸收剂的pH值,增强了吸收剂的氧化性,增大了脱硫率,但同时pH值的下降又不利于脱硫,两方面的作用使得脱硫率的变化不是很大.但φ(NO)的增大有助于脱硝率的提高,其原因可能是虽然高浓度NO的吸收降低了吸收剂的pH值,不利于脱硝,但由于 φ(NO)的增加增大了传质推动力,提高了NO传质速率,促使反应式(4)向右进行,从而增大了脱硝率;同时吸收剂pH值的下降增强了吸收剂的氧化性,增大了脱硝率.φ(NO)的增加对脱硝率的促进作用大于阻碍作用,从而表现出的脱硝率提高.
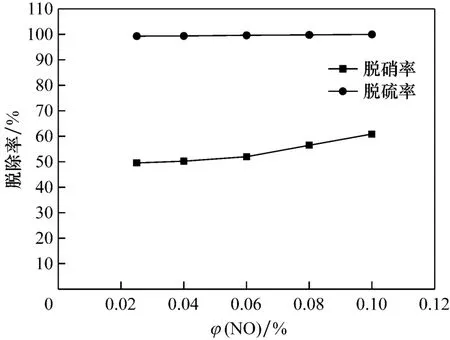
图7 烟气中NO体积分数对脱除率的影响Fig.7 Effect of NO concentration on the removal efficiency
2.7 SO2体积分数对脱硫脱硝率的影响
在常压条件下,模拟烟气气体流量为1 L/min,气相中 φ(O2)为 6%,φ(NO)为 0.1%,c(I2)为 5 mmol/L,c(Fe3+)为2 mmol/L,反应温度为40℃时,考察φ(SO2)对脱硫脱硝率的影响,试验结果见图8.
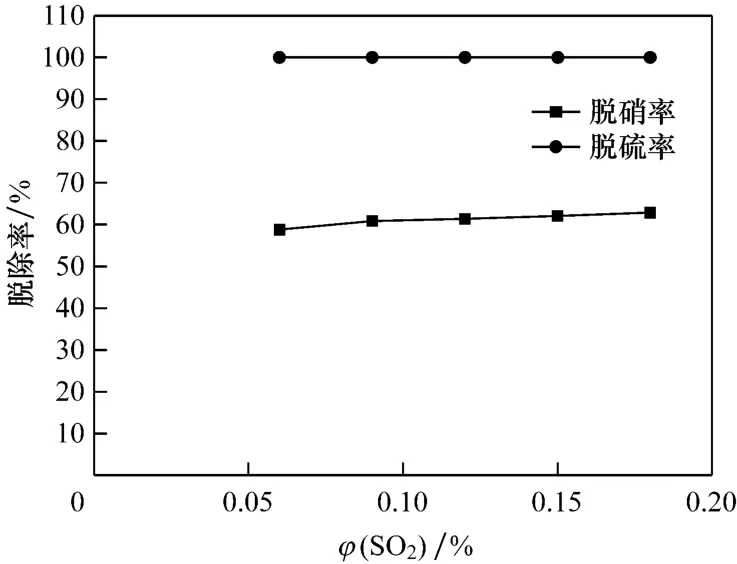
图8 烟气中SO2体积分数对脱除率的影响Fig.8 Effect of SO2concentration on the removal efficiency
从图8可以看出,模拟烟气中SO2体积分数对脱硫率几乎没有影响,脱硫率一直保持在100%.这是因为SO2体积分数的增加使其在气相中的分压增大,加大了SO2传质速率,因而SO2的相界面通过率增大,促使反应式(3)和向右进行,从而增大了脱硫率.另外SO2体积分数增大能够降低pH值,使氧化剂的氧化性提高,从而增大SO2氧化率;但pH值的降低不利于SO2的吸收.因此SO2体积分数对脱硫率几乎没有影响.但随着φ(SO2)的增大NO的脱除率逐渐增大.这是由于φ(SO2)的增大能够降低pH值,使氧化剂的氧化性增大,从而提高NO的氧化率;另外中间产物HSO-3的生成可以促进NO2的吸收.但I2可以将亚硫酸根离子氧化成硫酸根离子,方程式为:
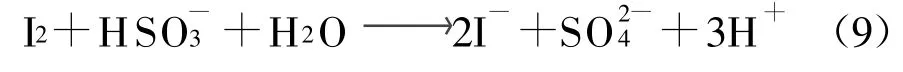
这样就降低了 HSO-3对脱硝率的影响,同时pH值的降低不利于NO2的吸收,因此脱硝率增长幅度不大,这跟Deshwal[9]的研究结果一致.
2.8 烟气流量对脱硫脱硝率的影响
在常压条件下,气相中 φ(O2)为6%,φ(SO2)为0.09%,φ(NO)为 0.1%,c(I2)为 5 mmol/L,c(Fe3+)为2 mmol/L,反应温度为 40℃时,考察烟气流量对脱硫脱硝率的影响,试验结果见图9.
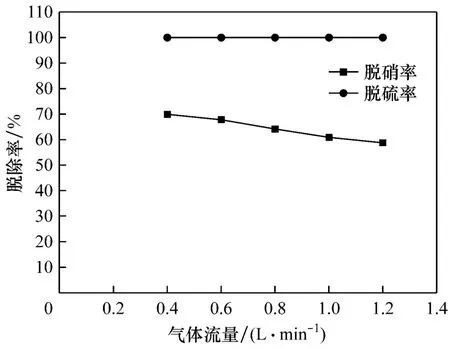
图9 烟气流量对脱除率的影响Fig.9 Effect of flow rate of flue gas on the removal efficiency
由图9可以看出,烟气流量对脱硫率几乎没有影响,脱硫率一直保持在100%;但对脱硝率影响显著,随着烟气流量的增大脱硝率逐渐减小.这主要是由于NO是难溶气体,气液传质则主要由液膜控制,烟气流量增大,NO在溶液中的停留时间减少,NO的相界面通过率就减少,这样气液接触的NO减少,从而降低了脱硝率;而SO2为中等溶解度的气体,气液传质则主要由液膜和气膜共同控制,烟气流量增大,虽然SO2在溶液中的停留时间减少,但由于气膜阻力减小,总传质阻力降低,因而SO2的相界面通过率变化不大,脱硫率几乎不变.当烟气流量为0.4 L/min时,脱硝率达69.9%.
3 结 论
(1)烟气中SO2极易被脱除.由于在试验条件下SO2脱除率均大于99%,操作工艺条件变化对脱硫率的影响不是很明显,主要是影响脱硝率.
(2)NO的脱除率随吸收剂初始浓度、Fe3+物质的量浓度、含氧量、NO浓度及SO2浓度的增大而增大,随烟气流量的增加而降低.
(3)由于吸收液pH值对脱硫脱硝率的影响不是很大,因此吸收液的pH值可取在弱酸到弱碱的范围内,操作弹性大,且对设备材质的防腐蚀性能要求不高.
(4)在烟气气体流量为0.4 L/min,气相中O2体积分数为6%,SO2体积分数为0.09%,NO体积分数为0.1%,I2物质的量浓度为5 mmol/L,Fe3+物质的量浓度为2 mmol/L,反应温度为40℃的条件下,脱硫脱硝率分别达到100%和69.9%.
[1]钟秦.燃煤烟气脱硫脱硝技术及工程实例[M].第二版.北京:化学工业出版社,2007.
[2]LEE H K,DESHWAL B R,YOO K S.Simultaneous removal of SO2and NO by sodium chlorite solution in wetted-wall column[J].Korean JChem Eng,2005,22(2):208-213.
[3]白云峰,李永旺,吴树志,等.KMnO4/CaCO3协同脱硫脱硝实验研究[J].煤炭学报,2008,33(5):575-578.BAI Yunfeng,LI Yongwang,WU Shuzhi,et al.Simultaneous absorption of SO2and NO from flue gas with KMnO4/CaCO3slurry[J].Jounal of China Coal Society,2008,33(5):575-578.
[4]JIN D S,DESHWAL B R,PARK Y S.Simultaneous removal of SO2and NO by wet scrubbing using aqueous chlorine dioxide solution[J].Journal of Hazardous Materials,2006,135(3):412-417.
[5]刘凤,赵毅,王亚君,等.酸性NaClO2溶液同时脱硫、脱硝的试验研究[J].动力工程,2008,28(3):425-429.LIU Feng,ZHAO Yi,WANG Yajun,et al.Simultaneous removal of SO2and NO by NaClO2acidic solutions[J].Journal of Power Engineering,2008,28(3):425-429.
[6]T HOM AS D,VANDERSCHUREN J.Analysis and prediction of the liquid phase composition for the absorption of nitrogen oxides into aqueous solutions[J].Sep Sci Technol,2000,18:37-45.
[7]马双忱,赵毅,郑福玲,等.液相催化氧化脱除烟道气中SO2和NOx的研究[J].中国环境科学,2001,2l(1):33-37.MA Shuangchen,ZHAO Yi,ZHENG Fuling,et al.Study On reducing SO2/NOxin flue gas by aqueous catalytic oxidation[J].China Environmental Science,2001,21(1):33-37.
[8]Christian Brandt,Rudi Van Eldik.Transition metalcatalyzed oxidation of sulfur(Ⅳ)oxides:atmospheric relevant processes and mechanisms[J].Chemical Reviews,1995,95(1):119-190.
[9]DESHWAL B R,LEE S H,JUNG J H,et al.Study on the removal of NOxfrom simulated flue gas using acidic NaClO2solution[J].Journal of Environmental Sciences,2008,20(1):33-38.
