结核病易感性相关基因-MBL基因的研究进展
2011-05-28张杰张万江
张杰 张万江
(石河子大学医学院病理生理学教研室/石河子大学《新疆地方与民族高发病》教育部重点实验室 石河子 832000)
结核病易感性相关基因-MBL基因的研究进展
张杰 张万江
(石河子大学医学院病理生理学教研室/石河子大学《新疆地方与民族高发病》教育部重点实验室 石河子 832000)
结核病是人类最古老的传染病之一,是由结核分枝杆菌引起的一种世界性传染病,是人类健康的重要杀手。据2000年我国第四次全国结核病流行病学抽样调查结果表明:我国活动性肺结核病患病率、涂阳率和死亡率分别为367/10万,106/10万和9.8/10万,结核病疫情在我国仍较为严峻,并且结核病的患病年轻化、病变多系统化,卡介苗预防效果不佳,结核病与艾滋病等疾病交叉感染以及结核分枝杆菌多重耐药性等现象致使我国结核病流行现状复杂化,导致我国结核病防治形势严峻,防治任务紧迫[1]。
近年来,多种结核病候选易感基因被发现,并且证实了这些基因在结核病发生发展中的重要作用。目前,这些基因功能研究明确,同时也有充分的生物学证据支持它们与不同人群的结核病易感性关联,在结核病的发生发展中起重要作用,甘露糖结合凝集素(MBL)是最具多态性的系统,MBL基因在抗原提呈和免疫应答中起着重要作用,其某些变异的等位基因可能使人体对某些疾病产生易感性。现已发现有70余种疾病与MBL基因多态性相关联,其中大多数自身免疫性疾病与MBL基因相关。本文就近年来MBL基因多态性与结核病遗传易感性的关联加以综述。
1 MBL基因的发现
1975年,人们发现哺乳动物细胞内可能存在一种能与甘露糖特异结合的蛋白质。1978年,Kawasaki T[2]等证实了这一可能性。他们从兔肝细胞质溶液中提出一种蛋白质,能与糖蛋白的甘露糖残基结合。此后,其他科学家用亲和层析等方法相继从人、大鼠、牛、小鼠、兔血清中也证实了该物质的存在,并确定此蛋白属于Lectin家族中的1个成员,其结构主要含有糖识别域(carbohydrate recognation domain,CRD)。Lectin通过CRD与细菌、细胞表面的不同糖配体结合,介导细菌凝集、调理作用、活化补体、诱导炎症反应、参与细胞表面识别。1993年将此蛋白命名为甘露糖结合的凝集素(mannose-binding lectin,MBL)。该蛋白质广泛存在于动物和人的肝脏及血液中。目前,对人的MBL的蛋白质和基因结构与功能有较深入的研究。已明确MBL由肝脏细胞合成后分泌入血循环中,通过识别与结合甘露糖,发挥免疫调节作用,或者激活补体系统,发挥调理素作用。它在机体免疫监视及免疫防御中有重要意义。
2 MBL基因的结构与功能
2.1 MBL基因的结构 甘露糖结合凝集素是Ca2+依赖型(C型)凝集素家族一员,为一种能特异识别糖类并与之非共价结合的糖蛋白,它广泛存在于人的肝脏及血液中,是机体天然免疫的1个重要组成部分[3]。MBL的蛋白质是多个亚单位的聚合体,每一亚单位由3条完全相同的肽链(每条链相对分子质量为28~32 kD)构成。各肽链均为4个区域:(1)N-端富含胱氨酸区:含20~21个氨基酸,其中胱氨酸参与亚单位间N-端二硫键形成;(2)胶原区:含18~20个Gly-Xaa-Yaa序列,为典型的胶原三螺旋结构,参与免疫调理和补体活化过程;(3)颈区:位于胶原区与糖识别区之间,功能尚不清楚,可能与亚单位的稳定有关;(4)糖识别区(CRD):含120个氨基酸其中有(17~18个保守氨基酸和14个可变氨基酸,保守氨基酸是维持蛋白质特殊的疏水核心所必需),呈一花蕾样结构。花蕾中三花瓣彼此间相距 54A,瓣尖平面为一正三角形,此结构为MBL蛋白质发挥生理效应的基础[4-5](图1)。
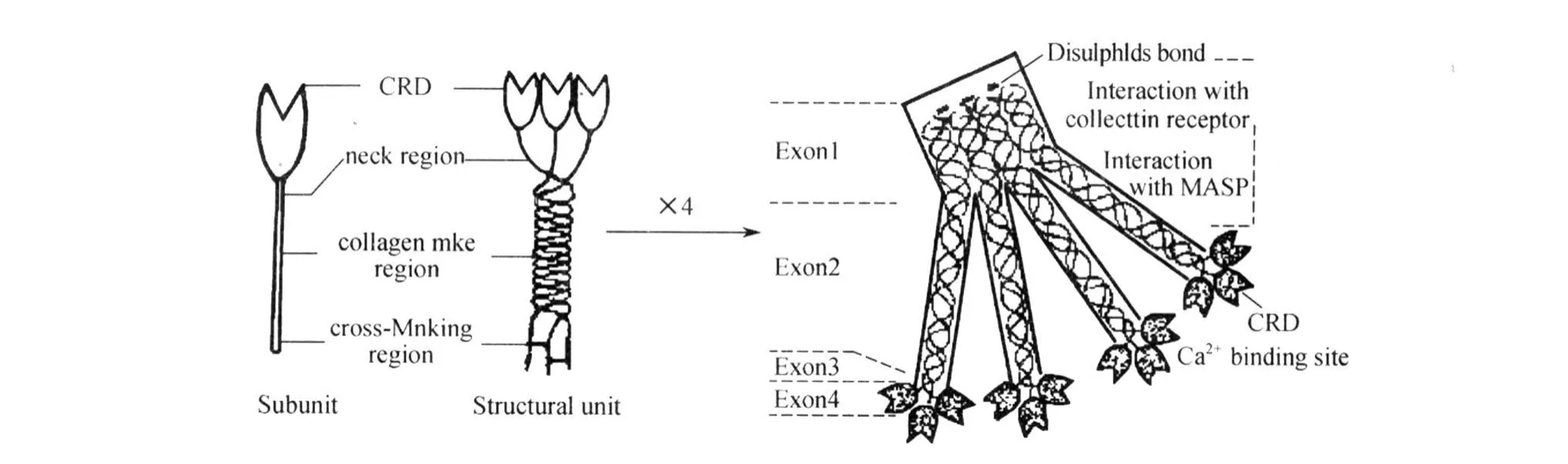
图1 MBL分子的亚单位、结构单位和多聚体结构
2.2 MBL基因的功能
2.2.1 识别糖配体MBL的CDR识别糖配体-糖结构的功能区,MBL能选择性地识别并可逆性结合于单糖成分,而当配体具有多个糖基时,其与多个CDR上的糖结合位点结合显示出高亲和性。正常哺乳类宿主的MBL仅识别外源性糖配体,而对内源性细胞表面糖结构不起反应,主要取决于:(1)MBL糖结合位点的规律性间隔(4.0~4.5 nm)与微生物表面大范围重复糖基之间匹配的衔接。(2)相对固定的CDR结合方向。正常生理状态下,组织细胞表面覆盖的糖蛋白一般为唾液酸低聚寡糖,不被MBL识别,但某些被病毒感染修饰的细胞或肿瘤细胞,如神经胶质瘤、结肠癌(SW116株)细胞在生长过程中表面的寡糖类紊乱,表达高甘露糖结构,进而成为MBL结合的配体[6]。
2.2.2 启动补体系统活化MBL是目前发现的惟一能活化补体系统的胶凝素,CDR是其主要的效应功能区。MBL启动补体系统活化与2种新的丝氨酸蛋白酶(MASP-1.MASP-2)有关。2种MASPs都具有裂解C2的活性。不同大小的MBL寡聚体在补体活化中可能起不同的作用。MBL-MASPs活化补体的途径又称为MBL途径或凝集素途径,补体通过此途径在病原体或细胞表面活化,发挥杀菌、溶解病毒和调理吞噬等免疫防御功能[7]。
2.2.3 促进吞噬、免疫调节作用MBL与C1q高度同源,与C1q受体(C1qR),又称胶凝素受体,有较强的亲和力。MBL能抑制C1q与C1qR的结合,竞争性结合表达于单核-巨噬细胞、中性粒细胞和吞噬细胞表面的C1qR。MBL与胶凝素受体的结合可桥联和促进富含甘露糖的靶配体如病原体与表达受体的细胞接触,增强吞噬细胞的呼吸爆发,加速杀灭病原微生物,启动和调节免疫应答[8]。MBL的CLR还可能与单核-巨噬细胞表面的相关受体结合,直接调理吞噬作用。
3 MBL基因多态性在人类不同种族之间的差异性
近年来,随着MBL基因定位、克隆及结构分析的进展,对MBL遗传性缺损的分子病理基础已有了较深入的了解。经研究血清MBL的水平受MBL基因结构区变异及启动子区基因不同的调节活性影响。在正常人群中MBL基因的突变率是很高的,MBL基因多态性导致胶原样区域的氨基酸取代可降低MBL的装配性和稳定性,导致人群中血清MBL水平波动在 5 ng/ml至>5 μ g/ml。这可能反映了机体对于MBL相关免疫的自主调节机制,低血清MBL浓度的个体可能不易患补体介导的自身免疫性疾病。MBL基因外显子1第52、54和57位点的 3个点突变[9]以及启动子区-550、-221和+4位点的H/L、X/Y、P/Q的基因多态性均与凝集素低水平有关[10]。已进行的调查发现,不同人种MBL基因突变频率有较大差异,除Gys52点突变频率在所研究人群中均较低外(P≤0.05),Asp54突变频率在英格兰人为0.19,香港汉族人为0.11,非洲人中罕见。Glu57突变频率在非洲冈比亚人为0.29,而在高加索人中为0.02[11]。MBL在启动子区域-550(H/L)和-220(X/Y)的多态性呈连锁不平衡,存在的3个单倍型H/Y、L/Y和L/X分别与血清MBL高、中和低水平相关。已调查的白种人中3个单倍型出现频率分别为0.38、0.38和0.24;非洲黑人中分别为0.11、0.65和0.24[12]。施红[13]等利用PCR-RFLP方法检测了中国5个民族的955份样本,MBL-54基因突变频率分别为汉0.181、维吾尔族0.128、蒙古族0.181、藏族0.179以及彝族0.181,在所有的样品中均未发现MBL-52和MBL-57基因突变,对22份汉族样本DNA序列的测定验证了这一结果。维吾尔族人群MBL-54基因突变频率较其他4个民族低,与汉族人群相比,2组之间MBL-54基因型分布和突变频率的差异有统计学意义(分别为:χ2=7.998,P <0.025和 χ2=5.78,P<0.025)。经 χ2检验,5个民族MBL-54等位基因分布符合Hardy-Weinberg平衡。
由此可见,MBL结构基因点突变和启动子区SNP是决定血清MBL水平的关键因素。MBL胶原样区结构被破坏,影响稳定性和功能性MBL的形成,进而降低血浆中功能性MBL的含量,且在不同的种族中普遍存在,但不同人种的基因突变频率有所不同。
4 MBL基因在结核杆菌易感性方面表现出的多态性
MBL是一种存在于血清中的C型凝集素,其通过结合病原生物表面的甘露糖等糖基受体而直接介导调理吞噬作用或通过MBL途径激活补体,在机体的固有性免疫防御中发挥重要作用[14],具有2个等位基因改变的个体,其血清MBL浓度极低或测不到,而且易出现感染的复发。MBL缺乏被认为是世界上最常见的免疫缺陷疾病,其改变的等位基因非常常见,Garred等[15]推测杂合子的优势是通过传递对分枝杆菌疾病的抵抗来保持MBL改变的等位基因高频率的出现。Bellamy等[16]在冈比亚的研究发现非洲人MBL-57位密码子变体(variant)等位基因在结核病患者低于对照组(P=0.037)。由于处于统计结果有意义的临界点,此结果尚需在其他人群中进一步证实。
国外报道[17-18],印度人和非洲裔美国人肺结核病例MBL-54等位基因突变频率高于对照组,而在美国白人和西班牙裔人及土耳其人中未发现MBL基因突变与肺结核的相关[18-19],甚至发现MBL-57位点突变型是肺结核的保护基因型[16]。国内冯福民等[20]研究则认为,总MBL和MBL-52突变型等位基因可能与肺结核发病有关。还认为[20]MBL-54位点G/A突变可能与肺结核发病相关。刘玮等[21]研究认为,甘露糖结合凝集素(MBL)基因多态性可能与汉族人群肺结核发生的易感性相关。
总之,从目前的研究结果来看,人类肺结核病易感性与基因多态性有关联性,但种族间这种关联性存在差异。MBL基因多态性与肺结核易感性的相关性更密切、更直接,仍有待更进一步研究。
5 展望
尽管人们对结核病易感基因-MBL基因的作用以及其机制的认识已经有了一定的进展;而且已经在不同人群中开展了进一步的流行病调查研究,并对MBL基因与结核病发生发展之间的进一步的研究。但总的看来还不够深入,主要表现在对此基因突变位点数目及与抗病力之间的关系研究极为有限。到目前为止对其作用已得到初步实验证据,但对其抗病菌侵染的作用机理仍停留在假设水平上。今后还需对MBL基因在抗病菌侵染中的具体作用机制方面进行进一步的研究。从而进一步认识结核分枝杆菌感染的发病机制,促进治疗方案的改进,以及在流行病学和预防医学方面为人类抵抗结核分枝杆菌作出更大的贡献。
[1]全国结核病流行病学抽样调查技术指导组.第四次全国结核病流行病学抽样调查报告[J].中华结核和呼吸杂志,2002,25:3.
[2]Kawasaki T,Etoh R,Yamashina I.Isolation and characterization of a mannan-binding protein from rabbit liver[J].Biochem Biophy s Res Commun,1978,81(3):1018-1024.
[3]Fujita,T.Evolution of the lectin-complement pathway and itsrole in innate immunity,Nat Rev Immunol[J].2002,2(5):346-353.
[4]贾天军,刘萍,刘士先.MBL及其补体激括的 LECTIN途径.国外医学临床生物化学与检验学分册[J].2001,22(6):316-317.
[5]Presanis JS,Kojima M,Sim RB.Biochemistry and genetics of mannan-binding lectin(MBL)[J].2003,Biochem Soc.T rans,2003,31(4):748-752.
[6]M a Y,Uemura K,Oka S.Antitumor activity of mannan-binding proteinin vivoas revealed by a virus expression system:mannan-binding protein-dependentcell-mediated cytotoxicity[J].Proc Natl Acad Sci USA,1999,96(2):371-375.
[7]Gadjeva M,Thiel S,Jensenius JC.T he mannan-binding lectin pathaway of the innate immune response[J].Curr Opin Lmunal,2001,13(1):74-78.
[8]Mastushita M.T he lectin pathaway of the complement system[J].Microbial Immunol,1996,40(12):887-893.
[9]RiisA L,Hansen TK,Thiel S.T hyroid hormone increases mannan-binding lectin levels[J].Eur J Endocrinol,2005,153(5):643-649.
[10]M adsen HO,SatzM L,Hog h B.Different molecular events result in low protein levels of mannan-binding lectin in populations from southeast Africa and South America[J].J Immunol,1998,161(6):3169-3175.
[11]Madson HO,Garred P,Kurtzhals JA L.A new frequent allele is the missing link in the structure polymorphism of the humman mannan-binding protein[J].Immunogenetics,1994,40(1):37-44.
[12]Madson HO,Garred P,Thiel S.Interplay between promoter and structural gene variants contral basal serum level of mannan-binding protein[J].Immunol,1995,155(6):3013-3020.
[13] 施红,王福生,金磊,刘明旭,洪卫国,杜清友,雷周云,侯静,施明,邢利和.中国五个民族的甘露糖结合蛋白基因多态性特点及意义[J].中华医学遗传学杂志,2001,6(18):3:78-80.
[14]WA LL IS R.Interactions between Mannose-binding Lectin and MASPs during complement activation by the Lectin Pathway[J].Immunobiology,2007,212(4/5):289-299.
[15]Garred P,Harboe M,Oettinger T.Dual role of mannan binding protein in infections:another case of heterosis?[J]Eur J Immunogenet,1994,21(2):125-131.
[16]Bellamy R,Ruwende C,McAdam KP.Mannose binding protein deficiency is not associated with malaria,hepatitis B carriage nor tuberculosis in Africans[J].QJM,1998,91(1):13-18.
[17]Selvaraj P,Narayanan PR,Reetha AM.Association of functional mutant homozygotes of the mannose binding protein gene with susceptibility to pulmonary tuberculosis in Indian[J].Tuber Lung Dis,1999,79(4):221-227.
[18]El Sahly HM,Reich RA,Dou SJ.The effect of mannose binding lectin gene polymorphisms on susceptibility to tuberculosis in different ethnic g roups[J].Scand J Infect Dis,2004,36(2):106-108.
[19]Ozhas-Gerceker F,T ezcean I,Berkel AI.T he effect of mannose binding-protein gene polymorphisms in recurrentrespiratory system infections in children and lung tuberculosis[J].Turk J Pediatr,2003,45(2):95-98.
[20] 冯福民,刘茜,郭梅,王东,高宝霞,安雅臣,纪春梅,孙永红.甘露醇结合蛋白基因多态性与肺结核发病关系的研究[J].中华流行病学,2006,27(12):1082-1085.
[21]刘玮,张芳,赵秋敏,吴晓明,张翠英,田磊,李春芝,张浮河,杨红,曹务春.甘露糖结合凝集素基因多态性与肺结核易感性的研究[J].中国热带医学,2006,6(3):387-389.
国家自然科学基金资助项目(30760237)
张万江(zwj1117@sina.com)
2010-04-17)
(本文编辑:张晓进)
