熔盐电解技术在冶金中的应用
2011-03-21高华朱立光王超
高华,朱立光,王超
(河北联合大学 冶金与能源学院,河北唐山 063009)
0 引 言
离子熔体电解在冶金工业中占有十分重要的地位,离子熔体电解法可以得到水溶液电解方法不能生产的产品,其中包括制取所有的轻金属(Li,Na,K,Rb,Cs,Be,Mg,Ca,Sr,A l,Ba,Ti),难熔重金属(Zr,H f,V,Nb,Ta, Mo,W),稀土金属和某些非金属(B,C,Si,Te等)。大部分重有色金属在溶液中的电极电位比氢正,一般皆应用水溶液电解法提取或精炼。近三十年来,冶金工业面临环境污染和资源贫化等技术问题,引起人们对熔盐电解法在冶金中应用研究的关注。离子熔体由于它具有很高的导电与导热性,交换电流大,在这类介质中进行的化学与电化学反应速度快,允许采用的比电流强度比水溶液的比电流强度值高1~2个数量级。20世纪60年代苏联和加拿大相继开展了熔盐电解技术在冶金中应用方面的研究,七十年代的已进入扩大或工业试验阶段,某些技术已取得专利。考虑列熔盐电解技术的某些特点可茕有助于解决重金属抬金所面临的某些技术问题,为此,本文介绍了熔盐电解技术在电解制取与精炼金属钛、镍、铝的研究现状及其开发前景。
1 制取金属钛
Chen等利用二氧化钛(金红石或锐钛矿)制备Ti,FFC工艺的原理是:在槽温950℃,施加3V的槽电压下,选用固态二氧化钛做阴极,在CaCl2熔盐中进行熔盐电解反应,实验结果显示:有氧离子由TiO2阴极电离出来,并移至阳极以氧气形式放出。在电解槽的底部有金属钛沉积。在气体的收集中还发现了CO和CO2,这是因为阳极的石墨电极被氧化生成的。总电解反应为:TiO2(固态,阴极)=Ti(阴极)+ O2(阳极)电解池示意图为图1所示:
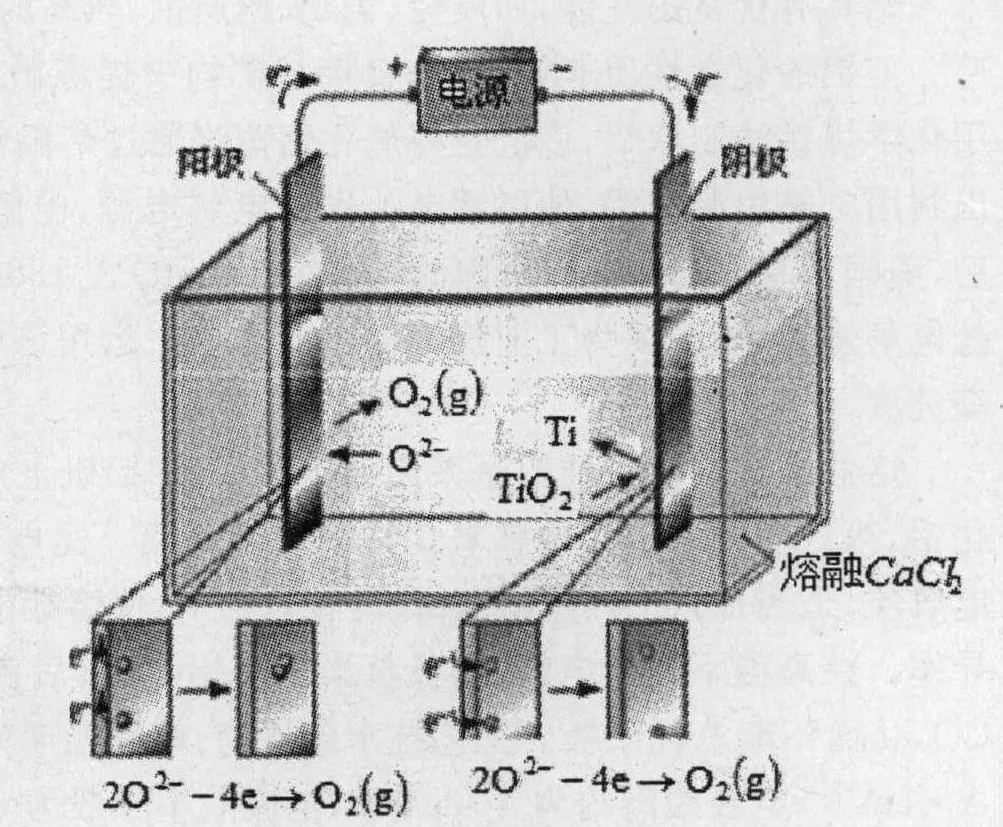
图1 电解池示意图
Chen等进行的研究中,对电解槽坩埚的材料、阴极TiO2的大小、结构及形貌等做了不同的尝试研究。研究:电解槽坩埚可用钛制作;若将TiO2和水以5:2的质量比混合做为阴极原料,浇铸成形状、大小不同的阴极,经室内自然干燥,在空气中以950℃烧结两个小时,合成TiO2阴极,该阴极可满足工作强度及孔隙度(40%~50%)。为方便电解产物的提取,采用约1.0 mm厚的钛箔篮式阴极,在钛箔上钻出许多空洞。篮式阴极的尺寸为15mm×45mm×45 mm,钛箔空洞的直径约为3.5mm大小,石墨坩埚尺寸为深40mm、直径70 mm和壁厚10 mm。以此方法制得海绵状或粉末状的钛,微粒的尺寸都在1~100μm之间[1]。Chen等在实验中做出了含99.8%的海绵钛产品。
东北大学的王淑兰[1]等利用CaC12熔盐做电解质,800~860℃电解TiO2,得到:1)TiO2的还原经过两个步骤TiO2先还原为TiO,TiO再还原Ti;2)这两个步骤的还原电极电势随着温度的升高而降低。郭胜惠等[2]在CaC12熔融体系中,采用自制球团状TiO2阴极直接电解还原制得海绵钛,并发现石墨阳极上有氧气放出。2004年Suzuki[3]提出MSE工艺,即金属氧化物的钙热还原和电解熔融CaCl2中的CaO的方法。赵志国等人[3]在2005年提出运用固体透氧膜技术(SOM工艺)制备金属钛,该工艺对于生产率有很大提高,真正做到了绿色环保,并降低了生产成本。
2 制取金属镍
英国剑桥大学的Fray等[4~5]人,用Nb2O5为阴极,将CaCl2,NaCl以1:1的摩尔比混合作为熔盐电
解质,施加3.1V的槽电压(低于熔盐的分解电压)进行熔盐电解,得到多孔的金属Nb片,经调整阴极和熔盐电解的条件,得到海绵状的金属Nb。进一步,Fray等对此工艺过程中的参数条件进行了优化[6~7],例如:阴极Nb2O5的颗粒尺寸、阴极片的形状、制片压力、烧结温度及时间、电解温度及时间和熔盐体系的改变等。得到:(1)电脱氧还原Nb2 O5制备Nb的过程分两步:第一步金属氧化物被阴极氧的离子化直接还原;第二步利用电化学除去Nb-O固熔体中的氧;(2)最佳的电解温度为800~950℃,电解时间为12~20h。同样,许茜[8~10]等人对利用熔盐电解由Nb2O5制备金属Nb也做了大量工作,通过优化控制参数,经过实验得出:将Nb2O5压制成片状,在1 200℃烧结12h,电解温度选用800℃,施加3.1V的电压进行熔盐电解,经过8h电解得到的产物中氧含量为1.09%。Nb2 O5电极的还原是分步进行的:Nb5+→Nb4+→Nb2+→Nb即按照由高价向低价的顺序进行还原。提出,Nb的β-Nb2O5变体对电脱氧最有利。值得注意的是,许茜等[11]通过改进阴极的活性研究得到在Nb2O5粉中加入CaCO3粉、CaO粉和石墨粉,有助于提高烧结样品中的氧空位,增强阴极片的电化学反应活性,对降低能源消耗,提高电解反应的速度。
3 制取金属铝
铝具有优良的性能,如质轻、美观、耐腐蚀、较高的强度、较高的导电及导热性能高,在各个领域中大受欢迎。但铝的化学性质非常活泼,直接从矿物中提炼出纯铝相当困难。1845年,德国的韦勒(wohler)提出运用化学炼铝法制取铝,该法是将氧化铝蒸汽通过熔融钾表面,得到金属铝。1854年德国的本生(Bunsen)提出利用电解法制取铝,他以蓄电池作为电解电源,电解NaCl-A lCl3熔盐制取金属铝。1867年发电机问世后,美国的霍尔(Hall)和法国的埃鲁(Heroult)在1886年提出“霍尔-埃鲁法”,即以冰晶石氧化铝混合的熔盐电解炼铝,该法成为工业炼铝的主要方法。运用该电解法所得铝的纯度达99.9%,电解精炼可进一步提高纯度。
熔盐电解法制备纯铝是采用铝土矿(又称铝矾土)为主要原料,因此炼铝的第一步是由铝土矿中提取氧化铝,第二步则是利用电解氧化铝制取金属铝。此电解过程中,选用Na3 A lF6-A l2 O3(3w t%~10w t%)为电解质,适当加入CaF2、LiF、M gF2等添加剂,使熔盐电解质的熔点降低,减少铝的损失,同时提高熔盐的电导率。在高温下进行电解,阴极析出液态铝,出槽后浇铸,得到铝锭。采用碳电极为阳极,阳极生成CO2及CO,从而不断消耗阳极。工艺技术条件为:电解温度为950℃~970℃,电流密度约为6000 A◦cm-2~10000 A◦cm-2,电极距离约为4~5mm,电流效率一般为85%~95%,槽电压约为4V~4.3V,每生产1t铝的总能耗高达15 000~17 500kWh。其反应方程式如下:
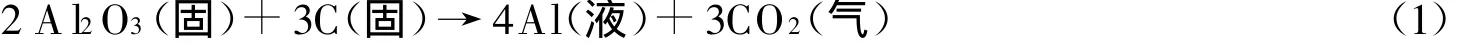
此后,美国铝业公司又研究开发出了氯化铝电解法。选用含2%~15%A lCl3(由A l2O3和C,Cl2反应得到)的NaCl-LiCl为熔盐电解质,石墨做阳极,电解温度为700℃,电流密度为10kA◦m-2进行电解得到A l,电解反应为:2 A lCl3→2A l+3Cl2结果显示,运用此方法制铝电能消耗比H all-Herou lt法低[12]。
4 制取金属铅
文献采用NaCl-KCl-PbS系熔体,原料PbS在熔体中处于悬浮状态,电解温度为690~730℃,1500A级电解槽槽电压达7~11V,阳极是石墨,阴极为液态铅,铅精矿成分为:71.75%Pb,1.7%S,3.66%Fe,0.32% Cu,3.0%Zn,0.030%Bi,0.05%Sb,As、Sn、Cd各为0.02%,Ag0.05%,SiO2及M gO各为1~1.4%,在NaCl-KCl熔体中电解PbS时,可能会进行如下过程:

其他文献则介绍采用NaOH和NaPO3-KPO3-NaC1熔体电解溶于其中的PbS,在NaOH中,电解温度低达265℃,电流效率达81%。
近年来由于回收废蓄电池极板的需要,文献研究了用离子熔体技术电解PbO的工艺,电解质为PbCl2-NaCl,PbC l2-KCl-NaOH及PbC12,采用碳或石墨作电极,在500℃下,PbO分解电压仅0.55V,通电后,较正电性杂质(Bi,Sb,Sn,Cu,Ag)与铅一起在阴极析出,而负电性杂质Na,A 1,Si,Fe则留于熔盐中。当Dk为0.13A/cm2,Dk为0.28A/cm2时,槽电压仅2.1V。PbO在熔盐中的溶解度近34%,电流效率迭70~98%,铅的纯度为99%,每公斤纯铅电耗1.3度。
5 结束语
综上所述,可以认为,熔盐电解技术在电解制取和精炼某些金属中的优点是明显的,它在冶金中的开发应用是值得注意的,其开发应用的关键是,1)在于需解决耐高温熔体侵蚀的设备材质和隔板材料;2)应采用低温电解工艺以降低能耗。由此可见,深入研究离子熔体电解技术的基础理论和电解工艺是有实际意义的。
[1] Wang Sh.L,Li Y.J.Reaction mechanism of direct electroredun tion of titanium dioxide inmolten calnium chloride[J].JElectroanalyticalChem,2004:547~637.
[2] 郭胜惠,彭金辉,张世敏,等.熔盐电解还原TiO2制取海绵钛新技术研究[J].昆明理工大学学报,2004,29(4):50~55.
[3] Suzuki RO.Calciotherm ic redu ction of TiO2and in situ electrolysis ofCaO in themolten CaC l2[J].Journalof Physicsand Chem istry of Solids,2005,66(1):461~465.
[4] Yan X Y,Fray D J.Direct electrochem ical reduction of niobium pentoxide to niobium metal in a eutectic of CaC l2-NaC lmelt[C]. Light Metals:Proceedings of Sessions,TMS AnnualM eeting(Warrendale,Pennsylvania),2002:5.
[5] Yan X Y,Fray D J.Production of niobium pow der by direct electrochem ical reduction of solid Nb2O5in a eu tectic CaCl2-NaC lm elt [J].M etall T rans B,2002,33 B:685~694.
[6] Yan X Y,Fray D J.Using electro-deoxidation to synthesize niobium sponge from solid Nb2O5in alkali-earthm etalchloridemelts[J]. JM ater Res,2003,18(2):346~353.
[7] Yan X Y,Fray D J.Electrochemical studies on reduction of solid Nb2O5in molten CaCl2-NaCl eu tectic:I.Factorsaffecting electrodeoxidation of solid Nb2O5to niobium[J].JElectrochem ical Soc,2005,152(1):12~18.
[8] 邓丽琴,许茜,李兵,等.电脱氧法由Nb2O5直接制备金属铌[J].中国有色金属学报,2005,15(4):541~545.
[9] Xu Q,Deng L.Q.A study of cathode imp rovemen t for electrodeoxidation of Nb2O5in a eutectic CaCl2-NaC lmelt at 1073K[J].J A lloys Comp,2005,396:288~295.
[10] 邓丽琴,许茜.电脱氧法由Nb2O5直接制备金属铌的研究[D].沈阳:东北大学,2004.
[11] 邓丽琴,许茜,马涛,等.电脱氧法制铌用Nb2O5阴极活性的改进[J].金属学报,2005,41(5):551~555.
[12] 陈延禧.电解工程[M].天津:天津科学技术出版社,1993.
