新型高效饲料组合酶的最新理论研究与应用技术
2011-03-09冯定远
冯定远
酶制剂作为一种具有生物活性的天然催化剂,通过与底物的结合,降低反应所需要的活化能,可以极大地提高化学反应速度。饲用酶制剂的研究开发和推广应用,已成为生物技术在饲料工业和养殖中应用的重要领域,酶制剂作为一种新型高效饲料添加剂,为开辟新的饲料资源、降低饲料生产成本提供了行之有效的途径,同时可以提高动物生产性能和减少养殖排泄物的污染,为饲料工业和养殖业高效、节粮、环保等可持续发展提供了保障和可能性,而新型的饲料酶制剂不断被研究和开发是重要前提。组合酶作为酶制剂产品设计的创新理念,有别于传统的单酶和复合酶,能充分体现酶制剂的高效性、针对性,以“差异互补、协同增效”为核心理念。
1 饲料酶制剂的种类
至今为止,已发现有3000多种酶,用于饲料中只是其中很小的一部分。生物体内生化代谢途径中的酶可分为氧化还原酶类、水解酶类、转移酶类、裂合酶类、异构酶类和合成酶类等几类。工业上应用的酶制剂大多数为水解酶。酶制剂的分类按作用底物的不同,可分为淀粉酶、蛋白酶、脂肪酶、果胶酶、木聚糖酶、β-葡聚糖酶、纤维素酶、植酸酶、核糖核酸酶等。单胃动物能分泌到消化道内的酶主要属于蛋白酶、脂肪酶类和碳水化合物酶类。底物大分子物质(如蛋白质、脂肪、多糖等)在酶的催化下被降解为易被吸收的小分子物质,如氨基酸、寡肽、脂肪酸、葡萄糖、寡糖等。饲料酶制剂的分类方法仍没有统一,饲料酶制剂大致可分为外源消化酶和非消化酶两大类。非消化酶是指动物自身不能分泌到消化道内的酶,这类酶能消化动物自身不能消化的物质或降解一些抗营养因子,主要有纤维素酶、木聚糖酶、β-葡聚糖酶、植酸酶、果胶酶等。外源消化酶是指动物自身能够分泌,但大部分来源于微生物和植物的淀粉酶、蛋白酶和脂肪酶类等。催化水解同一种底物的酶可以有不同来源,例如,催化水解纤维素的酶有绿色木霉(Trichoderma viride)纤维素酶、嗜松青霉(Penicillium pinophilum)纤维素酶、生黄瘤胃球菌(R.flavefaciens)纤维素酶,等等。针对这一特点,我们先后系统地比较研究了不同来源的纤维素酶(黄燕华,2004)、不同来源的木聚糖酶(于旭华,2004)和不同来源的蛋白酶(未公开资料)。同样,同一来源的生物,特别是微生物(包括真菌、细菌、放线菌等)可以产生不同的酶,例如,厌氧微生物能产生降解木聚糖、甘露聚糖的复合多酶系统。另外,所谓木聚糖酶、β-葡聚糖酶、纤维素酶等是一个笼统的概念,它们是一类作用相近的酶的统称,例如,纤维素酶主要有三种,即内切葡聚糖酶、外切葡聚糖酶和β-葡糖苷酶。
所谓单酶或单一酶(Single Enzyme)是指特定来源而催化水解一种底物的酶制剂,如木瓜蛋白酶、胃蛋白酶、里氏木霉(T.reesei)纤维素酶、康宁木霉(Trichoderma koningii)纤维素酶、曲霉菌(Aspergillus)木聚糖酶、隐酵母(Cryptococcus)木聚糖酶等等,它们都是单酶。
与单酶相对应的是复合酶。所谓复合酶(Complex Enzymes)是指由催化水解不同底物的多种酶混合(mix)而成的酶制剂。多种酶的来源可以不同,也可以相同,特别是有些商业系统微生物的固体发酵,单一菌株都可以产生多种酶。复合酶可以以动物种类及阶段为目标设计酶谱和活性,如蛋鸡日粮专用酶;也可以以日粮特性为目标配制酶的种类和有效成分,如小麦型日粮专用酶。目前饲料和养殖业使用的除少量是单酶添加剂外,大多数为复合酶添加剂。
2 组合酶和组合型复合酶的概念和特性
饲料工业和养殖业面临影响可持续发展三大问题:违禁药物和促生长剂大量使用导致的饲料安全问题、未被充分吸收利用养分的大量排放造成的环境污染问题和常规饲料原料缺乏及价格上涨问题。饲料酶制剂由于其独特的作用,被广泛认为是目前唯一能够在不同程度同时解决这影响可持续发展三大问题的饲料添加剂。尽管这项技术已有了长足发展,但是迄今为止,全球单胃动物饲料仅有20%左右使用了酶,总价值约3亿美元。于是饲料酶产业界质疑:饲料酶的发展为什么不能更快些?尤其那些已经显示出良好商业前景的饲料酶。
当然,酶制剂不能简单等同于促生长剂,而且酶的影响因素很多,其发挥作用既有动物的因素,又有日粮的因素,还有酶本身的因素(Marquardt和Bedford,2001)。过去我们广泛使用的是单一酶(如小麦型日粮添加一种单一的木聚糖酶),或者复合酶(如仔猪日粮使用蛋白酶和淀粉酶等组成的复合酶)。如何解决酶制剂使用的针对性和高效性是酶制剂发挥其效果的关键。目前在酶制剂理论研究和产品开发,恰恰在针对性和高效性存在很大的问题。应该承认,我们对酶在饲料中的应用了解还很有限,有很大的盲目性。如何高效地发挥酶的催化功能,必须在酶制剂的应用上,创新思维,构建新的应用体系。冯定远(2004)在讨论饲料工业的技术创新时就提出了饲料酶制剂应用的组合酶概念,它有别于传统上的复合酶。此后,饲料酶行业已经开始关注并实践。
所谓组合酶(Combinative Enzymes)是指由催化水解同一底物的来源和特性不同,利用酶催化的协同作用,选择具有互补性的两种或两种以上酶的配合 (formulate)而成的酶制剂。例如,蛋白酶组合酶制剂由多种来源不同的蛋白酶组成,可以有木瓜蛋白酶和黑曲霉蛋白酶,甚至其他来源的蛋白酶;木聚糖酶组合酶制剂由多种来源不同的木聚糖酶组成,真菌木聚糖酶和细菌木聚糖酶的组合;纤维素酶组合酶制剂由木霉纤维素酶和青霉纤维素酶组成等等。组合酶不是简单的复合,而应该是根据不同酶的最适特性、作用特点和抗逆性的互补有机组合。可以是多种内切酶的组合,也可以是内切酶和外切酶的组合。组合酶应用最常见的例子是有目的地选择多种蛋白酶水解蛋白质原料生产生物活性肽,根据蛋白质原料的不同,几种蛋白酶的要求不同;而目的肽的不同,几种蛋白酶的选择也不一样。
饲料组合酶是酶制剂应用技术体系的一个技术创新。饲料组合酶一般应具备四个方面的特性:①催化水解同一底物酶的来源多样性(在一定程度体现经济性);②酶的催化反应的配合性(催化水解位点的不同和配合);③酶最适条件和抗逆特性的互补性;④酶的应用效果的高效性。饲料组合酶最终反映在解决催化饲料复杂底物的高效性问题。从严格意义上讲,设计和开发生产饲料组合酶应考虑这些特性,组合酶不是多种催化水解同一底物酶的简单混合,而是根据各自酶学特性的有机组合。
一般地,与常见的单酶与复合酶相比,科学合理的组合酶应考虑作用底物更有针对性、多种酶源的配合及互补和催化作用更加高效性。组合酶在饲料中应用的最大好处就是在酶的催化环境条件不理想的情况下,发挥其配合作用,从而达到高效能的目的。
如果考虑复合酶的作用同时,又要考虑组合酶的效果,可以配制应用组合型复合酶制剂(Combinative&Complex Enzymes)。一个典型的组合型复合酶制剂产品应该包括催化水解多种底物,而且催化水解同一底物的酶制剂有几种来源不同的单酶组成,例如,应用大量杂粕和麦类的非常规原料的日粮,可以设计含有真菌木聚糖酶、细菌木聚糖酶、木霉纤维素酶和青霉纤维素酶等组成的组合型复合酶制剂。
目前酶制剂产品开发仍然比较混乱,其中一个方面就是不同企业产品酶活之间没有可比性,只是笼统标明各种酶的活性,例如一个典型复合酶产品的例子,仔猪日粮专用酶:木聚糖酶(180000 U/g)、β-葡聚糖酶(25000 U/g)、纤维素酶(11000 U/g)、果胶酶(400 U/g)、淀粉酶(2000 U/g)、酸性蛋白酶(3000 U/g),添加量为50~100 g/t。木聚糖酶活性180000 U/g是高还是低?比另一企业产品的木聚糖酶活性120000 U/g是更好吗?不能简单评判。
组合酶的另一个作用是可以部分解决不同企业产品酶活之间可比性问题。组合酶的成分一般都要注明酶的来源,例如,小麦-杂粕型日粮专用组合型液体酶:哈茨木霉木聚糖酶(450000 U/g)、蓝状菌木聚糖酶(350000 U/g)、纤维杆菌纤维素酶(300000 U/g),嗜松青霉纤维素酶(350000 U/g),添加量为80~100 g/t。由于明确了酶的来源,酶活的意义就能够比较容易规范。
在上述的小麦-杂粕型日粮专用组合型液体酶配方中,考虑了木聚糖降解酶间的协同作用。木聚糖降解酶的同型协同作用已经在蓝状菌(Talaromyces byssochlamydoides)(Yoshioka等,1981) 和哈茨木霉(Trichoderma harzianum)(Wong等,1986)中得到了很好的验证。
3 提出新型饲料组合酶的理论基础
3.1 催化降解同一底物的酶来源很多,它们之间的催化功能既有可替代的、也有不可以替代的。这样,可替代性就有更多的选择性,对整体降低应用成本有好处;不可替代性就存在着互补性,对真正发挥酶的最大效率有好处。例如,蛋白酶有来源于动物、植物和微生物的蛋白酶,而动物、植物和微生物蛋白酶又分别有许多种。同样,植酸酶有来源于微生物、植物和动物的植酸酶,Dvorakova(1998)综述了3类植酸酶的结构和动力学特征。纤维素酶和木聚糖酶多由细菌和真菌产生,此类微生物包括:需氧性微生物(aerobes)、厌氧性微生物(anaerobes)、嗜温微生物(mesophiles)、嗜热微生物(thermophiles)和极温微生物(extremophiles)。耐超高温的微生物[如栖热袍菌属(thermotoga sp.)、激烈热球菌(pyrococcus furiosus)和热丝菌属(thermofilum sp.)]能生长在 85~110 ℃环境中,并能产生极其稳定的分解纤维素和半纤维素的酶(Simpson等,1991;Antranikian,1994;Witerhalter等,1995)。细菌纤维素酶有多种不同水解纤维素的机理,例如耗氧菌[纤维杆菌属(Cellulomonas)、假单胞杆菌属(Pseudomonas)、嗜热放线菌(Thermoactinomycetes)、褐色高温单胞菌(T.Fusca)、细小双孢子菌(Microbispora)]和粪堆梭菌(C.stercorarium)产生的纤维素分解酶系,有点类似于耗氧真菌产生的纤维素分解酶,这些纤维素分解酶系通过不同酶组分的相互协作来降解纤维素(Beguin 等 ,1992;Wood,1992;Gilbert 和 Hazlewood,1993)。植酸酶可以大致分成6-植酸酶和3-植酸酶两类。这种分类是根据植酸分子水解的起始位点而划分的,6-植酸酶多来源于植物,3-植酸酶是由真菌(Aspergillum sp.)产生的(Dvorakova,1998)。
3.2 不同来源酶的酶学性质是不同的,它们催化降解的位点不同,有些是外切酶,有些是内切酶。有目的互补组合,能够发挥各自性能,配合而达到最佳的作用效果。例如,木聚糖酶对多聚木聚糖的内部β-1,4键有活性,这种木聚糖酶称为内切木聚糖酶。根据其对不同多糖的活性,内切木聚糖酶又可分为特异性和非特异性木聚糖酶(Coughlan,1992;Coughlan等,1993)。特异性内切木聚糖酶仅对木聚糖的β-1,4键有活性,而非特异性内切木聚糖酶可以水解以β-1,4键连接的木聚糖、混合木聚糖的β-1,4键及其他β-1,4连接的多糖,如CM-纤维素。大多数内切木聚糖酶能特异性地作用于木聚糖的非取代木糖苷键,并释放取代的和非取代的木寡糖。相反,其他内切木聚糖酶特异性作用于在主链上的接近取代基团的木糖苷键。例如,来源于黑曲霉(Aspergillus niger)的两种酶(PI 8.0和9.6)对去掉阿拉伯糖取代基的木寡糖和木聚糖表现很小活性或没有活性(Frederick等,1985)。对混合木聚糖(具有 β-1,3、β-1,4键的 rhodymenan)作用的大多数内切葡聚糖酶能特异地作用于β-1,4键(Coughlan,1992)。同时,内切木聚糖酶除了能降解主链外,还可根据其能否降解支链释放阿拉伯糖而分为两类(Coughlan 等,1993)。
3.3 如果饲料成分复杂底物,特别是非淀粉多糖的降解需要多种酶之间协同作用。二个或更多的酶之间的有效配合,其作用效果好于单一添加任何一种酶制剂的叠加作用,这种现象就是协同作用。Giligan等(1954)在水解纤维素的过程中,首次证实了不同纤维素酶间的协同增效作用。类似的几项研究验证了在晶体纤维素的溶解过程中,内切葡聚糖酶和外切葡聚糖酶之间的协同作用(Wood,1988;Klyosov,1990;Bhat,1994)。有报道在真菌纤维素酶中存在五种协同作用:①内切葡聚糖酶和一种称为C1的非水解蛋白间的协同作用(Reese等,1950);②β-葡聚糖酶和内切葡聚糖酶或者CBH之间的协同作用(Eriksson等,1985);③两个免疫学上相关的或截然不同的CBH之间的协同作用(Wood等,1986);④源自相同或不同微生物内切葡聚糖酶和CBH之间的协同作用(Wood等,1989);⑤两种内切葡聚糖酶之间的协同作用(Klyosov,1990)。另外,细菌纤维素酶和真菌纤维素酶之间也有协同作用,来自嗜热纤维素单胞菌(C.thermocellum)的多酶复合体的亚基之间存在协同作用(Bhat等,1994;Wood 等,1994)。Coughlan 等(1988)、Wood(1988)以及 Klyosov(1990)等深入地研究了来自真菌的纤维素酶之间的协同作用。大部分的协同模式有:①内切葡聚糖酶和外切葡聚糖酶间的协同作用;②外切葡聚糖酶和外切葡聚糖酶之间的协同作用;③内切葡聚糖酶和内切葡聚糖酶之间的协同作用。Wood等(1972)认为,被内切纤维素酶裂解的纤维素链可以变成外切纤维素酶的底物,两种酶相互协同降解纤维素。但是该模型不能解释两种不同CBHs间的协同作用、或者CBH不能与来自不同微生物的内切葡聚糖酶相互协同作用的现象。因此,使用高纯度的内切葡聚糖酶和来自嗜松青霉(P.pinophium)的CBHs的研究表明,只有两种内切葡聚糖酶(EGⅢ和EGⅤ)对纤维素具有很强的吸附性,与CBHsⅠ和CBHsⅡ有协同作用(Wood等,1989)。他们认为,在CBHsⅠ和Ⅱ与内切葡聚糖酶之间的协同作用,是因为这两类酶间的不同立体空间结构造成的。有效而彻底的分解木聚糖需要有不同特性的主链裂解酶和支链裂解酶的协同作用(Coughlan 等,1993;Coughlan 等,1993)。对于木聚糖降解酶来讲,因为底物来源的天然差异,所以仅衡量产生的还原糖量,不足以证实其协同作用。因此,必须分离和纯化,并进行定性、定量分析其分解产物,以获得木聚糖降解酶协同作用的更为清晰的资料。事实上两种酶之间的协同作用模式有三种类型:①同型协同;②异型协同;③抗协同(Coughlan等,1993)。同型与异型协同可能有一种或二种产物。同型协同可以是在二种或多种的侧链裂解酶之间的协同,也可能是在二种或多种的主链裂解酶之间的协同(Coughlan等,1993)。同样,植酸水解为肌醇的全部过程已经确定,已经清楚,没有哪一个单独的酶能水解植酸分子中所有的磷酸,因此,整个水解过程是在很多非特异性酶的联合作用下完成的(Maenz,2004)。
3.4 在一定条件下(特定的作用环境和时间),某一种酶数量或活性进一步增加并不能提高催化性能,各种酶和对应的底物浓度的反应基本动力学是米氏方程(陈石根等,2001)。而不同来源作用同一种底物的酶的米氏方程不一样(陈芳艳,2010)。
3.5 同一类酶而来源不同其最适条件差异很大。不同菌属来源、不同发酵方式生产的纤维素酶在酶系组成及酶学特性上存在差异(孟雷等,2002)。绝大多数来自真菌的内切葡聚糖酶和外切葡聚糖酶的分子量均在20~100 kDa的范围内,而β-葡萄糖苷酶的分子量范围为50~300 kDa。通常情况下,来自真菌的酶活性的最佳pH值在4.0~6.0之间,而来自细菌的酶的最佳活性pH值为6.0~7.0之间(Wood,1985)。来自嗜温(mesophilic)真菌和细菌的内切葡聚糖酶、CBHs和β-葡萄糖苷酶的最佳活性温度是40~55℃(Wood等,1988;Bhat等,1989;Christakopoulos等,1994),而来自嗜温和嗜热微生物的纤维素酶的最佳活性温度分别为 60~80 ℃和 90~110 ℃(Khandke等,1989;Bhat等,1993;Antranikian,1994)。在黄燕华(2004)的试验中三种纤维素酶分别来自木霉固体发酵、木霉液体发酵和青霉液体发酵,三种酶的组分和酶学特性都存在差异。三种不同来源的纤维素酶在相同测定条件下其酶活差别较大。由于不同来源的酶活性上的差别,在实际应用中以重量比来添加,显然会造成使用效果差异较大。不同来源的纤维素酶虽然作用相同,但具有不同的最适pH值和温度,因此,用同一种测定方法测定不同来源的纤维素酶得到的酶活值尚不能完全具有代表性。
3.6 同一类酶而来源不同其热稳定性差异很大。例如:经80℃高温处理1~3 min后,三种纤维素酶的剩余酶活差异较大;其中,青霉液体发酵的酶的热稳定性较好,剩余酶活仍保留了94.8%。而木霉固体发酵酶和木霉液体发酵酶热稳定性较差(黄燕华,2004)。
3.7 同一类酶而来源不同其对于胃肠道的蛋白水解酶的耐受性差异很大。对于畜禽胃肠道环境的稳定性最终决定外源酶制剂的应用效果,只有在消化道内能保留足够的活性,存留足够的时间,酶制剂才能发挥应有的作用。研究发现,在消化道环境中对于3种纤维素酶,木霉液体发酵酶的稳定性最好,木霉固体发酵酶最差(黄燕华,2004)。另外,在体外试验中胃蛋白酶对木霉固体发酵酶影响最大,木霉液体发酵酶耐受性较好。
3.8 来源于不同饲料中的一些离子对同一类酶的活性影响差异很大。如我们的研究发现:Fe2+、Zn2+和Ca2+对3种纤维素酶的CMCase和FPase活性均有抑制作用,但抑制作用都不显著,只有木霉液体发酵酶的CMCase活性受Ca2+影响较大;Mn2+对3种纤维素酶的CMCase和FPase活性均有激活作用;Cu2+对3种纤维素酶的CMCase活性有激活作用,但对其FPase活性则是抑制作用,其中木霉液体发酵酶受影响最大;Mg2+对3种纤维素酶的作用出现了差异,它使青霉液体发酵酶的CMCase和FPase活性提高,而使木霉固体发酵和木霉液体发酵酶的CMCase和FPase活性降低,其中,木霉液体发酵酶的FPase活性受影响较大(黄燕华,2004)。离子对酶活抑制或激活影响的不一致,可能是因为不同来源的纤维素酶需用作电子载体的特定金属离子不同造成的。
4 饲料组合酶的设计技术
4.1 差异性筛选技术
组合酶的筛选首先需要明确作用于同一底物的多个酶不是同一种酶,如木聚糖酶有内切酶和外切酶(苏玉春,2008)、植酸酶有3-植酸酶(EC 3.1.3.8)和6-植酸酶(EC 3.1.3.26)(付大伟,2010)等。为确定组合酶组合筛选的对象为不同的酶,可采取以下4种方法进行区分:①蛋白分子特性的差异性筛选。如Sapag等(2002)研究了26个来源的木聚糖酶,通过比较长度、分子量和等电点可发现其中哪些是同种酶(见表1)。其中,通过电泳的方式测定酶蛋白的分子量最直接、简单和快捷,如我们课题组在2004年从市场上采集了2个企业的木聚糖酶,通过电泳发现真菌性木聚糖酶和细菌性木聚糖酶的分子量分别为23.65和24.45 kDa,属于不同的木聚糖酶(于旭华,2004)。②不同来源酶的氨基酸组成和含量。如于旭华(2004)比较了6个来源的木聚糖酶,发现其氨基酸组合和含量上有明显差异(见表2)。③米氏常数的比较。如陈芳艳(2010)对蛋白修饰改造之后谷胱甘肽过氧化物酶与修饰前的米氏常数比较发现分别为1.484 mmol/l和0.2857 mmol/l。④对酶蛋白的三维空间结构进行分析。如采用X-ray衍生技术分析到的瘤胃微生物植酸酶(郭瑞庭等,2004)、大肠杆菌植酸酶(Liu等,2004;Xiang等,2004)和芽孢杆菌植酸酶(Ha等,2000;Shin等,2001)的空间结构分别见图 1、2、3。

表1 不同微生物来源木聚糖酶的蛋白质分子特性
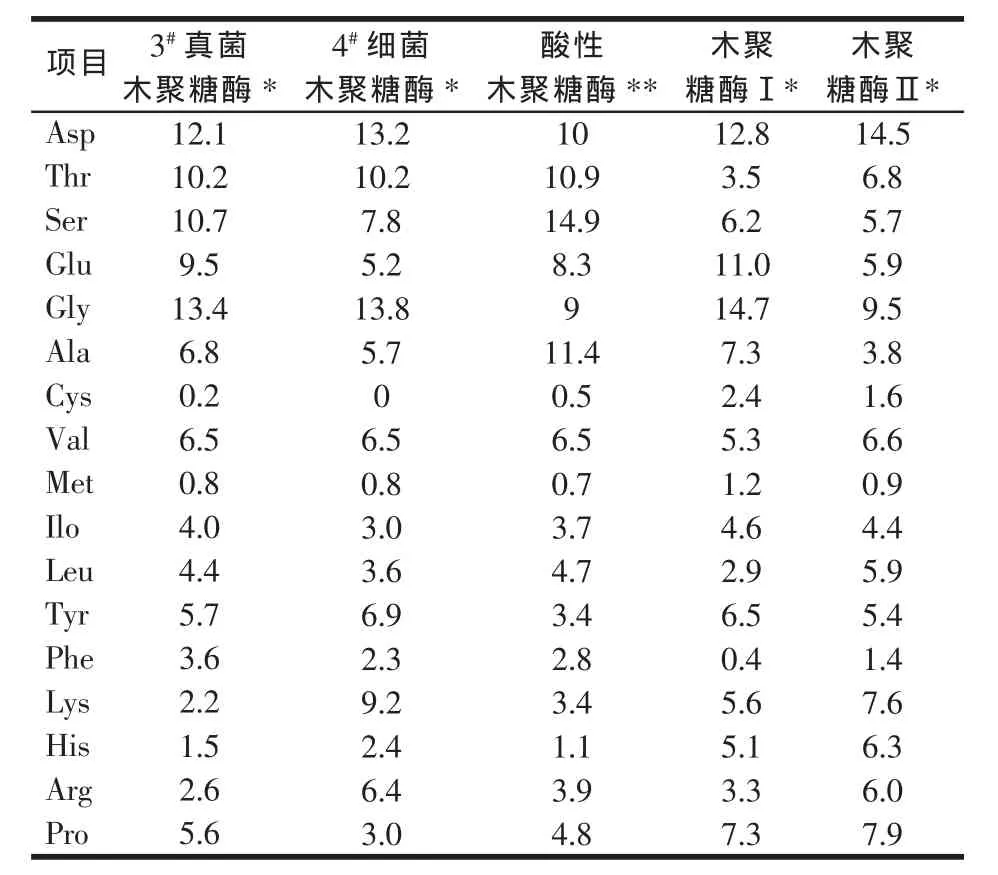
表2 3#真菌木聚糖酶和4#细菌木聚糖酶氨基酸组成和含量(%)
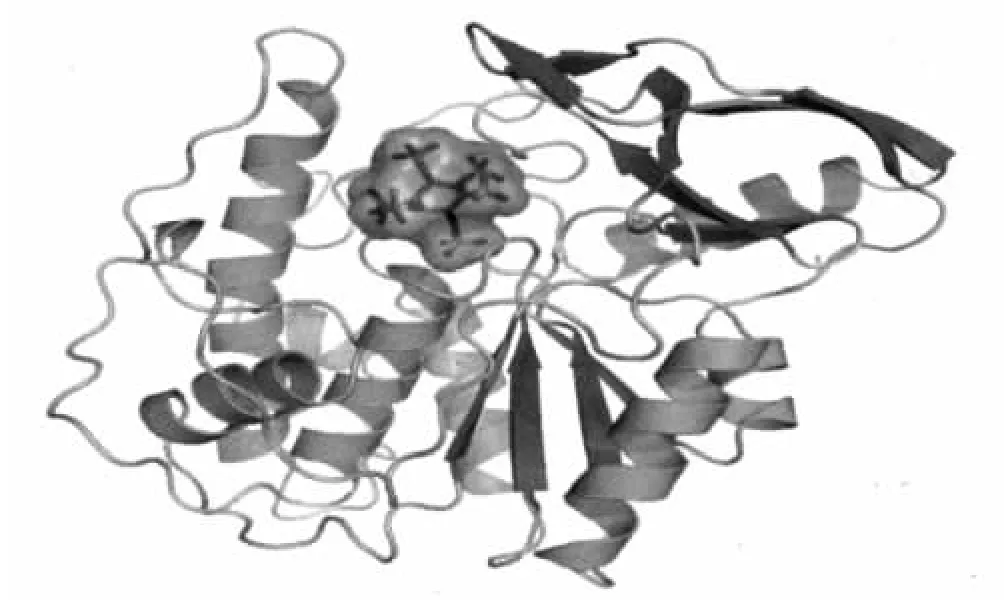
图1 瘤胃微生物植酸酶

图2 大肠杆菌植酸酶

图3 芽孢杆菌植酸酶
4.2 互补性筛选技术
差异性是组合酶组合筛选的基本条件,而不同单酶的差异性则是组合酶组合筛选的基本要求。为确定组合酶组合筛选的对象之间的互补性,可根据酶最适条件和抗逆特性进行筛选:①酶最适条件的互补性。如于旭华(2004)比较分别来源细菌和真菌的木聚糖酶耐热性,发现真菌性木聚糖酶3#在30~50℃之间具有比细菌性木聚糖酶4#更高的活性,而在50~80℃则相反,理论上两者组合具有充分利用肠道和加工过程中多个水解位点的组合增效性;而酸性植酸酶在pH值2~4.5条件下具有比中性植酸酶更高的酶活,而在pH值4.5~7.0条件下则相反,具有在不同pH值条件下的互补性(李春文,2007)。②抗逆特性的互补性。如于旭华(2004)在比较木聚糖酶对Ca2+浓度耐受性发现,真菌性木聚糖酶在低Ca2+浓度条件下具有较高的活性,而细菌性木聚糖酶在高Ca2+浓度条件下具有较高的活性;而黄燕华(2004)比较三个来源的纤维素酶对胃蛋白酶和胰蛋白酶耐受性的结果发现,纤维素酶B在胃蛋白酶处理条件下具有最高活性,而纤维素酶C在胰蛋白酶处理条件下具有最高的活性。
4.3 组合酶筛选的基本方法
在差异性和互补性筛选的基础上,组合增效才是组合筛选的最终目的。根据前两部分的工作,我们归纳出,一般组合酶组合筛选的思路可选择内切+外切、中性+酸性及真菌性+细菌性3种。在此基础上,筛选的方法可以以组合之后提高产物的降解效率、组合提高酶的活力、组合提高降解原料的效率、体内和体外消化代谢试验、饲养试验等。其中,在以中性+酸性的模式筛选组合蛋白酶时发现,相对单酶,中性和酸性蛋白酶以3:7的比例组合可显著提高豆粕总水解度、可溶性蛋白水解度和蛋白浸出率(曾谨勇,2010;雷建平,2010),而且可提高豆粕降解产物中小肽的含量;内切+外切筛选技术方面,Wood等(1989)发现,来自嗜松青霉(P.pinophlum)的CBHS(外切葡聚糖纤维二糖水解酶)(Ⅰ和Ⅱ型)与内切葡聚糖酶(EⅠ至EⅤ)之间在水解棉花纤维上具有显著的协同作用;真菌性+细菌性筛选技术方面,我们最近选择了4种不同来源的木聚糖酶,其中真菌性木聚糖酶A+细菌性木聚糖酶C按3:7组合,显著提高了降解木聚糖、小麦的效率,并在后期肉鸡饲养试验中也表现出相对单酶更高的生长性能;此外,张民(2010)选用组合木聚糖酶、真菌酸性木聚糖酶、真菌中性木聚糖酶、细菌中性木聚糖酶进行蛋鸡的饲养试验表明,添加1:1:1组合的木聚糖酶对产蛋鸡产蛋率和降低料蛋比的影响显著优于不同来源的单一木聚糖酶。
5 饲料组合酶应用的价值和意义
组合酶产品并不是一个完全新的产品,已经有少量饲料酶制剂产品初步具有组合酶的特性。但是,总体而言,开发应用组合酶或组合型复合酶还很少,有意识、专门化设计生产组合酶或组合型复合酶就更少。组合酶有别于传统上的复合酶,作为一个专门类别的新型酶制剂进行讨论,规范和完善它的概念、特性和作用还是第一次,其目的是为了强调它的重要性和应用前景。目前,饲料组合酶的应用主要有如下几方面的价值。
5.1 催化同一底物而来源不同的酶的价格是不同的,互相组合,可以利用一些来源方便,商业生产成本比较低的酶制剂,再结合一些相对成本高、而作用能够互补的酶制剂,在保证酶添加使用效果的情况下,整体降低饲料酶制剂添加剂的使用成本,有利于酶制剂添加剂推广使用。
5.2 饲料生产成本的问题,相当程度是由于原料成本上涨造成的,开发和有效利用非常规饲料原料是关键。非常规饲料原料主要是由于含有一些抗营养因子,影响了它们的高效利用。目前处理非常规饲料原料往往使用一些专门的酶制剂,但是由于一些非常规饲料原料成分和结构的复杂性,一般的单酶或者复合酶并不能有效的解决其利用效率的问题。组合酶或组合型复合酶由于其酶种来源及其互补和协同特性,在理论上具有比一般单酶或复合酶的酶学特性的优势,能够发挥其快速高效作用的潜能。因此,组合酶或组合型复合酶在提高非常规饲料原料日粮的利用效率、有效地开发非常规饲料原料资源等方面具有巨大的潜力。
5.3 一些畜禽由于种类和生长阶段、消化生理特性的关系,不能很好地利用人工配制的日粮,特别是日粮中含有较多的植物性成分和一些难于利用的成分,使一些饲料产品的质量低且不稳定。例如,仔猪对大豆蛋白的抗原性问题、谷物抗性淀粉利用问题、水产动物对植物蛋白利用问题、宠物对植物成分利用问题等。人们尝试开发的一些所谓特别饲料,例如,早期的猪禽无鱼粉配方、仔猪无乳制品日粮、低鱼粉或无鱼粉水产饲料、甚至最近的猪禽无玉米、豆粕日粮,等等,尽管有成功的例子,但广泛应用不多,当然因素很多,其中一个重要的因素是处理好动物的消化生理和日粮成分的特性关系。解决动物的消化生理和日粮成分的特性关系问题的一个措施是应用饲料酶制剂。但是,在开发上述饲料产品,人们普遍考虑了酶制剂,甚至使用了一些专门的酶制剂或强化了用量,而通常效果并不理想。如果我们利用组合酶或组合型复合酶互补性和协同特性,有针对性开发特种动物专用或者特种类型日粮专用的组合酶或组合型复合酶,组合酶或组合型复合酶有可能为部分或全部解决这些问题提供一种有效措施。
应用组合酶添加剂的前提是日粮中存在大量复杂的大分子、难分解的营养或抗营养成分底物,需要多种针对同一底物的酶配合完成水解任务。相反,有一些相对容易分解的底物,可能一种酶就可以完成有效的催化任务,就没有必要一定使用组合酶。所以,从应用成本角度,应用饲料酶的总原则是:可以应用单酶(单一酶)添加剂基本解决问题的,就不要使用组合酶或复合酶添加剂;可以应用复合酶添加剂基本解决问题的,就不要使用组合型复合酶添加剂。
组合酶与广泛应用的复合酶的目的意义是不同的,饲料复合酶的特点是解决催化多种饲料成分底物的问题;而饲料组合酶的最大特点是解决催化饲料成分底物的高效性问题。目前,饲料酶制剂应用的最大问题就是高效性问题,特别是酶如何在饲料加工过程中能够发挥作用,以及考虑在消化道的抗逆性,在短时间内如何使酶的配合发挥最大效率的问题最突出。随着非常规饲料原料的大量使用,高效的组合酶将更有优势。因此,今后饲料酶制剂的发展方向,应该是研发和使用更多的组合酶或组合型复合酶产品。
[1]于旭华.真菌性和细菌性木聚糖酶对肉鸡生长性能的影响及机理研究[D].华南农业大学博士学位论文,2004.
[2]付大伟.Yersinia spp.来源植酸酶的酶学性质及结构与功能研究[D].中国农业科学院博士学位论文,2010.
[3]冯定远.饲料工业的技术创新与技术经济[J].饲料工业,2004(11):1-6.
[4]张民,范仕苓,马秋刚,等.不同来源的木聚糖酶及组合酶对产蛋鸡生产性能的影响[J].饲料工业,2010,31(6):12-15.
[5]李春文.复合植酸酶对饲料中钙磷体外消化率的影响 [D].华南农业大学本科论文,2007.
[6]苏玉春.木聚糖酶的酶学特性及基因克隆表达研究 [D].吉林农业大学博士学位论文,2008.
[7]陆健,曹钰,陈坚,等.米曲霉RIBI28耐酸性木聚糖酶的研究[J].无锡轻工大学学报,2001,20(6):608-611.
[8]陈石根,周润琦.酶学[M].上海:复旦大学出版社,2001:166-176.
[9]陈芳艳.猪谷胱甘肽过氧化物酶的修饰及生物活性研究 [D].华南农业大学博士学位论文,2010.
[10]孟雷,陈冠军,王怡,等.纤维素酶的多型性[J].纤维素科学与技术,2002(2):47-54.
[11]黄燕华.不同来源纤维素酶的酶学特性及其在马冈鹅中的应用[D].华南农业大学博士学位论文,2004.
[12]曾谨勇.中性蛋白酶不同比例对豆粕蛋白水解效果的影响[D].华南农业大学本科论文,2010.
[13]雷建平.不同中性蛋白酶水解豆粕多肽最佳组合的筛选[D].华南农业大学本科论文,2010.
[14]Antranikian G.Extreme thermophilic and hyperthermophilic microorganisms and their enzymes [M].Advanced Workshops in Biotechnological on Extremophilic Microorganisms,NTUA,A-thens,Greece,1994:1-30.
[15]Beguin P,Millet J,Chauvaux S,et al.Bacterial cellulases[J].Biochemical Society Transactions,1992,20:42-46.
[16]Bhat K M,McCrae S I,Wood T M.The endo- (1-4)-0-D-glucanase system of Penicillium pinophilum cellulase:isolation,purification and characterization of five major endog1ucanase components[J].Carbohydrate Research,1989,190:279-297.
[17]Bhat S,Goodenough P W,Bhat M K,et al.Isolation of four major subunits from Clostridium thermocellum cellulosome and their synergism in the hydrolysis of crystalline cellulose [J].International Journal of Biological Macromolecules,1994,16:335-342.
[18]Bhat K M,Gaikwad J S,Maheshwari R.Purification and characterization of an extracellular β-glucosidase from the thermophilic fungus sporotrichum thermophile and its influence on cellulase activity[J].Journal of General Microbiology,1993,139:2825-2832.
[19]Christakopoulos P,Goodenough P W,Kekos D,et al.Purification and characterization of an extracellular β-glucosidase with transglycosylation and exoglucosidase activities from Fusarium oxysporum[J].European Journal of Biochemistry,1994,224:379-385.
[20]Coughlan M P,Ljungdahl L G.Comparative biochemistry of fungal and bacterial cellulolytic enzyme systems[M]//Aubert J P,Beguin P,Millet J.(eds)Biochemistry and Genetics of Cellulose Degradation.FEMS Symposium No.43.Academic Press,London,1988:11-30.
[21]Coughlan M P,Tuohy M A,Filho E X F,et al.Enzymological aspects of microbial hemicellulases with emphasis on fungal systems[M]//Coughlan M P,Hazlewood G.P.(eds.)Hemicellulose and Hemicellulase.Portland Press,London,1993:53-84.
[22]Coughlan M P,Hazlewood G.P.P-l,4-D-Xylan--degrading enzyme systems:biochemistry,molecular biology and applications[J].Biotechnology and Applied Biochemistry,1993,17:259-289.
[23]Coughlan M P.Towards an understanding of the mechanism of action of main chain-hydrolysing xylanases[M]//Visser,J.,Beld-man,G.,Kusters-van Someren,M.A.and Voragen,A.G.J.(eds)Xylans and Xylanases.Progress in Biotechnological,Elsevier,Amsterdam,The Nether1ands,1992:111-139.
[24]Dvorakova J.Phytase:sources,preparation and exploitation[J].Folia Microbiology,1998,43:323-338.
[25]Eriksson K E,Wood T M.Biodegradation of cellulose[M]//Higuchi,T.(ed.)Biosynthesis and Biodegradation of Wood Components,Academic Press,New York,1985:469-503.
[26]Frederick M M,Xiang C H,Frederick J R,et al.Purification and characterization of endo-xylanases from Aspergillus nicer.I.Two isozymes active on xylan backbones near branch points[J].Biotechnology and Bioengineering,1985,27:525-528.
[27]Gilbert H J,Hazlewood G.P.Bacterial cellulases and xylanases[J].Journal of General Microbiology,1993,139:187-194.
[28]Giligan W,Reese E T.Evidence for multiple components in microbial cellulases[J].Canadian Journal Microbiology,1954,1:90-07.
[29]Ha N C,Oh B C,Shin S,et al.Crystal structures of a novel,thermostable phytase in partially and fully calcium-loaded states[J].Nature Structural&Molecular Biology,2000,7:147-153.
[30]Khandke K M,Vithayathil P J,Murthy S K.Purification of xylanase,β-glucosidase,endocellulase,and exocellulase from a thermophilic fungus,Thermoascus aurantiacus[J].Archives biochemistry and Biophysics,1989,274:491-500.
[31]Klyosov A.Trends in biochemistry and enzymology of cellulose degradation[J].Biochemistry,1990,29:10577-10585.
[32]Liu Q,Huang Q,Lei X G,et al.Crystallographic snapshots of Aspergillus fumigatus phytase,revealing its enzymatic dynamics[J].Structure,2004,12:1575-1583.
[33]Maenz D D.Properties of phytase enzymology in animal feed[M]//Bedford,M.R.and Partridge,G.G.(editors),Enzymes in Farm Animal Nutrition.CABI publishing,United Kingdom,2001:66-79.
[34]Marquardt R R,M.Bedford.Future trends in enzyme research for pig appplications.In:Enzymes in Farm Animal Nutrition[M].Marquardt,M.R.and G.G.Bedford(Eds).Finnfeeds International,Wiltshire,United Kingdom.Published by CAB International,2001:299-305.
[35]Rani D S,Nand K.Purification and Characterisation of Xylanolytic Enzymes of a Cellulase-free Thermophilic strain of Anaerobe Clostridiumabsonum CFR-702[J].Anaerobe,2001,7:45-53.
[36]Reese E T,Si R G.H,Levinson H S.The biological degradation of soluble cellulose derivatives and its relationship to the mechanism of cellulose hydrolysis [J].Journal Bacteriology,1950,59:485-497.
[37]Sapag A,J.Wouters,C.Lambert,et al.Eyzaguirre and E.Depiereux,The endoxylanases from family 11:computer analysis of protein sequence reveals important structural and phylogenetic relationship[J].Journal of Biotechnology,2002,95:109-131.
[38]Shin S,Ha N C,Oh B C,et al.Enzyme mechanism and catalytic property of beta propeller phytase[J].Structure,2001,9:851-858.
[39]Simpson H D,Haufler U R,Daniel R M.An extremely thermostable xylanase from the thermophilic eubacterium Thermotogd[J].Biochemical Journal,1991,277:413-417.
[40]Witerhalter C,Liebl W.Two extremely thermostab1e xylanases of the hyperthermophilic bacterium Thermotogd mdritimd MSB8[J].Applied and Environmental Microbiology,1995,61:1810-1815.
[41]Wong K Y,Tan L U L,Saddler J N.Functional interactions among three xylanases from Trichoderma harzianum [J].Enzyme and Microbial Technology,l986,8:617-622.
[42]Wood T M,McCrae S I.The cellulase of Penicillium pinophilum:synergism between enzyme components in solubilizing cellulose with special reference to the involvement of two immunologically distinct CBHs[J].Carbonate Research,1986,234:93-99.
[43]Wood T M.Properties of cellulolytic enzyme systems [J].Biochemical Society Transactions,1985,13:407-410.
[44]Wood T M.Preparation of crystalline,amorphous,and dyed cellulase substrates[M]//Wood W A,Kellogg S T.(eds).Methods in Enzymology.VO1.160.Academic Press,London,1988:19-25.
[45]Wood T M.Microbial enzymes involved in the degradation of the cellulose component of plant cell walls[M]//Rowett Research Institute Annual Report,1992:10-24.
[46]Wood T M,McCrae S I,Bhat K M.The mechanism of fungal cellulose action.Synergism between enzyme components of Penicillium pinophilum cellulose in solubilizing hydrogen bond ordered cellulose[J].Biochemical Journal,1989,260:37-43.
[47]Wood T M,McCrae S I,Wlson C,et al.Aerobic and anaerobic fungal celluloses with special reference to their mode of attack on crystalline cellulose [M]//Aubert J P,Beguin P,Millet J.(eds)Biochemistry and Genetic of Cellulose Deglutition.FEMS Symposium No.43,Academic Press,London,1988:31-52.
[48]Wood T M,Wlson C A,McCrae S I.Synergism between components of the cellulase system of the anaerobic rumen fungus Neocallimastix frontalis and those of the aerobic fungus Penicillin pinophilum and Trichoderma koningi in degrading crystalline cellulose[J].Applied Microbiology and Biotechnology,1994,41:257-261.
[49]Xiang T,Liu Q,Deacon A M,et al.Crystal structure of a heat-resilient phytase from Aspergillus fumigatus,carrying a phosphorylated histidine[J].Journal of Molecular Biology,2004,339:437-445.[50]Yoshioka H,Nagato N,Chavanich S,et al.Purification and properties of thermostable xylanase from Talaromyces by ssochlamydoides[J].Agricultural Biological Chemistry,1981,45:2425-2432.
