自制电凝聚反应器降解活性艳蓝KN-R的因素研究
2011-01-31刘钊
刘钊
(武汉纺织大学环境工程学院,湖北 武汉 430200)
1 引言
电凝聚法处理印染废水是常用的处理方法之一,本研究采用的反应器是在传统设备基础上,综合考虑电极钝化等因素自行改进设计的[1,2]。活性艳蓝KN-R模拟染料废水为处理对象。考察了电解时间、电解质的浓度、电流密度和搅拌速率对降解效果的影响,得到了该反应器最佳反应条件。
2 材料与方法
2.1 实验装置
实验用装置为自制环流多段式型电凝聚器,装置示意图如图1所示。

图1 电凝聚槽示意图
2.2 实验方法
用蒸馏水配置成浓度为100mg/L的模拟KN-R废水,采用单因素优化实验方法考察电流强度、通电时间、搅拌速度、电解质NaCl投加量对脱色率和CODCr的去除率的影响。为确保每次实验条件的一致性,实验完毕均用稀硫酸浸洗反应器。
3 实验结果分析
3.1 电流强度的影响
分别用电流强度2A,4A,6A,8A,10A对100mg/L的KN-R模拟废水进行处理,将搅拌速率控制在V=50r/min,调节p H=7,倒极频率60s/次,NaCl投加量为2g/L,出水静置30min后取上清液,CODCr随反应时间的降解率如图2所示。
由图2发现:对于一定大小的电极板,搅拌速率一定的情况下,电流强度大小决定了单位时间内电解出铝离子、氧气、氢气的速率及电极表面氧化还原反应的能力的大小。随着电流强度增大,在反应时间到达40min时,CODCr的去除率越大;电流强度越大,单位时间内电解产生的Al3+的数量越多,形成的Al(OH)3水合胶粒越多,所能絮凝的染料分子量越多,CODCr在相同时间内降解的速率越快。
不同的电流强度下,CODCr的降解速率最快阶段出现的时间不同。电流强度越大,出现这个阶段的时间越早;电流强度越小,这个阶段越晚,电流强度为2A时,至设定反应时间结束时,仍未出现降解速率最快阶段。
电流强度越大,对水及电解质NaCl的电解氧化作用越明显,因而相同时间内,产生的 O3-、HClO、ClO-速率越快,所能氧化断键的染料分子水量越多。因为电凝聚过程中,从开始电解出铝盐离子到溶液中存在大量Al(OH)3胶体是一个水解反应平衡过程,最基本的水解方程式如下:
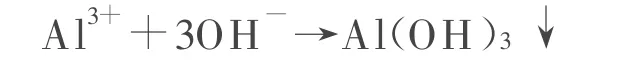
当电流强度越大时,越能缩短溶液内满足Al(OH)3达到最大浓度时所需Al3+浓度的时间,越能缩短最快反应速率出现时间。图2的结果显示,选用8A或10A电流强度时,色度去除率在反应25min时均能超过90%,CODCr去除率在反应进行到30min时都在60%左右,相差不大,故从经济角度考虑,在保证一定出水水质情况下,选用8A电流强度处理100mg/L的KN-R模拟废水是合理的。
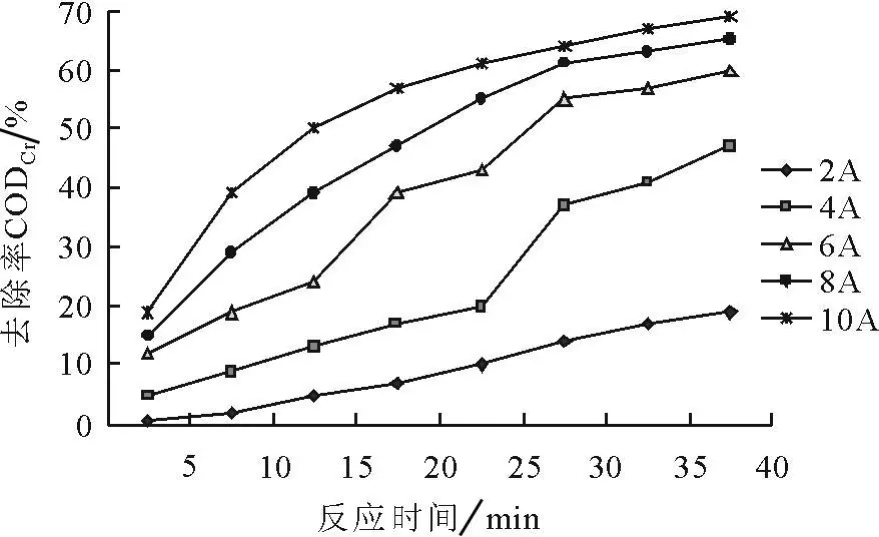
图2 电流强度对CODCr去除率的影响
3.2 通电时间的影响
选用8A电流强度,pH控制为7,搅拌速率调节为50r/min,NaCl投加量控制在2g/L,倒极频率60s/次,对100mg/L的KN-R模拟染料废水进行处理,定时取样,静置30min,测得通电时间对模拟废水色度及CODCr去除率影响如图3所示。
由图3可知,在电解初期色度和CODCr去除速率都比较快,到了电解后期降解速率趋于平缓。随着电解的进行,溶液内絮体浓度越来越大,析氧反应加快,同时由于溶液中染料分子浓度降低,分子间发生碰撞的几率较前期大大降低,反应速率降低,随着氧化反应的深入,溶液中残余的小分子氧化电位可能升高,氧化反应所需的活化能增大,降解速率降低。色度去除率在反应进行到25min就达到了93%,此时CODCr去除率达到 55%,继续反应时,去除率变化速率变慢。达到30min以后,两项指标降解速度较慢,为提高出水效果,将反应时间确定为40min。
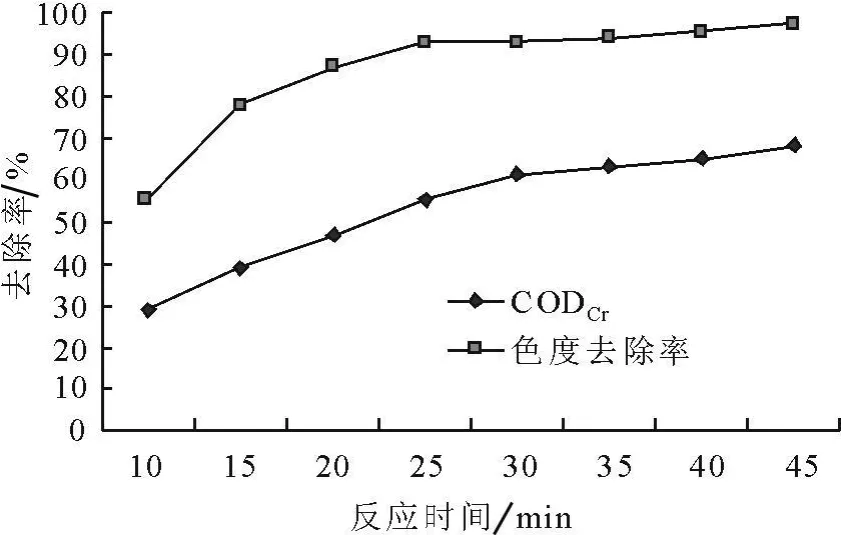
图3 通电时间对CODCr和色度去除率的影响
对实验结果进行数学分析,发现对于100mg/L的KN-R模拟染料废水,采用8A恒电流直流电电凝聚时,CODCr和色度去除率随反应时间遵循以下二级模拟反应动力学,相关性较好,相关系数分别为0.9862和0.9531。CODCr模拟反应动力学方程为:

色度模拟反应动力学方程为:
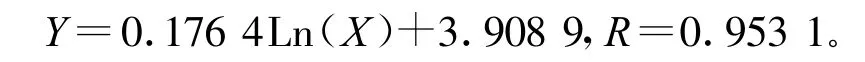
3.3 电解质投加量的影响
控制反应电流强度为8A,将搅拌速率控制在V=50r/min,调节 pH=7,倒极频率60s/次,对初始质量浓度为100mg/L的KN-R模拟染料废水进行降解,反应时间控制为40min,分别投加 0g/L、1g/L、2g/L 、4g/L 、8g/L 的 NaCl电解质,出水静置30min,考察电解质NaCl投加量对色度和CODCr去除率的影响如图4所示。

图4 NaCl投加量对CODCr和色度去除率的影响
图4表明:随着反应水样中NaCl浓度从0g/L增加到2g/L,反应液中Cl-浓度随之增大,单位时间内被电极电解生成的具有强氧化性HClO、ClO-的量增大,氧化断键的染料分子的量也增多,造成CODCr和色度的去除率增大;当NaCl浓度进一步提高时,CODCr和色度的去除率并没有明显增加趋势。由此可判定2g/LNaCl浓度为该种反应器降解低浓度染料废水最佳浓度。
NaCl投加量的对降解效果的影响主要有以下原因:一方面,在一定浓度范围内,NaCl浓度的增大能够提高电极板上析氯电位。析氯电位随着Cl-浓度的增加而降低,活性氯的量随之而增多,使得反应器对染料分子间接氧化能力增强;同时Cl-浓度的增加,使阳极上的吸附竞争加强,副反应减弱,因而使脱色率升高。但当 NaCl浓度较高时,产生的活性氯足够多,Cl-在阳极上的吸附也基本达到饱和,继续增大NaCl浓度,染料的降解情况就不明显了。另一方面,由于NaCl的存在,电解产生的氯氧化物能够及时与电极表面的附着膜层发生反应,削弱极板钝化作用,延长了反应的有效时间。
3.4 搅拌速率的影响
调整进水NaCl浓度为2g/L,电流强度保持8A恒定电流,调节pH=7,搅拌桨搅拌速率分别采用为 0r/min、20r/min、50min/min、80r/min、100r/min,出水静置30min,对浓度为 100mg/L的KNR模拟染料废水进行40min降解,定时取样,考察搅拌速率CODCr的影响如图5和图6所示。
从图5观察发现:当搅拌速率为0时,色度去除率随时间按增加平缓,达到40min反应终点时,色度去除率为61%;搅拌速率为20r/min时,色度去除率较 0r/min稍高,反应终点时,色度去除率为86%;搅拌速率为50r/min或80r/min时,色度去除率上升很快,到达 25min时为93%左右。反应继续,80r/min的搅拌速率条件下的脱色率能继续缓慢上升,50r/min则保持不变;而采用100r/min的高搅拌速率时,反应前期,脱色率上升速度快效率高,在20min达到最高点,随后脱色率出现了急剧下降趋势,30min后又趋于平缓。
从图6发现:CODCr的去除率与搅拌速率的关系变化与色度去除率相类似,所不同的是采用80r/min搅拌速率时,CODCr的去除率要比采用50r/min搅拌速率高出5%。
对于染料浓度、NaCl浓度一定的染料溶液,其溶液中Cl-浓度是相同的;采用固定的电流强度降解时[3],其电极上氧化还原电位也是相同的,然而采用不同搅拌速率时,出水的色度和CODCr的去除率差别巨大,推测其原因为:一方面,采用不同搅拌速率时,电极板表面电解离子的传质速率不同,搅拌速率越快,传质速率越高,由电解平衡原理知电极表面多溶解的铝盐越多,产生的具强氧化性的氯氧化合物越多,单位时间内通过吸附、氧化手段降解染料分子越多;另一方面,搅拌造成的水力紊流能提高染料分子与强氧化性分子反应的几率,提高小分子染料与Al(OH)3水合胶粒的结合概率。搅拌速率越快,提升的效果越明显。但是,当电极表面溶解铝盐速度达到饱和以后,过高的搅拌速率对提高电解作用效果不再明显,过大的水力紊流反而会把凝聚成团的絮体打碎,导致出现处理效果回落的现象。
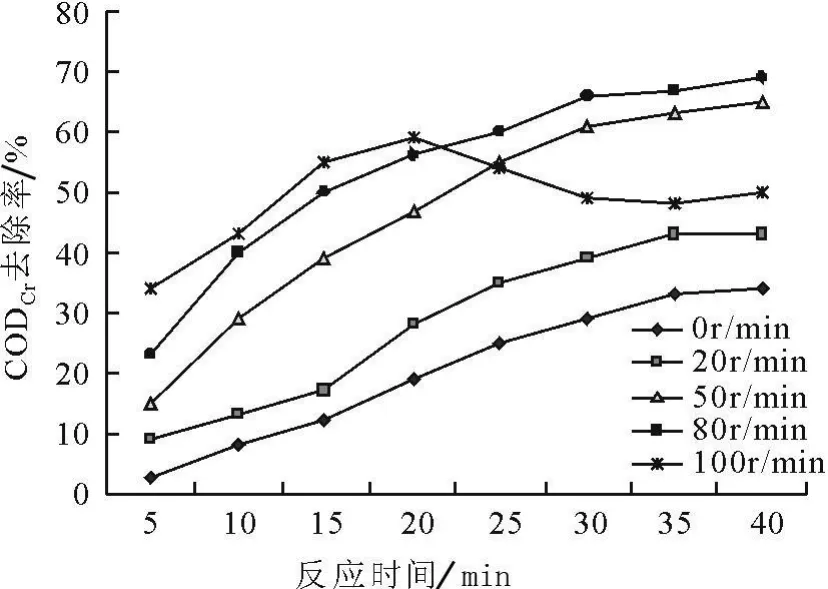
图5 搅拌速率对CODCr去除率的影响
不同搅拌速率所形成的絮体大小、密度存在较大差异,导致出水絮体的沉降性能也存在较大差别,不同的搅拌速率下,反应40min,取出水测定出水浊度,然后静置10min,再次测定浊度,按下列公式计算絮体沉降率,得到搅拌速率与絮体沉降率关系如图6所示。


图6 搅拌速率对絮体沉降率的影响
从图6可以看出,采用80r/min时,所得絮体沉降率最好,10min达到83%;采用过低搅拌速率0r/min时,所得絮体沉降性能最差;过高搅拌速率100r/min时,出水的絮体沉降性能也不佳。出现这些情况的原因可能为:过低的搅拌速率导致絮体碰撞几率小,力度不够,形成絮体小而蓬松,不易沉降;过高的搅拌速率虽增大了絮体碰撞几率[4],但过大的水力剪切力会打碎已有的钒花,使絮体体积小,难沉降;只有适宜的搅拌速率能使絮体易抱团、压实,具有好的沉降性能。综合考虑处理效果和絮体沉降性能,80r/min搅拌速率为最佳搅拌速率。
4 结语
通过上述的试验研究,确立了各项因素的最佳条件如下。
(1)降解初始质量浓度为100mg/LKN-R的模拟染料废水时,最佳电流强度I=8A,最佳通电时间t=40min,最优搅拌速率V=80r/min,最佳倒极频率为60s/次,最佳NaCl浓度为2g/L。
(2)在最佳条件下,CODCr和色度去除率分别达到68.8%和98%。
(3)采用8A恒电流直流电电凝聚时,CODCr和色度去除率随反应时间遵循以下二级模拟反应动力学,相关性较好,相关系数分别为0.9862和0.9531。
[1]王 娟,陆雍森,赵大传.活性染料废水的电解絮凝预处理研究[J].给水排水,2005,31(2):51~54.
[2]刘增超,刘文辉,郑先俊.电絮凝-气浮法对印染废水脱色的实验研究[J].工业安全与环保,2007,33(4):8~10.
[3]Tunay O , Kabdasli I , Eremektar G , et al.Color removal from texi-tile waste water [ J] .Water Science Technology , 1996 , 34(11):9~16 .
[4]丁忠浩.有机废水处理与应用[M].北京:机械工业出版社,2006.
