骨科植入器械国内外标准比较分析
2011-01-26丁彪李元超
【作 者】丁彪,李元超
1 上海市医疗器械检测所,上海,200070
2 上海交通大学,机械与动力工程学院,上海,200240
骨科植入器械是人体骨骼替代、修复、补充及充填的一大类植入器械的统称,用于人体骨骼的维持、支撑和修补,是目前临床使用较为普遍的骨科用医疗器材。骨科植入器械包括:创伤、人工关节、脊柱内固定器和融合器、骨修复材料等。这些植入器械的使用,解决了许多临床技术难题,使骨科疾病治疗水平不断提高,广大患者获得了较好的治疗效果。据中国医疗器械行业协会外科植入物专业委员2010年会信息统计,至2010年,我国骨科植入器械的使用量已超过100多亿元。但近年来骨科植入器械的不良事件也逐年上升[1]。
据国家药品不良反应监测中心统计,自2002年12月至到2007年3月31日止,中心共计收到与骨科植入器械有关的疑似不良事件报告786份,占国家医疗器械不良事件数据库中疑似不良事件报告数量的8.4 %。可能发生的原因包括:患者不遵医嘱,过早负重;引起此类事件选材不当;产品质量方面的原因等[2]。
这些不良事件的发生与植入器械固有的风险有关,更与我国目前对植入器械的设计、试验、研究、管理及认识密不可分,而植入器械的设计、试验、管理等又与植入器械的标准紧密相连。目前我国标准研究水平落后于国际先进水平、标准引进的不完整,临床使用中缺乏足够的生物力学方面认识及植入器械风险意识得不到足够的重视和普及。本文就国内外现有骨科植入器械标准做一比较分析。
1 国内外骨科植入器械标准
1.1 国内标准
国内骨科植入器械标准由全国外科植入物和矫形器械标准化技术委员会(SAC/TC110)归口(注1——某些植入器械标准并不归口于SAC/TC110,如GB/T 13810-2007《外科植入物用钛及钛合金加工材》等),截至2010年9月,等同采用、修改采用、非等效采用国际以及国外先进国家标准共55份。其中通用及专用标准7份,测试方法标准10份,材料标准24份,产品标准14份(创伤类12份、关节类2份),国际及国外先进国家标准的采标率89.0%。强制性标准17份,推荐性标准38份。标龄在5-10年的标准14份,占25.5%,标龄5年以下的标准41份,占74.5%,如图1所示。仅2008年和2009年就制修订骨科植入器械标准24份,全部为推荐性标准。说明全国外科植入物和矫形器械标准化技术委员会近年来加大了骨科植入器械标准的制、修订力度,积极引进国际标准或国外先进国家的标准。这种措施有效缩短了本国标准与国际标准之间的距离。
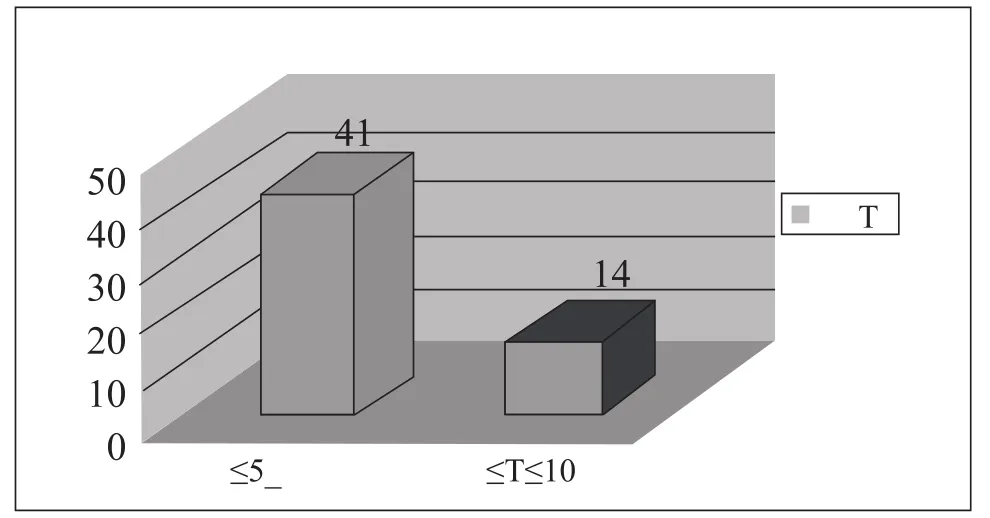
图1 国内骨科植入器械标龄统计Fig.1 Statistics of years of domestic standards on Orthopedic implants
1.2 国际ISO标准
ISO国际标准组织制、修订骨科植入器械标准的为外科植入物标准化技术委员会(ISO/TC150 ),下设“材料(Materials)”分技会(ISO/TC150/SC1)、“骨接合和关节置换(Bone and joint replacements)”分技会(ISO/TC150/SC4)与“骨结合和脊柱器械(Osteosynthesis and spinal devices)”分技会。截至2010年9月,共出版标准91份,正在制、修订的标准17份。其中通用和专用标准10份、材料标准30份,测试方法标准28份,产品标准22份。标龄5年以下的有32份,占35.2%,5年以上、10年以下的有23份,占25.3%,10年以上的有36份,占39.5%。如图2所示。
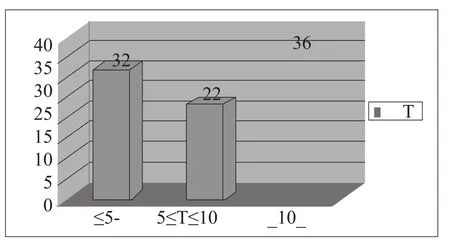
图2 国际骨科植入器械标龄统计Fig.2 Statistics of years of international standards on Orthopedic implants
1.3 美国ASTM标准
美国材料与试验标准协会ASTM对骨科植入器械标准的制修订倾注了极大的热情,一直走在世界各国的前列。到目前为止,共发布骨科植入器械有关的现行标准共158份。其中材料标准57份,涉及不同材料成分、相同材料成分不同型材、相同材料相同型材但不同加工工艺的材料要求与试验方法;试验方法标准97份,涉及植入器械单一产品各物理性能的试验方法,植入器械表面修饰要求,(电)化学性能,组件的匹(装)配性能,动态器械的疲劳性能、磨损性能以及生物学评价方法等,几乎涵盖了骨科植入器械所有性能要求的测试方法;产品标准4份。
1.4 其他
德国和英国大多采用国际标准,尤其是对一些关键性指标,如植入器械组件的匹(装)配性能,动态机械的疲劳性能、关节磨损性能、(电)化学性能以及生物学评价方法等均采用ISO标准。加拿大则大多采用美国ASTM标准。
2 国内外骨科植入器械标准的主要差异
2.1 国内标准的数量少
我国现行骨科植入器械标准共55份,仅为ISO现行骨科植入器械标准91份的60%,与ASTM现行骨科植入器械标准相比,仅为34.8%。其中,ISO制定的骨科植入器械通用要求、专用要求以及大部分材料标准已同等采用或修改采用转化成我国国内标准,而与骨科植入器械相关的性能要求标准转化较少。这与我国在骨科植入器械方面的科研基础比较薄弱以及相关实验设备的研制落后有很大的关系。因此国内标准并未全部涵盖骨科植入器械产品的各个质量方面的问题,使得企业对于产品生产质量控制存在阻碍。
2.2 植入器械关键性能标准引入较少
2007-2009年通过加大标准的引进力度,我国医疗器械材料标准基本与国际ISO标准接轨,反映在大多数的医疗器械材料都有标准进行规范,而且等同采用ISO标准。通用要求标准以及骨科植入器械的专用要求标准也基本与ISO标准接轨。但在欧美国家产品注册中必须考虑的一些关键性性能标准缺失较多,尚未有相应的国家标准如骨科植入器械的疲劳性能、匹配性能、关节的磨损要求等。某些骨科产品重要多种性能指标例如髋关节假体的试验如图3所示,至少要求12种测试,其中,股骨柄组件疲劳性能(ISO 7206-4:2010)和施加扭转的股骨柄组件疲劳性能(ISO 7206-8:1995)、股骨柄组件头部和颈部区疲劳性能(ISO 7206-6:1992)、模块化股骨头静态负荷强度(ISO 7206-10:2003)、髋关节的磨损性能(ISO 14242-1:2002,ISO 14242-2:2000)须由指定的专业实验室完成。标准中对于测试样品和对照样品的数量、间距、施加的载荷、角度、频率等都进行了详细的规定,甚至对夹具的材料也有明确的规定(ASTM F1717-04)。德国髋关节磨损实验室如图4所示。
2.3 翻译中存在一些问题

图3 髋关节植入器械测试方法和标准Fig.3 Standard testing methods on joints prostheses

图4 德国EndoLab髋关节磨损实验室Fig.4 Wear laboratory of EndoLab,Germany
如标准GB/T 13810-2007《外科植入物用钛及钛合金加工材》(参考引用ISO 5832-2、ISO 5832-3、ASTM F67、F136、F1472)则“在化学成分和显微组织等指标均等同于ISO5832的要求”情况下,将氢含量的规定为应不大于0.010%,提高了要求,增加了企业的生产成本。ISO 5832-2、5832-3 和 ASTM F67、F136、F1472规定:氢的含量为不大于 0.0125 或 0.015 (m/m)。关于氢的成分规定特别注明,坯料的氢成分应为 0.010% (质量比),而其加工材规定为0.015%(Except for billets,for which the maximum hydrogen content shall be 0.010% (mass fraction) )。
2.4 髋关节的磨损标准
2008年发布了YY/T 0651.1-2008《外科植入器械 全髋关节假体的磨损 第1部分:髋关节磨损试验机的负载和位移参数及相关的试验环境条件》(ISO 14242.1-2002,MOD)和YY/T 0651.2-2008《外科植入器械 全髋关节假体的磨损 第2部分:测量方法》(ISO 14242.2-2002,IDT)。但到目前为止,我国没有一家科研或检验机构有能力进行髋关节磨损试验,更没有相应的磨损试验数据库。假体关节运动部位的磨损,近年来为世界各国研究的重点,美国、英国、德国等不仅建立了大量的关节磨损数据库,不断改进试验设备,并且对磨损的部位、磨粒的尺寸分布、形态等对骨细胞的吸收、激活机理做了大量的工作[7]。我国磨损标准的推出,尚未进行真正意义上的验证。这反映了我国基础研究水平较差,缺乏足够的技术数据支撑。
3 讨论与展望
通过以上对比分析,我们可以看到我国骨科植入器械标准的一些不足。就以我国现阶段的骨科植入器械标准,还远远不能满足产业的发展和政府的监管的需求,更不能与国际水平接轨。因此,笔者建议可以采取以下措施来完善我国的骨科植入器械标准。
3.1 不断补充和完善骨科植入器械标准体系
通过标准的制修订工作,不断提高标准的质量,借鉴国际标准以及先进国家的标准管理模式,逐步建立适合我们国家的标准体系。
3.2 设立专项资金提高验证能力
3.2.1 骨科植入器械产品标准的制定涉及到大量性能试验的验证工作,其中多数试验设备属于骨科植入器械产品的专用设备,如疲劳试验机、模拟磨损试验机,这些设备的设计和制造技术仅被极少数发达国家公司掌握,因此设备引进和对使用人员的培训需要花费大量的费用和精力,无形中增加了标准验证及制定的成本和难度。建议国家或地方能给与专项资金的资助以提高标准的验证能力。
3.2.3 目前大多数国际标准主要注重对产品设计属性、预期性能的规范,但并未统一规定这些性能参数的可接受水平,这给我们评价产品的安全性、有效性带来了很大的困难。因此需要我们具备较高的技术水平,在工作中积累丰富的试验数据,同时构建已上市产品相关性能的数据库,从而科学地建立产品性能的评价体系。
3.3 鼓励国内企业积极开展产品的研究和开发
3.3.1 鼓励国内企业积极开展产品的研究和开发,从“以仿为主”到“仿创结合”,从“通用产品”到“个性化设计”,对原有产品在原材料、生产加工、制作工艺等环节有针对性进行改进,不断完善产品结构,优化产品性能,提高产品质量。
3.3.2 引导企业参与国内外标准化活动,加强与国内外先进技术的交流,掌握最新动态和发展趋势,提高自身的管理和技术能力。同时也提高我国技术人员在国际标准化工作中的话语权。
3.4 积极与科研单位合作,转化科研成果
我国许多科研单位在骨科植入器械的个性化设计、加工、转化以及失效等方面进行了研究,取得了不少成果。中国人在生活习惯等方面有自己特点,各相关部门积极合作,研究和设计符合中国人习惯和特点的骨科植入器械,并制定相应的标准,使国人享受更美好的生活功能。
[1] 邱贵兴. 骨科植入物医疗器械不良事件检测[J]. 药物警戒, 2005,2(1):23-24
[2] 黄嘉华, 姚天平, 丁彪等. 科植入物失效分析[J]. 中国医疗器械杂志, 2011, 35(1): 32-37
[3] GB 4234-2003《外科植入物用不锈钢》(ISO 5832.1-1997, MOD)[4] GB 24627-2009《医疗器械和外科植入物用镍-钛形状记忆合金加工材》(ASTM F-2063-05, IDT)
[5] YY 0117 系列标准, YY 0117.1—2005《外科植入物骨关节假体锻、铸件 Ti6Al4V 钛合金锻件》(ISO 5832-3:1996,MOD)
[6] YY/T 0605系列标准,0605.6—2007《外科植入物 金属材料 第6部分: 锻造钴-镍-铬-钼合金》(ISO 5832.6-1997, IDT)
[7] 林秾, 人体髋关节假体磨损微粒的研究进展. 医学研究生学报[J]. 2002, 15: 276-278
