富钒酵母中钒化学测定方法探讨*
2011-01-24孙宗强徐二丹张显忠
孙宗强 徐二丹 张显忠
(1.泰山医学院2008级生物工程本科,山东 泰安 271000;2.泰山医学院,山东 泰安 271000)
钒是人体一种必需的微量元素,令人兴奋的是钒的类胰岛素的作用[1]。但无机钒对人体安全范围小,且吸收不好[2],因此很多人在用微生物富集钒以将无机钒转化为有机钒而降低无机钒对人体的毒性,且用酵母富钒的研究报道少见[3,4]。钒的测定方法有电感耦合等离子体原子发射光度法[5]、石墨炉原子吸收光谱法[6]、富氧空气-乙炔火焰原子吸收光谱法[7]等,均操作复杂或费用很高。而化学法测定富钒酵母中的钒尚未见报道。根据4-(2-吡啶偶氮)-间苯二酚(PAR)能与钒生成红色复合物原理,经反复实验探索,得到具有较高的特异性和灵敏度,操作简单、费用低廉的成熟操作方法。
1 材料和方法
1.1 材料:
1.1.1菌源:从安琪活性干酵母中经活化分离出来的酵母菌。
1.1.2试剂和仪器
种子活化培养基:5%蔗糖; 固体培养基(PDA):20%土豆,2%葡萄糖 ,2%琼脂; 液体摇瓶培养基(PDA):20%土豆 ,2%葡萄糖; 偏钒酸钠; 4-(2-吡啶偶氮)-间苯二酚(PAR); 亚硒酸钠; 硝酸铝; 重铬酸钾; 醋酸铅; 钼酸钠; 硫酸亚铁; 浓硝酸; 高氯酸; 冰乙酸; 乙酸钠。
V-1100D可见分光光度计;DNP-9162BS-Ⅲ电热恒温培养箱等。
1.2 方法
1.2.1纯酵母培养 菌种活化培养基活化,然后平板分离的纯菌株接于液体培养基中,摇瓶培养36小时,28 ℃,120 r/min得纯酵母。
1.2.2富钒酵母培养 按100 ml加50 μl的量,向液体培养基中加入偏钒酸钠(浓度为100 mg/ml),28 ℃,120 r/min摇瓶培养36小时,用蒸馏水离心洗涤三次,置干燥箱中,50 ℃干燥36小时备用。
1.2.3标准曲线绘制 称取纯酵母粉0.1 g置于蒸馏烧瓶中,加入偏钒酸钠(100 mg/ml)20 μl。加入浓硝酸2 ml,高氯酸钾0.2 ml。低温回流加热至浅黄色澄清,150 ℃加热使其白烟冒尽,几近蒸干,冷却,用缓冲液(HAc-NaAc pH 4.5)定容到100 ml。
取消化后样品0.1、0.2、0.3、0.4、0.8、1.2、1.6、2.0、2.4、2.8 ml两组,分别补足缓冲液到8ml,一组加入0.8 ml PAR,另一组不加PAR的体系为空白对照。混匀室温放置5分钟,在560 nm处测其吸光度。绘制标准曲线。
1.2.4富钒酵母中钒含量的测定 取富钒酵母同上法消化,冷却用缓冲液(HAc-NaAc pH 4.5)定容到50 ml。取消化液1 ml,加缓冲液7 ml,混匀,加PAR0.8 ml,混匀,室温放置5 min,用不加PAR的空白管调零,在560纳米波长比色获得OD值,查标准曲线即得钒的含量。
2 结果与讨论
2.1 标准曲线的绘制
在偏钒酸钠0-8μg/ml时有很好的相关性,相关系数为0.999。(见图1)

图1 标准曲线
2.2 PH对显色的影响
取消化液1mL,调节pH到2、3、3.5、4.5、5.5、6.5、7定容到8 ml,加入PAR 0.2 ml测其吸光度。
在pH 4.5时出现最大显色吸光度(见图2),故实验采用缓冲液(pH 4.5)稳定pH,以达到最佳实验效果。

图2 pH对显色的影响
2.3 温度对试验方法的影响
温度梯度设为25 ℃、30 ℃、40 ℃、50 ℃、60 ℃ ,取1 μg/ml偏钒酸钠溶液加入0、1、2、3、4、5、6 ml,PAR 0.8 ml。测其吸光度。

图3 温度对试验方法的影响
温度在25~60 ℃能够呈现很好的线性关系(见图3),其中涵盖常温,故本实验中选择在常温下来测定。而温度达到70 ℃时吸光度明显下降,同时线性关系变差,故实验不应在较高温度下进行。
2.4 PAR对显色的影响
方法同上2.3,pH调至4.5,分别加入PAR 0.2、0.4、0.6、0.8、1.0 ml,测其吸光度以确定最适量。
在PAR加入量在0.8 ml及以上时吸光度上升微小且趋于平坦(见图4),因此本实验选用在8 ml体系中加入0.8 ml PAR。

图4 PAR对显色的影响
2.5 显色的稳定性
取1 ml消化后标准溶液,加入7 ml缓冲液,加入PAR0.8 ml。以不加PAR的为空白对照。在3小时吸光度并未有明显变化(见图5),实验呈现较好的稳定性。过夜后呈现明显的下降,且取出后发现红色沉淀,故在测定时不能放置过夜。

图5 显色的稳定性
2.6 方法特异性检验
每组分别加入偏钒酸钠、亚硒酸钠、硝酸铝、重铬酸钾、醋酸铅、钼酸钠、硫酸亚铁(均为1 μg/ml)溶液0、1、2、3、4、5、6、7、8 ml,然后补水(缓冲液)到8ml,加入PAR 0.8 ml,稍静置测其吸光度。有较好的特异性,但对于硫酸亚铁有较好的相关性(见图6)。因此在后续反应中,不应人为加入亚铁离子和硫酸根离子。
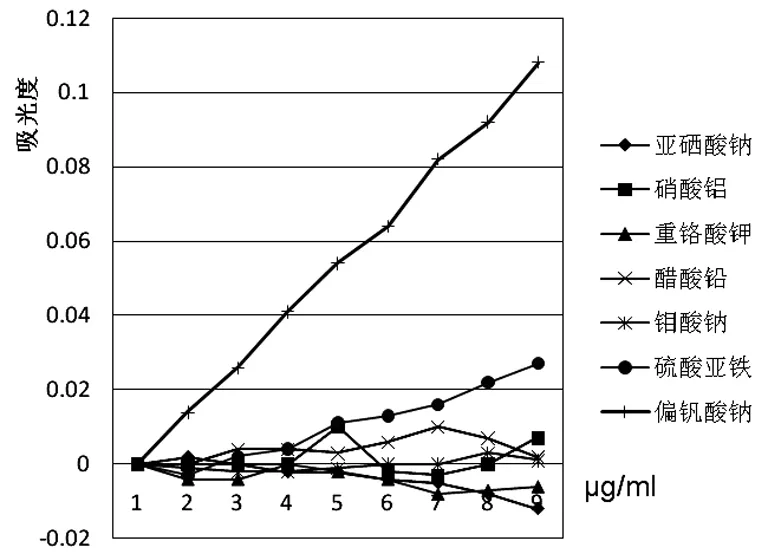
图6 方法特异性检验
2.7 方法回收率测定
分别取3 ml、4 ml、5 ml、6 ml样品两组,均补足缓冲液到8 ml。其中一组加入PAR 0.8 ml,另一组未加PAR的作为空白对照。测其吸光度,计算含量。以3 ml数据为样本统计回收率,回收率95.0~103.1%(见表1)。

表1 回收率检验
3 结 论
本实验分别从pH、温度、PAR用量对实验的影响、实验的特异性及回收率多个方面对富钒酵母中钒化学测定方法进行了探究。结果表明: pH对实验影响较大,pH值在4.5时有很好的显色效果;温度对实验影响较小,在25~60 ℃这一较宽泛的温度范围内均有较好的实验效果;对显色剂PAR的量从显色及用量经济性上也存在一个上限值,在8 ml试验体系中,PAR最佳值为0.8 ml;特异性实验发现硫酸亚铁对实验有一定的影响,实验中应避免引入,相比之下其它离子对本实验几乎无影响;95.0%~103.1%的回收率完全能够满足实验要求。本实验较全面的探究了实验的各种影响因素,并进行优化设计,形成具有特异性和灵敏度俱佳、操作简单易行、成本低廉的方法,对钒的研究具有较高的应用价值。
[1] 李延红,张宏伟,徐荷,等.微量元素与糖尿病[J].上海预防医学杂志,2001,13(4):158-190.
[2] Patrick P, Subodh V, Marc D, et al. Vanadium and diabetes[J]. Molecular and Cellular Biochemistry, 1998,188:73-80.
[3] 张琛,李春如,樊美珍,等. 富钒酵母菌株的筛选及摇瓶培养条件的初步研究[J]. 安徽大学农业大学学报,2006,33(2):234-237.
[4] 张琛,李春如,樊美珍. 富钒酵母中钒含量的初步研究[J]. 食品与发酵工业,2009,35(6):37-39.
[5] 庞晓辉,禹洁丽. 电感耦合等离子体原子发射光谱法测定镍合金及铁合金中微量钒[J].分析仪器,2009,21(2):31-33.
[6] 侯明,胡存杰. 微波消解-石墨炉原子吸收光谱法测定土壤中微量钒[J]. 冶金分析,2009,29(1):25-29.
[7] 吴少尉,葛文,金平等. 富氧空气-乙炔火焰原子吸收光谱法测定地质样品中的钒[J]. 岩矿测试,2003,22(4):300-302.
[8] 沈含熙,王振清. 钼-水杨基荧光酮-溴化十六烷基三甲基铵显色反应的研究[J]. 高等学校化学学报,1982,3:300-303.
[9] 李子夏,贺茂勇.电感耦合等离子体原子发射光谱法测定龋齿牙釉质和牙本质中微量元素[J].理化检验-化学分册,2010,46(11):1250-1252.
