牡丹花的成分及应用研究进展
2011-01-09高亚辉张少文张淑霞陈复生
高亚辉 ,张少文 *,张淑霞 ,陈复生 ,万 珊
(1.洛阳理工学院 环境工程与化学系,河南 洛阳 471023;2.洛阳出入境检验检疫局,河南 洛阳 471003;3.河南工业大学 粮油食品学院,河南 郑州 450052)
牡丹花的成分及应用研究进展
高亚辉1,张少文*1,张淑霞2,陈复生3,万 珊1
(1.洛阳理工学院 环境工程与化学系,河南 洛阳 471023;2.洛阳出入境检验检疫局,河南 洛阳 471003;3.河南工业大学 粮油食品学院,河南 郑州 450052)
分析了牡丹花的各种化学成分及花色素的提取、性能及应用,阐述了牡丹花的营养保健作用、抗氧化性和对DNA氧化损伤的保护作用,指出了研究应用中存在的问题,提出了今后的研究方向.
牡丹花;成分;花色苷;抗氧化性
0 前言
牡丹素有“花中之王,国色天香”的美誉,象征着富贵吉祥,历来为世人所珍爱.广泛分布于河南洛阳、山东荷泽、安徽铜陵、陕西汉中、河北柏山、四川、甘肃、浙江等地.据统计,我国牡丹的种植面积已达2万hm2[1].目前,牡丹花除作为重要的观赏花卉之外,主要利用其根皮(即丹皮)作为中药材,由于受到花期和气候条件的限制,导致花开时经贸、旅游活动繁荣,花落时惨淡经营的不良局面,且受制于深加工技术落后,每年有大量的牡丹花白白地浪费掉.近年来,为了改变这种现象,许多专家学者先后对牡丹花的成分和应用性展开了全方位的研究,以期对牡丹花进行深度的开发利用,笔者对该方面进行了综合分析,为开发利用牡丹花,提高经济附加值提供了依据.
1 牡丹花的化学成分
1.1 挥发油成分
牡丹花挥发油已鉴定出49种成分[2],主要是含有天然香味物质,如香茅醇、香叶醇、芳樟醇等;同时还含有丰富的帖烯及烃类化合物,如十四烷酸、十六酸、3,7-二甲基 -2,6-辛二烯 -1-醇,3,3-二甲基 -双环[2,2,1]-庚烷 -2-酮等.周海梅等[3]用固相微萃取装置(SPME)顶空提取牡丹花的挥发性成分,通过分析10个品种的牡丹花,共检测出34种化学成分,其中多数是烷烃,且所含烷烃种类基本相同,但不同品种所含的天然香味物质如香茅醇、烯类、酯类等不同,导致其香味各异.这些天然化合物在食品、饮料及日用化工产品中可作为纯天然添加剂加以利用.
1.2 营养成分
通过牡丹花瓣中脂肪酸组成的定性和定量测定以及不同时期花瓣中脂肪酸组分和含量变化的研究表明[4]:花瓣中含有多种重要的高级脂肪酸,主要以棕榈酸(C16∶0)、亚油酸(C18∶2)和亚麻酸(C18∶3)为主.不饱和脂肪酸具有降低血脂,防止动脉硬化的功效,如亚油酸是人体必需脂肪酸,在人体内可以转变为花生四烯酸,对于合成磷脂,形成细胞结构,维持一切组织的正常功能,以及合成前列腺素,都是必要的.亚麻酸是人体重要的营养素,具有抑制肿瘤转移、降低冠心病发病率、提高免疫力等功效.刘建华等[5]对牡丹花中的蛋白质、脂肪、氨基酸、矿物质元素和维生素等营养成分进行分析测定,并与脱水蕨菜和脱水白菜的营养成分进行比较.结果显示:蛋白质、K、Ca、Mg、P、Se等元素及VB1、VB2和类胡萝卜素等含量较高,是一种较好的天然营养保健资源.史国安等[6]选5个牡丹花品种,采用紫外分光光度计、荧光分光光度计、氨基酸自动分析仪和原子吸收分光光度计,测定了牡丹花中多酚类物质、维生素、氨基酸和10种矿物元素的含量.结果表明:5个牡丹品种花瓣中含有丰富的多酚类物质、维生素、蛋白质和矿物质;所含氨基酸种类齐全,必需氨基酸和呈味氨基酸含量较高.用原子吸收光谱法测得牡丹花中主要含6种金属元素[7]:铜、铁、锌、锰、钴、镍,其含量分别为 54.53、19.16、29.98、3.71、1.15、0.25μg/g,这些是人体必需的微量元素.因此,从营养保健角度分析,牡丹花瓣具有较高的营养价值,是可利用的食疗资源.
2 牡丹花色素
2.1 牡丹花色素提取工艺
目前国内从牡丹花中提取色素的生产工艺主要有溶剂萃取法、超临界流体萃取法和酶法提取等.在实验室中超声波辅助萃取法、微波辅助萃取法也得到较好的应用.吴龙奇等[8]研究了牡丹花红色素提取过程的乙醇体积分数、盐酸体积分数、温度和浸取时间等操作条件的影响.结果显示,牡丹花红色素的合适浸取剂为1%HCl-C2H5OH溶液,浸取温度50℃,浸取3 h.该方法的不足之处在于成本高,提取速度慢.朱文学等[9-10]和刘耀玺等[11]改进了提取方法及工艺,将牡丹花、水和甲醇在不锈钢容器内加热后,经框板过滤机过滤,滤液置回收塔内加温回收甲醇至膏状,放干燥箱内烘干至水含量适中时取出,即为牡丹花色素.
2.2 牡丹花色苷结构及降解动力学
牡丹花色素属于类黄酮化合物,主要有花色苷、黄酮和黄酮醇等.花色苷(anthocyanin)是花色素(anthocyanidin)与糖以糖苷键结合而成的一类化合物,存在于植物的花、果实和叶中,使其呈现由红、紫红到蓝等不同颜色.王晓[12-13]利用高速逆流色谱结合柱色谱分离纯化牡丹花的化学成分,检测出9种化合物:芹菜素-7-O-β-D-芦丁糖苷、木樨草素-7-O-β-D-葡萄糖苷、芹菜素-7-O-β-D-葡萄糖苷、山奈酚-7-O-β-D-葡萄糖苷、山奈酚、芹菜素、木樨草素、苯甲酸、没食子酸.樊金玲等[14-15]利用高效液相色谱与二极管阵列检测器和电喷雾电离质谱联用技术研究了牡丹花中的花色苷类化合物,分离检测了5种花色苷,结合紫外吸收光谱和质谱信息分别鉴定为:矢车菊-3,5-O-二葡萄糖苷、矢车菊-3-O-葡萄糖苷、芍药-3,5-O-二葡萄糖苷、芍药-3-O-葡萄糖苷和天竺葵-3,5-O-二葡萄糖苷.王亮生等[16-18]的研究表明牡丹花中含有6种花色苷(见表1).其基本结构式为3,5,7-三羟基-2-苯基苯并吡喃(见图1).牡丹中所含花色苷种类和含量的多少也与牡丹五彩缤纷的颜色有很大的关系,这有待于进一步深入研究.
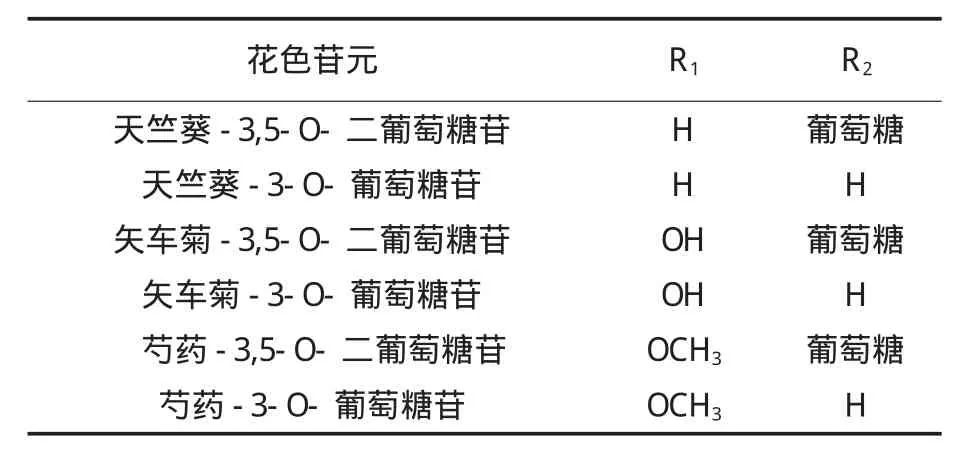
表1 牡丹花色苷元类型
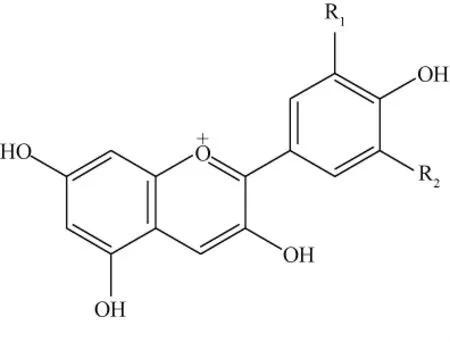
图1 牡丹花中花色苷基本结构式
樊金玲等[14-15]对牡丹花色苷的热稳定性和降解动力学进行了研究.结果表明,牡丹花色苷的热降解符合一级反应动力学模型.在70~90℃条件下,当 pH值为 2.6、3.0、3.6、4.0、4.6时,牡丹花色苷的半衰期分别为 27.0~7.9、32.1~8.5、27.9~8.9、35.9~9.4、27.3~10.7 h.提高温度,花色苷降解反应速率增大;降解反应速率常数与温度的关系符合Arrhenius公式,反应活化能为48.4~69.4 kJ/mol.牡丹花色苷单体的降解速率依次为:矢车菊-3-O-二葡萄糖>芍药-3-O-葡萄糖苷>矢车菊-3,5-O-二葡萄糖苷>芍药-3,5-O-二葡萄糖苷.牡丹花色苷降解生成褐色物质,褐变指数随加热时间的延长、加热温度的升高、pH值的增大而增大.这为牡丹花的工业化应用提供了理论上的依据.
2.3 牡丹花色素的性能及应用
牡丹红色素易溶于水和酒精,难溶于石油醚和乙醚,颜色随pH值变化而变化.在酸性条件下该色素对光、热有很好的稳定性,牡丹花色素在低于60℃情况下比较稳定.在酸性和中性条件下最大吸收波长为526.5 nm,不同溶剂的酸性色素溶液的最大吸收波长有微小的波动,但在花青素特征峰变动范围之内,因此可以确定牡丹花色素为花青素类色素.但其耐氧化性和还原性较差,Zn2+、Mg2+、Fe2+、K+、Cu2+、Ca2+等金属离子对牡丹花红色素的稳定性影响不大,但Sn2+、Fe3+离子可使色素溶液变色,影响稳定性[10].
胡少刚等[19]将黄色牡丹花天然植物染料用于羊毛织物的染色,结果表明,牡丹花黄色染料染色后羊毛织物的耐水洗、耐摩擦、耐汗渍和耐水色牢度均能达到GB 3级以上,唯日晒牢度稍差,仅2~3级.以明矾为媒染剂时牡丹花黄色染料对羊毛织物的最佳染色工艺条件:明矾用量7%(o.w.f),染料用量 4%(o.w.f),染色温度 100℃,染色 45 min(预媒染温度 60℃,媒染 30 min,染浴 pH 4,浴比 1∶20),得到了色泽鲜艳的黄色羊毛织物.肖海芳等[20]以牡丹品种洛阳红为原料,从中提取牡丹花红色素,并将其应用于果冻中.通过试验确定果冻的最佳配方为:0.6 g果冻粉,17 g白砂糖,26 mg牡丹花红色素,0.4 g柠檬酸,0.1mL草莓香精.
2.4 牡丹花色素抗氧化性
细胞中的氧在转变成水之前,会产生许多活性氧(ROS).正常情况下,生物体内活性氧的生成与清除处于动态平衡状态,当各种因素打破这一平衡而致活性氧浓度超过生理限度时,多余的氧自由基就会致使组织损伤,乃至诱发各种疾病和促使机体衰老.而各种抗氧化物质,可以将多余的活性氧自由基清除掉,从而保护细胞、组织免遭氧化伤害.牡丹花色素抗氧化性目前证实的主要表现在抗炎活性方面.在牡丹花色苷中,矢车菊色素-3,5-O-二葡糖苷(Cy3G5G)和天竺葵色素-3,5-O-二葡糖苷(Pg3G5G)具有通过抑制MAPK途径中COX-2的表达阻止炎症的发生.史国安等[6]研究了牡丹花中分离的花色苷和它的糖苷配基矢车菊色素的抗炎作用,结果表明矢车菊色素的抗炎活性强于阿斯匹林.
3 牡丹花对·OH引起的DNA氧化损伤的保护作用
4 牡丹花其他方面的研究
在牡丹花红色素理化性质研究的基础上,朱文学等[22]对品种为‘洛阳红’的牡丹花在干燥过程和干花自然存放过程色变的机理作了探讨.研究发现,牡丹花干燥过程中细胞内水分去除引起的pH值变化和细胞内酶的作用是导致牡丹花干燥过程花瓣变色的2个决定性因素.在牡丹干花自然存放过程中引起花材色变的主要因素是紫外线和氧气.张圣旺等[23]研究了牡丹花衰老过程中的生理、生化变化,结果表明,牡丹花从开放到凋谢期间,花瓣和叶片的可溶性蛋白质含量前期增加,后期下降,细胞质膜透性、丙二醛(MDA)、超氧阴离子()产生量随花瓣的衰老逐渐增加,超氧物歧化酶(SOD)活性逐渐降低,花瓣的变幅大于叶片.这与形态观察到的花瓣的衰老比叶片明显的现象一致.相关分析表明:花瓣可溶性蛋白质含量、质膜透性、MDA含量、SOD酶活性和超氧阴离子自由基之间呈显著相关关系;而叶片则不然,衰老末期可溶性蛋白质含量与游离氨基酸总量之间没有相关性,这与养分耗尽有关.因此认为牡丹花衰老是多因素综合调控而导致细胞编程性死亡的结果.
5 存在的问题及研究方向
牡丹中含有多种有用成分,其中黄酮类、多酚类化合物是牡丹花主要的活性成分,而花色苷有较强的抗氧化活性,具备抗肿瘤活性,它可以通过抑制肿瘤细胞的增殖、转移和诱导癌细胞的凋亡实现抗癌作用.因此,对牡丹花色素抗氧化性的医学应用价值值得期待,前景广阔.此外,牡丹花在营养保健、防治心血管疾病、抗癌、抗动脉粥样硬化、延缓衰老等方面具有较大的开发利用价值.但牡丹花色素中大部分色素对光、热、氧、金属等敏感,稳定性稍弱;多数牡丹花色素染着力较差,染着不易均匀,应用时专用性较强,范围较窄.
今后的研究重点,一是深入开展药理学研究,确定活性药用部分的成分与结构,建立品质评价和特征活性先导化合物寻找技术路线,组配科学合理的复合制剂,探讨疗效、药理和成分3者的量效关系,开辟民间药物研究应用的新途径;二是牡丹花色素的研究主要集中在合成工艺、生产技术和可替代的色素资源,加强牡丹花色素稳定性和使用过程中色素稳定化技术的研究.
[1]白喜婷,朱文学,罗磊,等.牡丹籽提取物的抑菌特性研究[J].中国酿造,2009(3):59-62.
[2]刘建华,董福英,谷颜杰,等.菏泽牡丹花挥发油化学成分分析[J].山东化工,1999(3)35-37.
[3]周海梅,董苗菊,李朴,等.固相微萃取-气相色谱-质谱分析牡丹花的挥发性成分[J].化学分析计量,2008(3):21-23.
[4]王荣花,刘雅丽.牡丹和芍药花瓣中高级脂肪酸组分及含量的测定[J].中国农学通报,2004,20(6):212-215.
[5]刘建华,董福英,王晓,等.牡丹花营养成分分析及其评价[J].山东科学,1999,12(4):60-62.
[6]史国安,郭香凤,包满珠.不同类型牡丹花的营养成分及体外抗氧化活性分析[J].农业机械学报,2006,37(8):111-114.
[7]张修景.火焰原子吸收光谱法测定牡丹花中6种金属元素[J].理化检验(化学分册),2008,44(3):243-244.
[8]吴龙奇,朱文学,易军鹏,等.牡丹花红色素类型判定及提取工艺试验[J].农业机械学报,2005,36(10):77-80.
[9]朱文学,王忠东,罗磊,等.牡丹花色素提取方法:中国,200610048469.8[P],2007-01-24.
[10]朱文学,吴龙奇,易军鹏,等.牡丹花红色素理化性质研究[J].农业工程学报,2006(6):224-226.
[11]刘耀玺,李志西.牡丹花色素提取与性质研究[J].林业实用技术,2006(5):42-44.
[12]王晓.超临界CO2/超声波强化萃取-高速逆流色谱纯化技术的集成及其在生物活性成分研究中的应用[D].泰安:山东农业大学,2004.
[13]Wang X,Cheng C,Sun Q,et al.Isolation and identification of four flavonoid constituents from the flowers of paeonia suffruticosa by high-speed counter-current chromatography[J].Journal of Chormaotgrpohy A,2005,1075:127-131.
[14]樊金玲,朱文学,沈军卫,等.高效液相色谱-电喷雾质谱法分析牡丹花中花色苷类化合物[J].食品科学,2007,28(8):367-371.
[15]樊金玲,朱文学,巩卫东,等.牡丹花色苷的热稳定性和降解动力学[J].应用化学,2010,27(2):231-236.
[16]Wang L S,Hashimoto F,Shiraishi A,et al.Chemical taxonomy of the Xibei tree peony from China by floral pigmentation[J].J Plant Res,2004,117(1):47-55.
[17]Wang L S,Hashimoto F,Shiraishi A,et al.Phenetics in tree Peony species from China by flower pigment cluster analysis[J].JPlant Res,2001,114:213-221.
[18]Wang L S,Shiraishi A,Hashimoto F,et al.Analysis of petal anthocyanins to investigate flower coloration of Zhongyuan (Chinese)and Daikon Island(Japanese) tree peony cultivars[J].JPlant Res,2001,114:33-43.
[19]胡少刚,周奥佳,阎克路.牡丹花天然植物染料对羊毛织物染色性能的研究[J].染料与染色,2009,46(1):26-30.
[20]肖海芳,孙雪,朱文学,等.牡丹花红色素的提取及其在果冻中的应用[J].食品研究与开发,2009,30(10):174-176.
[21]郭香凤,史国安.牡丹花水提液对氧自由基的清除作用[J].植物生理学通讯,2004,40(1):37-38.
[22]朱文学,钟莉娟,段续,等.牡丹花干燥过程中色变机理分析[J].干燥技术与设备,2007,5(3):128-133.
[23]张圣旺,郑荣生,孟丽,等.牡丹花衰老过程中的生理生化变化[J].山东农业大学学报:自然科学版,2002,33(2):166-169.
RESEARCH PROGRESSON COMPOSITION AND APPLICATION OF PEONY
GAO Ya-hui1,ZHANG Shao-wen1,ZHANG Shu-xia2,WAN Shan1
(1.Department of Environmental Engineering and Chemistry,Luoyang Institute of Science and Technology,Luoyang 471023,China;2.Luoyang Entry-Exit Inspection and Quarantine Bureau,Luoyang 471003,China;3.School of Food Science and Technology,Henan University of Technology,Zhengzhou 450052,China)
The paper comprehensively analyzed various chemical components and the extraction,the property and the application of anthocyanidin of peony,and described the nutrition and healthy action,the antioxidant activity,and the protection effect for DNA oxidative damage.Finally,the paper pointed out the problems existing in the study and application,and proposed the future research direction.
peony; composition; anthocyanins; antioxidant activity
TS201.2
A
CNKI:41-1378/N.20111220.1501.019
1673-2383(2011)06-0093-04
http://www.cnki.net/kcms/detail/41.1378.N.20111220.1501.019.html
网络出版时间:2011-12-20 03:01:44PM
2011-07-24
国家自然基金项目(20976037);国家教育部科学技术重点资助项目(205094);河南省杰出人才创新基金项目(05210005000)
高亚辉(1978-),女,河南平顶山人,讲师,研究方向为化工与食品资源的开发与利用.
*
