锂离子电池正极材料LiNi0.5 Mn0.5O2制备及光谱研究
2010-12-26赵立竹孟召宝薛明明邵长路
赵立竹,孟召宝,薛明明,邵长路
(东北师范大学物理学院,吉林长春130024)
锂离子电池正极材料LiNi0.5Mn0.5O2制备及光谱研究
赵立竹,孟召宝,薛明明,邵长路
(东北师范大学物理学院,吉林长春130024)
用共沉淀法合成了LiNi0.5M n0.5O2材料.为了探索共沉淀法合成LiNi0.5M n0.5O2的最佳工艺,详细研究了研磨时间、p H值、预处理温度、煅烧温度、煅烧时间和冷却方式等对材料结构的影响.以氢氧化锂为锂源,Ni(NO3)2·6H2O和M n(Ac)2·4H2O为镍源和锰源,锂与镍、锰物质的量比为1.1∶0.5∶0.5,经强氧化剂处理,900℃下煅烧12 h后经淬冷制备了LiNi0.5M n0.5O2样品.采用XRD,Raman和XPS对该样品进行了分析,结果表明:材料为标准的α-NaFeO2层状结构,属于六方晶系;镍以正二价的形式存在,锰主要以正四价存在,非常接近理论计算的理想结构.
锂离子电池;LiNi0.5M n0.5O2;正极材料
0 引言
锂离子电池是性能卓越的新一代绿色高能电池,已成为高新技术发展的重点之一.它以其高电压、高容量、低消耗、无记忆效应、无公害以及体积小、内阻小、自放电少、循环次数多等显著特点在众多的电池中脱颖而出.目前商业化正极材料多为LiCoO2和Li-Co-Ni-O系列的电池,但钴的资源匮乏、并且有毒性,危害人体健康和对环境不友好,价格昂贵等缺点,限制了锂离子电池的应用发展.人们迫切需要一种储量丰富,对环境友好,价格低廉的材料来代替钴系列锂电池,现在最大希望的就是锰、镍系列的电池,单一体系的LiNiO2和LiM nO2经大量研究后证实无法替代LiCoO2,即使经过多年研究也得到了一些进展,到目前为止能够代替LiCoO2的单一体仍无法实现.所以人们就把目光转移到对单一材料的掺杂改性,把希望寄托在复合材料上来[1],并且对复合材料的研究已经成为当今电池材料的一个热点和发展方向.锂离子电池正极材料一旦有所突破,将带来巨大的经济效益.近年来,研究者们对镍掺杂特别关注[2-8],理论计算指出LiNi0.5M n0.5O2中Ni和M n的价态分别为+2和+4,Ni2+的掺入可提高M n的平均价态,使材料的稳定性提高,LiNi0.5M n0.5O2材料有诸多优点,如充放电比容量高、结构更稳定、原材料经济廉价、资源丰富、对环境友好,有发展前景,但电化学性能与制备方法、合成条件直接相关,合成+4价锰的LiNi0.5M n0.5O2材料是关键.本文采用共沉淀法,通过不同煅烧温度、不同煅烧时间等实验条件探索,找到较佳的制备LiNi0.5M n0.5O2材料的条件.
1 实验部分
1.1 试剂与仪器
仪器:Rigaku D/MAX2500PC X射线衍射仪,辐射源CuKα(λ=0.154 1 nm),2θ测试范围为10°~90°;JY HR800微区拉曼测试仪,使用氩离子激光器,波长为488 nm;Perkin Elmer ICP/1000等离子发射光谱仪;ESCALABⅡ型X射线光电子能谱仪.
试剂:Ni(NO3)2·6H2O,M n(CH3COO)2·4H2O和LiOH·H2O等试剂均为分析纯.
1.2 样品的制备
采用共沉淀法将一定量的Ni(NO3)2·6H2O和M n(CH3COO)2·4H2O按化学式计量比1∶1配成混合物,用玛瑙研钵研磨3 h,镍锰混合溶液与氢氧化锂溶液分别逐滴加入到p H值为10~11且不断搅拌的氢氧化锂碱液中,长时间搅拌共沉淀溶液,为了加速氧化,加入了适量 H2O2,将前驱体溶液离心,过滤沉淀物,再用蒸馏水反复清洗滤饼,除去剩余的锂盐.将共沉淀物放置在真空干燥箱中,100℃保持24 h,得到锰镍共沉淀前驱体.将烘干后的共沉淀前驱体与氢氧化锂按n(Li)∶n(M n)∶n(Ni)=1.1∶0.5∶0.5的配比混合,在玛瑙研钵中研磨数小时,以便使其混合均匀.将其放入坩埚中移入高温炉中煅烧,缓慢升温,当温度达到700℃恒温4 h后继续升温,以后每升高100℃后,都要恒温4 h,直到达到设定温度,当温度达到设定温度时,恒温4 h,取出淬冷再煅烧,反复几次,直到达到所需反应时间.
2 结果与讨论
2.1 煅烧温度对材料的影响
用共沉淀法合成LiNi0.5M n0.5O2材料时,煅烧温度对材料的性能有着很大的影响:温度低,材料的结晶性不是很好,晶粒尺寸不均匀;温度高,团聚现象严重,对材料的电化学性能影响比较大,会影响电池的使用寿命.图1分别是在700℃,800℃和900℃下煅烧12 h的XRD谱.从图1中可以看出,合成的材料都是α-NaFeO2型结构,属于R空间群.
如图1所示,随着温度的升高,衍射峰强度也变得越来越强,越来越尖锐,说明结晶性随着温度的升高变得越来越好,文献[4]报道了温度超过900℃时,(003)峰会出现杂相,峰变得平缓,这主要是因为在合成过程中随着温度的升高,锂盐随之挥发,改变了Li元素的比例,晶体的结构就发生了变化,Ni2+很容易进入Li层,最终导致材料层状结构发生变化,但本文实验在900℃时,没有出现上面这种情况.
从衍射峰的角度值再根据布拉格方程算出晶面间距d值,通过d值计算700℃,800℃和900℃条件下合成的材料晶格参数列于表1.一般认为c/a的值大于4.93就可以说明材料的层状结构比较好,而表1中c/a值均大于4.93,并且随温度增加逐渐增大,说明层状结构随煅烧温度增加变得更好,并且表1中的晶格参数值与文献中报道的很接近[6,9].

表1 在不同温度制备的L iNi0.5 Mn0.5 O2样品的晶格参数
表1中最后一项数据是(003)和(104)两个衍射峰强度的比值,I(003)/I(104)的比值越大,说明在3(a)位的过渡金属离子和3(b)位的Li+错位越少,阳离子的无序性越小;比值越小,两个离子错位越多.从表1中可以看出,随着温度的增加,I(003)/I(104)的值越来越大,也就是说阳离子的无序性越来越少,晶格越来越有序,错位也越来越少,材料的六方结构更完美.
称取0.05 g合成的样品用盐酸微溶解,加入蒸馏水稀释,在50 m L容量瓶里定溶,用ICP检测仪检测Ni和M n含量.测得700℃,800℃和900℃3组样品中Ni和M n物质的量比分别为1.000 5∶1,1.005∶1,1.006∶1,十分接近1∶1,说明合成的样品为LiNi0.5M n0.5O2,达到了设计要求.
2.2 煅烧时间对材料的影响
在6,12和20 h条件下,900℃高温煅烧制得的LiNi0.5M n0.5O2样品XRD图(见图2).

图1 不同温度制备的L iNi0.5Mn0.5O2样品的X射线衍射谱

图2 不同时间制备的L iNi0.5Mn0.5O2样品的X射线衍射谱
从图2中可以看出,随着煅烧时间从6 h变为12 h,衍射峰强度在增加,峰也越来越尖锐,尤其是(003)和(104)晶面衍射峰变化最明显.但是随着时间进一步延长到20 h,我们会发现衍射峰强度有所减弱,(003),(101)和(104)晶面衍射峰变化最明显,并且在25°附近底线升高,这很有可能是随着时间的延长,锂盐的过度挥发,减少了Li元素的含量,Ni2+开始逐渐取代Li+的位置,材料中错位开始增加,层状结构变差,结晶质量变差.从图2也可以看出在900℃煅烧12 h的样品结晶性最好.
不同煅烧时间制备的3个LiNi0.5M n0.5O2样品,第一个主峰位于2θ=18.6°,对应(003)晶面,当采用CuKα作为 X射线源时,X射线波长为0.154 nm,对应700℃,800℃和900℃条件下得到的样品LiNi0.5M n0.5O2的半高宽分别为 0.149 94°,0.157 59°和 0.354 72°,一般采用 Scherer常数为 0.89,根据Scherer公式,计算获得晶粒尺寸为84.16,50.51和22.44 nm.我们可以看出,随着温度的增加,晶粒尺寸减小.对于3个样品,煅烧从6到12 h,I(003)/I(104)值逐渐在增加,20 h的样品和12 h的样品相比,I(003)/I(104)值也减小,这也说明了12 h煅烧的样品错位较少,晶格更有序,材料的结构更接近理想六方晶形.
2.3 超声和冷却方式对样品的影响
在制备前驱体时,采用了超声与不超声两种方法进行比较,一般来说,超声与否也会对材料的结构有着一定的影响.从两种方法制得LiNi0.5M n0.5O2材料的XRD图可以看出,经过两种处理方式得到的样品晶体结构差别很明显,主要还是表现在(101),(003)和(104)3个峰的强度上,经过2 h超声的样品的峰要比未超声的峰强度更大,更锐利.这可能是经过超声后制得样品内各元素混合得更均匀、充分,更有利于充分反应.
冷却的方式不同对样品的结构、结晶性也有很大的影响.本文采取自然冷却和淬冷2种方式,其中淬冷,在烧制样品过程中,当达到目标温度时,每过2 h将样品从炉中拿出淬火冷却到室温,再放入炉中,反复烧制,直到达到预定时间.对两种方式处理的样品进行了XRD分析,可以看出两者的不同表现在(003)和(104)两个晶面的衍射峰上,淬冷的峰强度更大,更尖锐,其结晶性更好一些,晶格结构更均匀.淬冷后的(003)与(104)晶面对应峰强度比值I(003)/I(104)要比自然冷却的值大,这也说明了经过淬冷样品的层错位少,晶格更有序.
2.4 X射线光电子能谱(XPS)分析
图3为LiNi0.5M n0.5O2材料的XPS谱.将XPS测得各元素的结合能与参考文献中给出的数据进行比较,可以得到各元素的价态.图3a和c中M n2p3/2的结合能为642.2 eV,M n3p的结合能为49.8 eV,这与M n4+结合能吻合[9-10],表明在材料中M n以正四价的形式存在.图3b中Ni2p3/2结合能为854.4 eV,这与文献[6]给出的Ni2+基本吻合,说明材料中Ni元素是以正二价的形式存在的.图3c中54.7 eV为Li1s的结合能[7].图3d中531.2 eV是O1s的结合能[10-11].从上述分析中可以看到,Ni元素主要是以正二价形式存在,M n元素主要是以正四价存在,没有表现出正三价的M n.这也正是我们所希望的那样,因为正三价的M n有高自旋态,对结构的稳定性很不利,正四价M n的材料的结构更稳定.

图3 L iNi0.5Mn0.5O2样品的X射线光电子能谱
2.5 拉曼光谱
图4为用900℃煅烧12 h的制备的样品的拉曼光谱,2个拉曼散射峰发生在594和481 cm-1处,这与R结构的商群计算结果一致,它们分别来自A1g和Eg振动模式的贡献.A1g振动模式主要与M n/Ni—O伸缩振动相关,Eg振动模式由O—M n/Ni—O弯曲振动引起,A1g振动表现为比Eg振动更强.由于尖晶石结构也有与NaFeO2结构相同的衍射谱,用Ni部分取代o-LiM nO2中的M n可获得结构为NaFeO2的晶体,拉曼光谱进一步验证了X射线衍射结果的正确性.
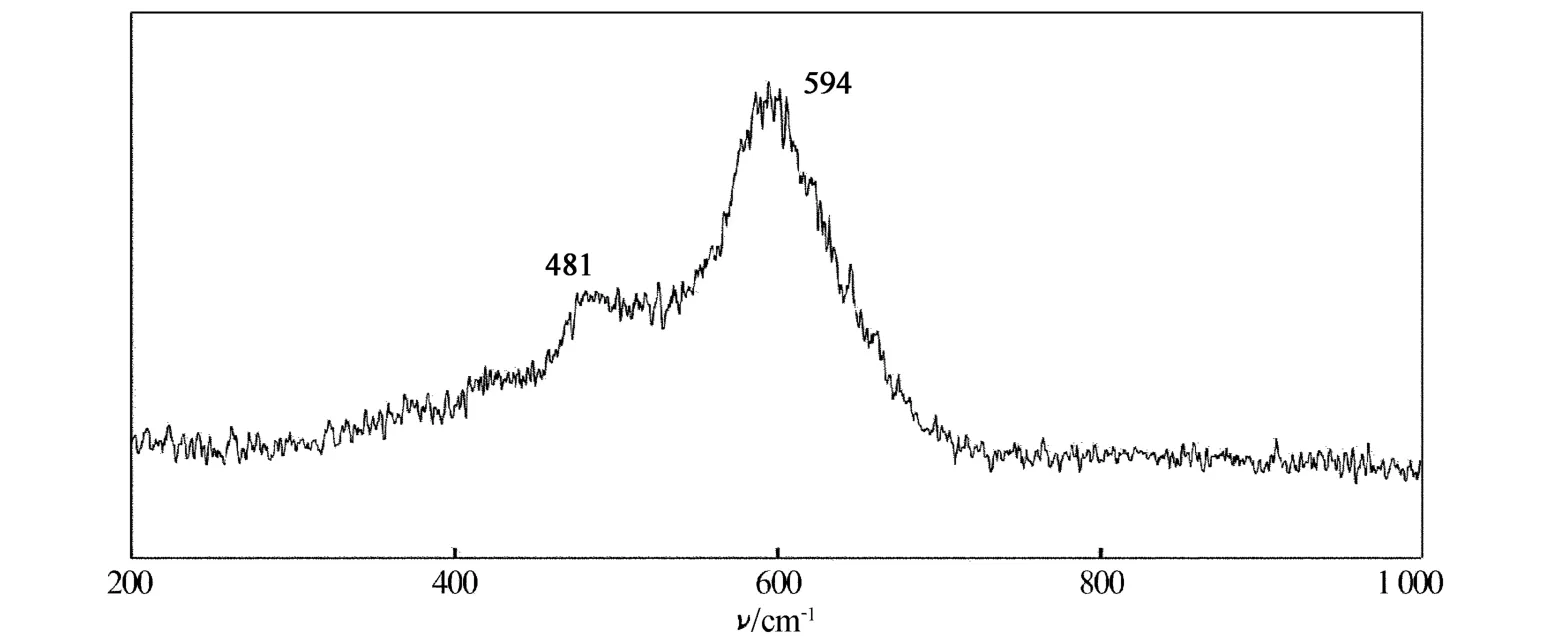
图4 L iNi0.5 Mn0.5O2样品的拉曼光谱
[1] 张凌,王荣顺,王淑英.锂离子电池LiFePO4/聚并苯复合正极材料的合成与改性研究[J].东北师大学报:自然科学版,2008,40(1):81-84.
[2] WH ITACRE J F,ZAGH IB K,WEST W C,et al.Dual activematerial compositecathode structures for Li-ion batteries[J].J Power Sources,2008,177:528-536.
[3] OHZUKU T,MA KIMURA Y.Lithium insertion material of LiNi1/2M n1/2O2for advanced lithium-ion batteries[J].J Power Sources,2003,119/120/121:156-160.
[4] KANG S H,AM INE K.Comparative study of Li(Ni0.5-xMn0.5-xM2x′)O2(M′=Mg,Al,Co,Ni,Ti;x=0,0.025)cathode materials for rechargeable lithium batteries[J].J Power Sources,2003,119/120/121:150-155.
[5] LU Z,MACNEIL D D,DAHN J R.Layered cathodematerials Li[NixLi(1/3-2x/3)Mn(2/3-x/3)]O2for lithium-ion batteries[J].Electrochem Solid-State Lett,2001,4:A 191-A 195.
[6] KANG S H,KIM J,STOLL M E,et al.Layered Li(Ni0.5-xMn0.5-xM′2x)O2(M′=Co,Al,Ti;x=0,0.025)cathode materials for Li ion rechargeable batteries[J].J.Power Sources,2002,112:41-48.
[7] KIM J H,YOON C S,SUN Y K.Structural characterization of Li[Li0.1Ni0.35Mn0.55]O2cathodematerial for lithium secondary batteries[J].J Electrochem Soc,2003,150:A 538-542.
[8] PASQURIER A D,BIRY A,COURJAL P.Mechanism for limited storage performance of Li1.05Mn1.95O4electrodes[J].J Electrochem Soc,1999,146:428-436.
[9] SHAJU K M,SUBBA Rao G V,CHOWDARIB V R.X-ray photoelectron spectroscopy and electrochemical behaviour of 4 V cathode,Li(Ni1/2M n1/2)O2[J].Electrochimica Acta,2003,48(11):1505-1514.
[10] SPAHR M E,NOVÁK P,SEHNYDER B,et al.Characterization of layered lithium nickelmanganese oxides synthesized by a novel oxidative cop recipitation method and their electrochemical performance as lithium Insertion electrode materials[J].J Electrochemical Soc,1998,145(4):1113-1121.
[11] SHAJU K M,SUBBA RAO G V,Chow dari B V R.Lithiated O2phase,Li(2/3)+x(Co0.15M n0.85)O2as cathode for Li-ion batteries[J].J Solid State Ionics,2002,152/153:69-81.
Study of preparation and spectroscopic on the lithium-ion battery cathode material L iNi0.5Mn0.5O2
ZHAO Li-zhu,M ENG Zhao-bao,XUEM ing-ming,SHAO Chang-lu
(College of Physics,Northeast Normal University,Changchun 130024,China)
The LiNi0.5Mn0.5O2materials were synthesized by co-precipitation method.In order to exp lore the best path of synthesis the LiNi0.5Mn0.5O2with co-precipitation,we studied detailedly the grinding time,p H,pretreatment,calcination temperature,calcination time and the coolingmethods.Experimental results show that lithium hydroxide isa lithium source,Ni(NO3)2·6H2O and M n(Ac)2·4H2O is the source for the nickel and manganese sources,so lithium and nickel,manganese molar ratio is 1.1∶0.5∶0.5.After strong oxidant treatment,900℃calcined 12 h,and quenching,the LiNi0.5Mn0.5O2materials were p repared,the samples structure were the standardα-NaFeO2layered structure and belongs to hexagonal system by XRD and Raman spectroscopy testing.XPS analysis showed that the nickel was divalent,the manganese is tetravalent.This is very close to the theoretical calculation of the ideal structure.
lithium-ion battery;LiNi0.5M n0.5O2;cathode material
O646.21
150·3050
A
1000-1832(2010)03-00103-05
2010-04-09
国家自然科学基金资助项目(10874023);吉林省科技发展计划项目(20090533).
赵立竹(1962—),女,博士,副教授,主要从事功能材料物理与化学研究.
(责任编辑石绍庆)
