乙酸存在下钴铝类水滑石催化氧化苯甲醛合成苯甲酸
2010-09-13谢鲜梅
吴 旭,谢鲜梅
(太原理工大学化学化工学院,太原030024)
水滑石是一类具有特殊结构的层状无机材料。水滑石类材料主要包括水滑石(Hydrotalcite,简称HT)及水滑石类化合物(Hydrotalcite-like compounds,简称H TLcs)。其结构既具有层板上阳离子的同晶取代性,又具有层间阴离子的可交换性[1]。水滑石因其独特的结构特性、组成及孔结构的可调变性以及优良的催化性能,在吸附、催化领域中占有重要位置,在催化工业、医药等方面具有广阔的应用前景。
苯甲酸作为一种最常见的有机酸,在医药、食品、化工等方面应用十分广泛,苯甲酸及其钠盐可用作乳胶、牙膏、果酱或其他食品的抑菌剂,也可作染色和印色的媒染剂。而苯甲醛氧化合成苯甲酸的研究由来已久。已有研究者[2-6]把HTLcs引入到苯甲醛催化合成苯甲酸中,但大都在其中加入了强氧化剂(如H2 O2)。此类强氧化剂的引入使反应相对复杂多变,从而使目标产物的反应转化率和选择性受到影响。本文将CoAl-H TLcs催化剂应用于乙酸作为溶剂下苯甲醛氧化合成苯甲酸的反应中,在以空气为氧化剂的前提下很好地完成了此催化反应,详细研究了诸多反应条件对催化活性及选择性的影响,并就CoAl-HTLcs催化剂对此反应的高效催化进行了理论解释。
1 实验部分
1.1 催化剂CoAl类水滑石化合物的制备和表征
将两种硝酸盐溶液Co(NO3)2◦6H 2 O(1 mol/L),Al(NO3)3◦9H 2O(0.5 mol/L)按比例配成混盐溶液。在不停的剧烈搅拌下,以1.0 mL/min的速度滴加1 mol/L NaOH溶液至所需pH。滴加完后继续搅拌0.5 h,再将所得浆液置于不锈钢反应釜中,在110℃下水热处理6 h。然后将晶化后的浆液洗涤至滤液pH值为7,抽滤干燥后研磨以备用。
采用日本产Rigaku D/max-2500型X射线固体粉末衍射仪表征其晶体结构。样品经研磨、压片后放入样品池,使用Cu靶,Kα射线(波长λ=0.154 18 nm),石墨单色器,靶电压40 kV,靶电流100 mA,扫描速率8°/min,扫描范围5°~80°,闪烁计数器记录强度。
FT-IR8400,日本岛津生产,测定波数范围为400~4 000 cm-1。
1.2 催化反应分析方法及仪器分析条件
准确量取一定量的苯甲醛和乙酸于三口烧瓶中,启动磁力搅拌控温装置。等达到反应温度后,将所制得的CoAl-HTLcs(预先在100℃下用N2气吹扫2 h)作为催化剂加入到三口烧瓶中,抽取此时的反应液进行气相色谱分析,作为反应为0 min时的数据。之后启动电磁搅拌和回流装置并以一定的转速搅拌,使反应充分进行,定时取样,用SP-2100气相色谱仪进行分析。分析条件:采用OV-101毛细管柱,柱温 210℃,进样器 250℃,FID检测器260℃。
2 结果与讨论
2.1 催化剂的表征
将上述共沉淀法制得的n(Co)/n(Al)=2的样品粉末作XRD测试,进行物相鉴定,结果见图1。
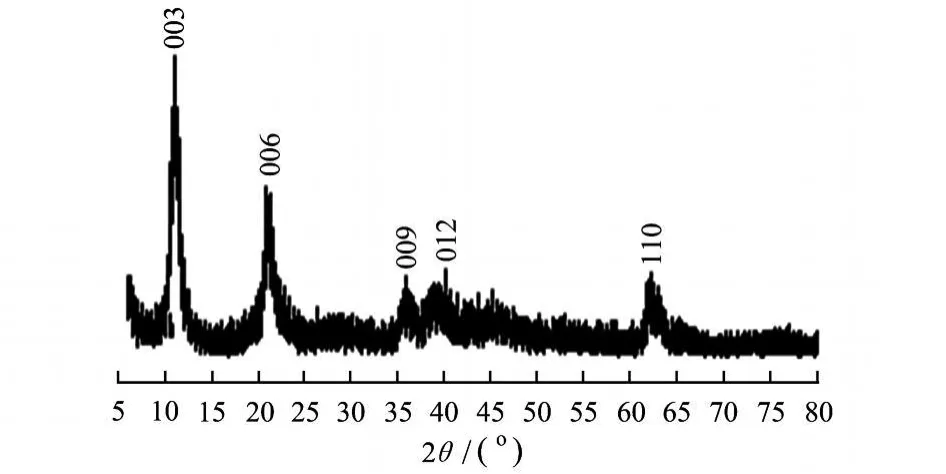
图1 CoAl-HTLcs的XRD谱图
由图1可知,合成的样品具有典型的水滑石结构,其特征衍射峰003、006峰强度高而且尖锐,说明合成的类水滑石晶相较好。另据a=2d 110和c=3d003可计算出相应的晶胞参数,见表1。

表1 钴铝类水滑石的晶胞参数 nm
将所制得的CoAl-HTLcs进行FT-IR分析,结果见表2。

表2 CoAl-HTLcs的FT-IR数据 cm-1
由表2可以得知,CoAl-HTLcs在3 439 cm-1处的吸收峰,应该是由样品表面和层间空隙所吸附的一定数量的H 2O分子的伸缩振动引起的。与自由状态-OH(约3 600 cm-1)相比,该峰向低波数方向发生了一定的偏移,说明层间H2O分子与层间CO32-离子及层板羟基存在一定的氢键作用,而3 006 cm-1附近的弱吸收肩峰也说明了这一点。在1 640 cm-1附近应是H2O中羟基的弯曲振动峰,而1 362 cm-1附近有CO32-的不对称伸缩振动,与CaCO3中CO32-(1 429 cm-1)相比,也向低波数方向发生了很大偏移,说明层间插入的CO32-离子与层间水分子及层板羟基存在很强的氢键作用;同时也说明层间CO32-排列整齐,对称性高,是晶形比较完美的水滑石。1 096 cm-1处出现一个比较尖锐的肩吸收峰,它可能是由于CO32-的对称性降低,使伸缩振动峰活化而引起的。而低于1 000 cm-1出现的第6、7吸收峰应属于指纹区。
2.2 催化剂和乙酸用量对反应的影响
为了考察CoAl-HTLcs催化剂和乙酸有无对此反应的影响,在反应温度为65℃、反应时间为45 min、实验搅拌速度为800 r/min、苯甲醛为5 mL时设计实验,见表3。
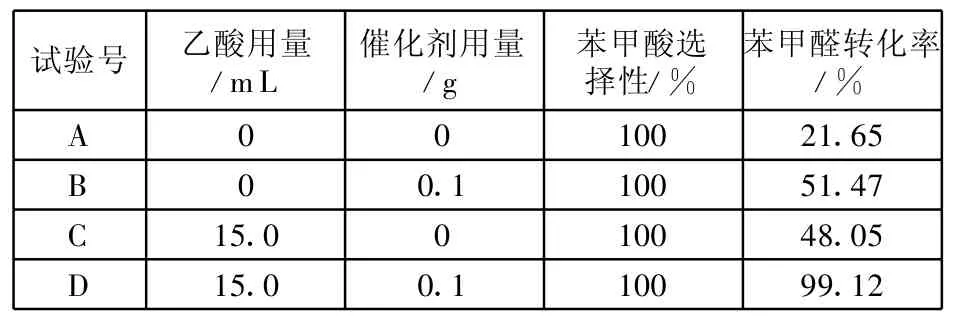
表3 催化剂和乙酸的存在与否对反应转化率的影响
由表3可以看出,CoAl-HTLcs催化剂及乙酸的存在与否对此氧化反应的选择性及转化率有很重要的影响。
而催化剂及乙酸具体用量对反应的影响如图2、图3所示。
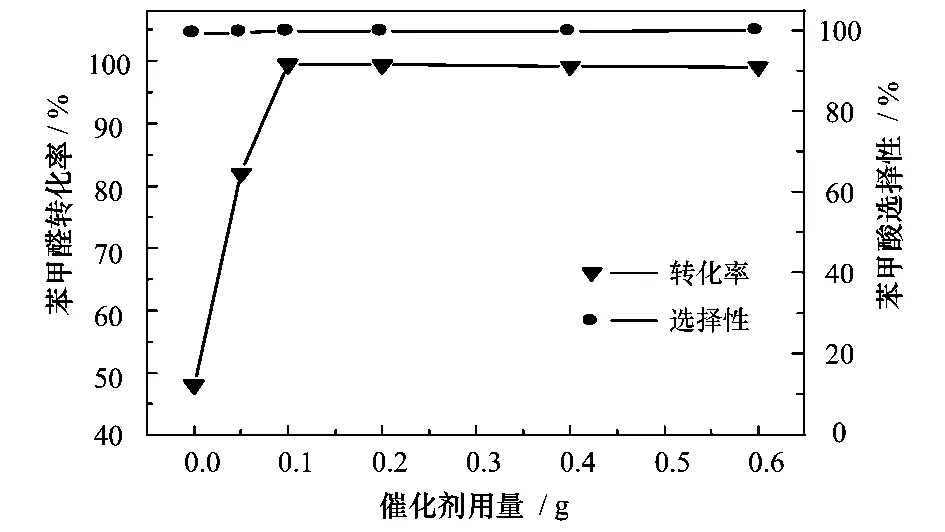
图2 催化剂用量对反应转化率的影响
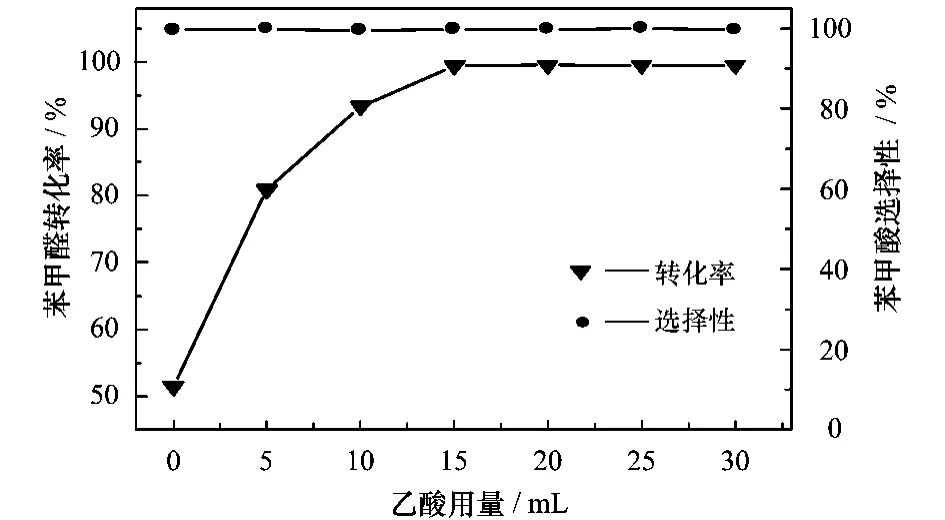
图3 乙酸用量对反应转化率的影响
由图2可看出,催化剂的加入很大程度上促进了反应的进行,使苯甲醛的转化率由48%升高至近100%,说明此催化剂对反应的催化作用很强,活性比较高。但在本实验条件下,催化剂用量超过0.1 g时,催化剂用量的大小对于反应的影响已不是很大,这是因为此时催化剂促进苯甲醛转化为苯甲酸已经达到了最大程度,反应已比较彻底。因此适宜的催化剂用量应为0.1 g。而由图3可知,在一定的反应条件下,随乙酸用量的增加,苯甲醛转化率随之提高。乙酸添加量为15 mL时反应45 min左右苯甲醛转化率就达近100%,之后几乎不变。说明此时反应已较为彻底。因此适宜的乙酸添加量为15 mL。
2.3 n(Co)/n(Al)对反应的影响
在温度65℃、时间45 min、实验搅拌速度为800 r/min、苯甲醛5 mL、乙酸 15 mL时,应用0.1 g不同n(Co)/n(Al)所得的催化剂进行反应,结果如表4所示。

表4 n(Co)/n(Al)对反应转化率的影响 %
由表4可以看出,n(Co)/n(Al)从0到∞变化时,苯甲醛转化率呈现抛物线变化规律。当n(Co)/n(Al)=2时苯甲醛转化率达最大,为99.46%。而Al(OH)3和Co(OH)2直接为催化剂时,反应转化率则较低。说明水滑石结构中的Co可能是反应的真正催化中心,之所以呈现出上述变化规律,可能与Co2+、Al3+之间存在很好的协同作用有关。
2.4 反应在敞开、封闭体系下的研究
在温度65℃、时间45 min、实验搅拌速度为800 r/min、苯甲醛5 mL、乙酸15 mL、催化剂为CoAl-HTLcs(0.1 g)时,分别考察敞开、封闭体系下反应的转化率,见图4。
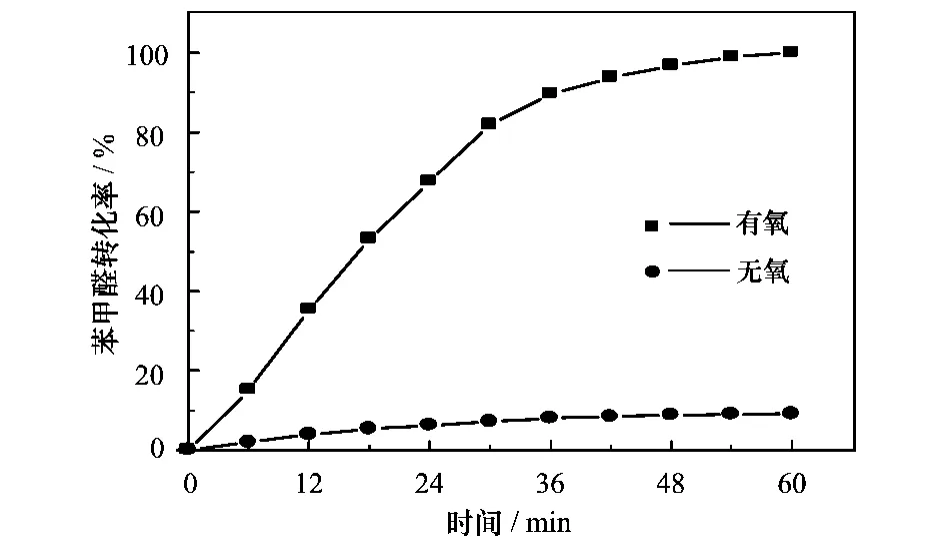
图4 敞开、封闭体系下反应转化率
由图4可知,在敞开体系下反应的转化率要远远高于封闭体系下的转化率,45 min后敞开体系下的转化率近100%,而封闭体系下的转化率只有9%左右,这说明敞开体系下苯甲醛到苯甲酸的高转化率主要应是空气中氧气的有效参与。而封闭体系下由于隔绝了空气,致使转化率极低,理论上它的转化率应该为0;之所以还有9%左右的转化率,我们认为是因为在加料过程中不可避免地吸收了少量氧气的缘故。
2.5 搅拌速度对反应的影响
本反应是以空气中的O2为氧化剂,因此该反应为气-液反应。所以它的总速率既决定于反应的本体动力学,也决定于氧气自气相向气-液相界面和通过相界面向液相本体的传质速率。反应中氧的供给过程由三个连续的步骤组成,即由气相向气-液相界面的传递,通过气-液相界面的传递和从相界面向液相本体的传递。通常,由于在相界面和液相本体内所发生的化学反应速率较高,因而自气相向气-液相界面的传递过程往往就是整个反应的控制步骤。要强化氧传质性能,通常需要提高搅拌速度。在敞开体系下,在反应温度为65℃,反应时间为45 min,V(苯甲醛)∶V(乙酸)=5∶15,CoAl-HTLcs催化剂用量为0.1 g时,考察不同搅拌速度下苯甲醛的转化率,得图5。

图5 搅拌速度对反应转化率的影响
由图5可见,在实验条件下,随着搅拌转速的增大,苯甲醛的转化率相应增大,苯甲酸的选择性未有太大改变。这说明在相同的条件下,提高搅拌速度,增大了体积传质系数,使单位反应器体积的气-液相界面增加,并一定程度上克服了催化剂分散性差的缺点。另外,本文中所选的CoAl-H TLcs催化剂由于其特殊的微孔结构,可能在实验中也一定程度上很好地充当了气体分布器的作用。几方面的共同作用使得在搅拌速度为800 r/min时,催化效果相当显著。
2.6 温度对反应的影响
当反应时间为45 min,实验搅拌转速为800 r/min,苯甲醛 5 mL,乙酸 15 mL,催化剂 CoAl-HTLcs为0.1 g时改变反应温度,所得结果如图6所示。
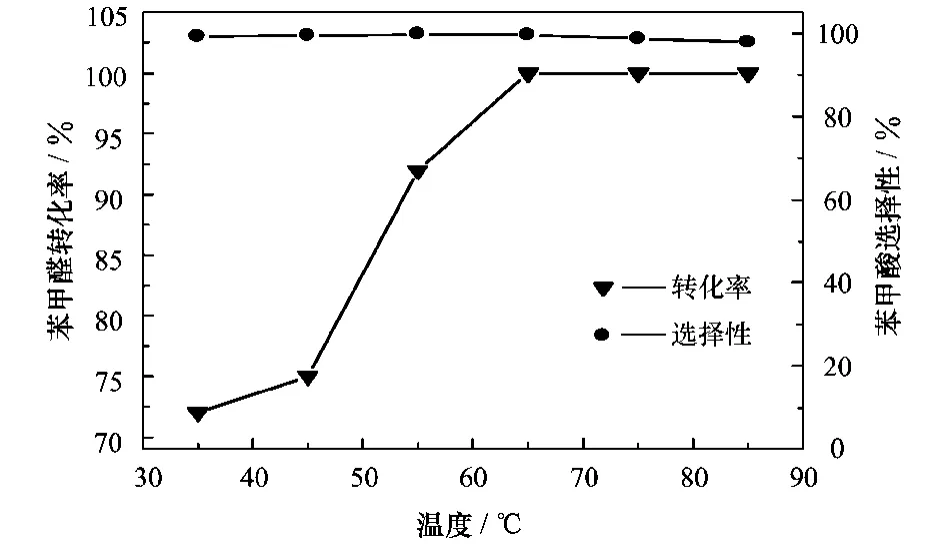
图6 温度对反应转化率的影响
我们知道,正常的氧化反应需要一个合适的吸氧速度,温度高些一定意义上有利于苯甲醛液相氧化反应的进行,但同时也会降低氧气在反应液中的溶解度,而在高温缺氧条件下一些中间产物也容易发生副反应,使反应的选择性有所降低。另外,此氧化反应又是一个强烈的放热过程,温度高也会抑制正反应的进行。从图6分析知,适宜的反应温度为65℃。
2.7 反应时间的影响
当温度为65℃、实验搅拌速度为800 r/min、苯甲醛5 mL、乙酸 15 mL、催化剂CoAl-HTLcs为0.1 g时作苯甲醛转化率随反应时间的变化图,所得结果如图7所示。
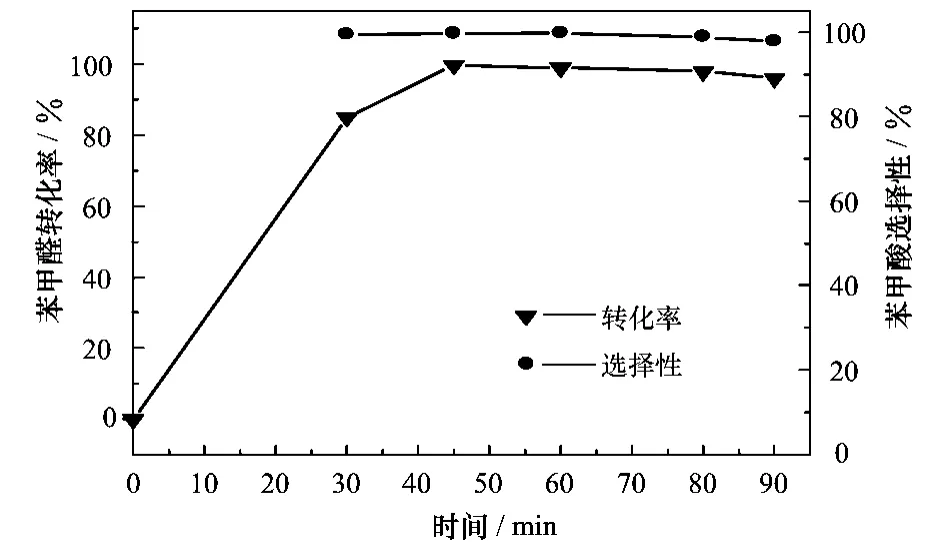
图7 反应时间对转化率的影响
由图7可看出,从反应开始至30 min,反应进行得很迅速,苯甲醛的转化率已经高达85%左右,在30~45 min内相对缓慢地提高至近100%。这说明此催化剂催化活性很高,在较短的时间内即可充分与反应物接触,使大量的苯甲醛转化为苯甲酸,而反应的选择性在反应时间内均未有太大的改变。
3 结论
实验结果表明,因CoAl-H TLcs催化剂能较好地活化分子氧,同时引入的质子型溶剂乙酸可以借助氢键与氧气缔合,有利于氧气在反应液中的溶解与扩散,且还可活化催化剂中的活性中心,使CoAl-HTLcs在有乙酸存在的条件下可以很好地催化氧化苯甲醛。当反应温度为65℃、时间为45 min、实验搅拌速度为 800 r/min、苯甲醛 5 mL、乙酸15 mL、催化剂(n(Co)/n(Al)=2)CoAl-HTLcs 0.1 g时,苯甲醛的转化率便可接近100%,苯甲酸的选择性为100%。
[1] Cavani F,Trifiro F,Vaccari A.Hydrotalcite-ty peanionic clay:preparation properties and application[J].Catal Today,1991,11:173-181.
[2] 谢鲜梅,杜琰,任秀荣,等.MgCoAl类水滑石对苯甲醛氧化的催化活性研究[J].煤炭转化,2005,28(Sup):92-94.
[3] 贺庆林,胡长文,张云峰,等.Studies on the oxidative activity and thermal stability of a new ty pe pillared layered cataly st Zn2Al-XW11 Z[J].催化学报,1996,17:559-562.
[4] Choudhary V R,Dumbre D K,Narkhede V S,et al.Solvent-free selective oxidation of benzyl alcohol and benzaldehyde by tert-butyl hyd roperoxide using MnO4--ex changed Mg-Al-hydrotalcite catalysts[J].Catal Lett,2003,86(4):229-233.
[5] 李拓,李琳.CoAl类水滑石催化苯甲醛氧化制备苯甲酸的研究[J].四川有色金属,2008(4):33-37.
[6] 农兰平,甘琳,黄艳仙,等.含铜三元类水滑石的合成及其催化苯甲醛H2O2氧化的应用研究[J].化学与生物工程,2006,23(9):18-20.
