顶空毛细管气相色谱法测定痰热清胶囊中有机溶剂残留量
2010-08-24张善杰岳随有
张善杰,岳随有
(河南省新谊药业股份有限公司,河南新乡 453731)
顶空毛细管气相色谱法测定痰热清胶囊中有机溶剂残留量
张善杰,岳随有
(河南省新谊药业股份有限公司,河南新乡 453731)
目的:建立痰热清胶囊有机溶剂残留量检测方法。方法:采用顶空毛细管气相色谱法,利用(6%)氰丙基苯基-(94%)二甲基聚硅氧烷毛细管气相色谱柱和FID检测器,内标法测定痰热清胶囊中有机溶剂残留量。结果:待测化合物线性相关系数均大于0.999 0,重复性试验RSD均小于2.0%,回收率试验结果符合规定。结论:此方法快速、简便,结果准确可靠,重复性好。
痰热清胶囊;顶空进样法;毛细管气相色谱;有机溶剂残留量
痰热清胶囊为新谊医药集团痰热清系列产品,是由多味药材提取物按制剂工艺制得的中药产品,由于各提取物及制剂生产过程中使用了乙醇、乙酸乙酯、正丁醇3种有机溶剂,为确保产品的安全可靠,笔者参照痰热清注射液质量标准[1]及其他文献资料[2-5]中相关内容对痰热清胶囊有机溶剂残留方法进行了研究,建立了顶空毛细管法测定痰热清胶囊有机溶剂残留量测定方法,现报道如下:
1 仪器与试剂
气相色谱仪(北京北分瑞利SP-3420A);顶空进样器(北京中兴汇利 DK-3001A);(6%)氰丙基苯基-(94%)二甲基聚硅氧烷毛细管柱;分析纯乙醇、乙酸乙酯、正丁醇、氢氧化钠;痰热清胶囊(河南省新谊药业股份有限公司)。
2 方法
2.1 检查限度的确定
依据《化学药物残留溶剂研究的技术指导原则》[6],乙醇、乙酸乙酯、正丁醇属于第3类溶剂,有机溶剂限度为0.5%。
2.2 色谱条件
参照残留溶剂测定法(中国药典2005年版二部附录ⅧP第一法)[7],分别对色谱柱温度、FID检测器温度、顶空平衡时间及温度进行了研究,经反复优选,确定按柱温80℃、进样口温度200℃、检测器温度250℃、顶空瓶平衡温度80℃及相应平衡时间30 min进行测定,乙醇、乙酸乙酯、正丁醇响应值及出峰情况最好。
2.3 内标及对照品溶液制备
取正丙醇适量,以水溶解制成每1毫升中含10 mg的溶液,作为内标溶液;另取乙醇、乙酸乙酯、正丁醇适量,用水溶解并定量稀释制成每1毫升中含量均为5 mg的溶液,作为对照品储备液,精密量取1 ml置于20 ml量瓶中,精密加内标溶液1 ml,加水稀释至刻度制成对照品溶液。
2.4 供试品溶液的制备
依据痰热清胶囊各提取物生产工艺,经反复试验,供试品须先用0.1 mol/L氢氧化钠溶液溶解后,再进行有机溶剂残留检查。具体方法为:取本品1.0 g,精密称定,置于20 ml量瓶中,精密加入内标溶液1 ml,以0.1 mol/L氢氧化钠溶液溶解并稀释至刻度。
2.5 专属性
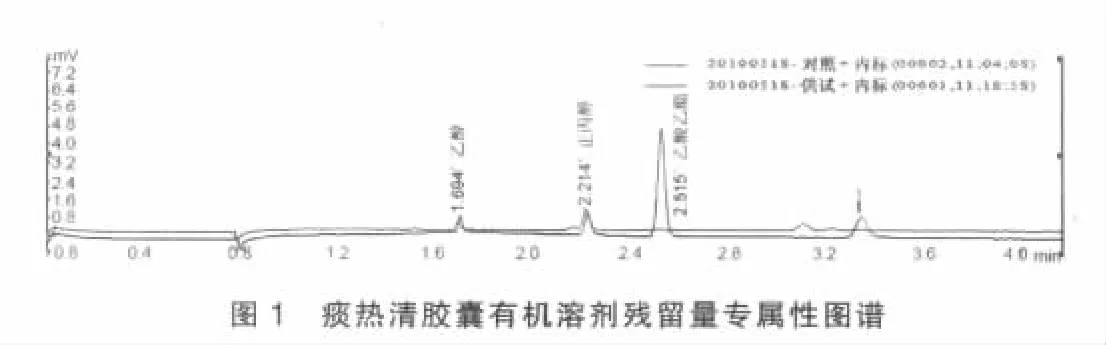
精密量取对照品溶液及供试品溶液各5 ml依法测定,记录色谱图(图1)。结果所采用方法能够满足痰热清胶囊有机溶剂检验要求。
2.6 线性
精密称取对照品贮备溶液,稀释制成每1 ml含内标物均为 0.5 mg、对照品分别为 0.10、0.25、0.50、1.00、2.50、1.00 mg系列浓度混合溶液,依法测定,以溶液中对照品的量C为横坐标,以峰面积A为纵坐标进行线性回归,乙醇回归方程为A=26.619 6+3 352.564 2C,r=0.999 8;乙酸乙酯回归方程为A=-2 962.843 6+46 107.968 6C,r=0.999 6;正丁醇 A=-86.139 7+1 1380.417 8C,r=1.000 0。
2.7 检测限及定量限
将对照品溶液进行逐步稀释,依法测定,结果0.01 mg/ml对照品溶液色谱图中S/N>3;0.05 mg/ml对照品溶液S/N>10。折合成对照品浓度,方法检测限为20 ng,定量限为50 ng。
2.8 精密度与稳定性
精密度:取对照品溶液连续测定6次,考察峰面积积分,结果RSD%分别为:乙醇1.54%,乙酸乙酯1.62%,正丁醇0.42%、正丙醇0.67%。
稳定性: 取对照品溶液于 0、1、2、3、4、5 h 分别取样测试,考察各组分峰面积积分,结果RSD%分别为:乙醇1.49%,乙酸乙酯为1.95%,正丁醇1.40%,正丙醇1.18%。
2.9 准确度
制成相当于样品中有机溶剂限度分别为80%、100%、120%的准确度试验用溶液,每个浓度各制备3份。依法测定,按内标法以峰面积计算回收率,结果:乙醇平均回收率为100.9%,RSD%为0.99%;乙酸乙酯平均回收率为99.1%,RSD%为0.92%;正丁醇平均回收率为99.9%,RSD%为1.15%。
3 样品测定结果
精密称取痰热清胶囊1.0 g,依法测定,按内标法以峰面积计算乙醇、乙酸乙酯、正丁醇含量,结果见表1。
4 讨论
本文进行了专属性、检测限、定量限、线性、精密度、溶液稳定性、准确度的研究,试验结果表明,在选定分析条件下,此方法能够满足痰热清胶囊有机溶剂残留量的测定。

表1 痰热清胶囊有机溶剂残留量测定结果(%)
用选定方法对产品有机溶剂残留量进行检查,结果显示该产品生产工艺相对稳定,其中乙醇因在胶囊剂制粒过程中使用残留量相对较多,约为0.4%,其他两种有机溶剂残留量均不超过0.1%,符合要求。
[1]国家食品药品监督管理局.国家药品标准[S].2009.
[2]化学药物残留溶剂研究的技术指导原则[D].http://www.cde.org.cn/zdyz.do?method=largePage&id=2064.
[3]鲁燕侠,刘祖德,沈丹,吴芳.毛细管气相色谱法测定左羟丙哌嗪中有机溶剂残留量[J].解放军药学学报,2010,26(3):241-243.
[4]陈荣宏,朱美容.头孢克洛有机溶剂残留量测定法[J].广东药学,2005,l5(3):21-23.
[5]孙启泉,施介华,刘燕,等.毛细管气相色谱法测定甲磺酸帕珠沙星中有机溶剂残留量[J].中国现代应用药学杂志,27,24(6):491-493.
[6]李辰,邸多隆,蒋生祥.顶空毛细管气相色谱法测定贞芪扶正胶囊中有机溶剂残留量[J].五邑大学学报(自然科学版),2010,24(2):3-9.
[7]国家药典委员会.中国药典[S].二部附录.2005:54-57.
Determination of residual organic solvents in tanreqing capsules by using headspace capillary gas chromatography
ZHANG Shanjie,YUE Suiyou(Henan Xin-Yi Pharmaceutical Co Ltd,Henan Province,Xinxiang 453731)
Objective:To develop an analysis of residual organic solvents for Tanreqing capsules.Methods:The content of residual organic solvents in Tanreqing capsules was determined by using the headspace capillary gas chromatography method involving the(6%)cyanopropyl-phenyl-(94%)dimethyl polysiloxane capillary column and the FID detector,and adopting the internal standard method.Results:The linear correlation coefficients were all more than 0.999 0,the repeata bility(RSD)was all less than 2.0%and the recovery rates accord with the requirements.Conclusion:The method is simple and rapid,the results are accurate and reproducible.
Tanreqing capsules;Headspace injection;Capillary gas chromatography;Residual organic solvents
R286.0
B
1674-4721(2010)11(c)-046-02
2010-09-29)
