鱼糜漂洗水中鱼蛋白的提取研究
2010-08-09杨金生丁迎燕夏松养
徐 律 杨金生 丁迎燕 夏松养
鱼糜制品是以鱼类为原料经采肉、漂洗、精滤、脱水、搅拌、成型、加热等工序加工而成的,营养价值高,深受消费者喜爱。鱼糜生产中,为了得到弹性好、色泽白的优质鱼糜,采肉后的碎鱼肉一般需进行漂洗。漂洗过程中一定量的水溶性蛋白质溶于水中,作为废水而废弃,十分可惜。鱼肉肉质鲜嫩美味,其中所含的必需氨基酸齐全,各种氨基酸组成合理,易被人体消化吸收利用,是一种优质蛋白质。从漂洗水中提取的蛋白,可作为蛋白源添加到食品中供人食用,也可以添加到饲料中,供各种动物养殖用,用途广泛。本文通过对鱼糜漂洗水中蛋白质的提取方法的研究,为科学利用废水鱼蛋白提供技术依据[1]。
1 实验材料、主要仪器与试剂
1.1 实验材料
原料(鱼糜漂洗水):鱼糜加工厂取样。
1.2 主要仪器、试剂
低速大容量离心机、冷冻离心机、氮蒸馏装置、pH计、冷冻干燥机、套式恒温器。三氯化铁、磷酸、明矾、乙酸。
2 实验方法
2.1 测定方法
水分的测定[2]按照GB;蛋白质含量的测定采用凯式定氮法;pH计测定pH值。
2.2 操作方法
2.2.1 等电点沉淀提取法[3-5]
2.2.1.1 工艺流程
原料→过滤处理(去渣)→调节滤液的pH值(用磷酸或乙酸)→pH值的测定→静置→去除上清液→干燥→称重
2.2.1.2 试剂的准备
将磷酸稀释到原来浓度的0.1%、0.2%、0.4%,乙酸稀释到原来浓度的0.2%、1.0%、4.0%,以上6种不同的酸溶液作为pH调节剂调节溶液的等电点。
①原料处理
用纱布(一层)对原液进行过滤,除去滤渣(滤渣可回收利用),使滤液看上去无明显的大颗粒悬浮物。
②滤液pH值的调节
准备 40 支试管,标号为 A1、A2…A19、A20,每支试管均加入 8.0 ml滤液。其中溶液 A1、A2…A9、A10以磷酸为pH调节剂,溶液A11、A12…A19、A20是以乙酸为pH调节剂。pH调节剂加入各试管中后,添加自然水,保证各试管溶液的体积达到10.0 ml。操作如下:
向 A1~A6分别加入 0.1% 磷酸 0、0.5、0.8、1.2、1.6、2.0 ml;向 A7~A9中分别加入 0.2% 磷酸 1.4、1.6、1.8 ml;向A10中加入0.4%磷酸1.2 ml,各加入滤液8 ml,并加水定容至10 ml。
向 A11~A14分别加入 0.2% 乙酸 0、0.2、1.0、1.8 ml;向 A15~A16中分别加入 1.0%乙酸 0.5、1.0 ml;向 A17~A20中加入 4.0%乙酸 0.8、1.0、1.2、2.0 ml;同时各加入滤液 8 ml,并加水定容至 10 ml。另取试管 B1、B2…B20,做平行试验,操作同上。
③pH值的测定
40份溶液配制完后,摇匀,快速用已调节好的pH计测得各溶液的pH值。
④离心干燥处理
溶液 A1~A20:静置 90 min,将 20份溶液分别倒入离心管内,在4 200 r/min下,离心15 min。除去上清液,在60℃下干燥约10 h,至恒重,称量。
溶液 B1~B20:静置 90 min后,产生分层现象,挑选出分层现象明显的试管,除去上清液,取絮状沉淀物在干燥皿中称量,在60℃的干燥箱内干燥约10 h,至恒重,称量。那些无明显分层现象产生的溶液,提取物质量记为0。
2.2.2 添加凝聚剂提取法[6-7]
2.2.2.1 工艺流程
原料→过滤处理(去渣)→添加凝聚剂→静置观察现象(混浊度)→去除上清液→干燥→称量
2.2.2.2 操作要点
①原料处理:用纱布对原液进行过滤,除去滤渣(回收利用),滤液中无明显的大颗粒悬浮物。
②凝聚剂的添加方法:向试管A21~A30中分别加入 0.1%三氯化铁 0、0.2、0.4、0.6、0.8、1.0、1.2、1.4、1.6、2.0 ml,各加入滤液 8.0 ml,用水定容至 10 ml。
向试管 A31~A40中分别加入 0.1%氯化铝 0、0.2、0.4、0.6、0.8、1.0、1.2、1.4、1.6、2.0 ml,各加入滤液 8.0 ml,用水定容至10 ml。
向试管 A41~A50中分别加入明矾 0、0.05、0.1、0.2、0.4、0.6、0.8、1.0、1.5、2.0mg,各加入滤液定容至 10.0 ml。
③离心干燥:分别把上述溶液摇匀静置,观察沉淀情况,当溶液有明显的絮状沉淀物产生时(约90 min),取出,去上清液,沉淀物置于干燥皿中,在60℃的烘箱内(约10 h)烘至恒重,称量。那些无明显分层现象产生的溶液,提取物质量记为0。
3 实验结果及讨论
3.1 原料的测定结果
经测定,原料(鱼糜漂洗液)中含蛋白质0.64%、水分98.70%;滤渣中蛋白质占15.4%、水分占82.30%;滤液中蛋白质含量为0.18%、水分99.74%。滤液及滤渣的固形物中蛋白质的纯度分别为:
P滤液=蛋白质(%)/[1-水分(%)]=[0.18%/(1-99.74%)]×100%=69.23%;
P滤渣=蛋白质(%)/[1-水分(%)]=[15.40%/(1-82.30%)]×100%=87.01%;
滤液的密度近似看成为1.0 g/ml。
可以看出滤渣中蛋白质的纯度竟达87.01%。滤液中仍含有较丰富的蛋白质,其干重可达0.18%,纯度也相当高,为69.23%,仍有很大的利用价值。
3.2 等电点沉淀法的结果及分析
3.2.1 溶液中蛋白质等电点的确定
经测定,室温下,溶液用磷酸为pH调节剂时:当pH值大于或等于6.28时,溶液基本保持原状,不出现混浊现象。pH值小于6.28时,溶液随着酸度的增加,溶液开始出现混浊现象了,溶液的混浊度先逐渐明显后又渐渐变小了;当pH值达5.28时,溶液混浊现象随酸度增加又开始消失。因此可以得出以下结论:滤液的等电点最接近管A5所配溶液,即pH值约为5.28。
以乙酸为调节剂的溶液A11~A20对应的pH值如表1所示。

表1 溶液A11~A20(B11~B20)对应的pH值(乙酸)
在室温下,滤液在使用乙酸调节pH值时,滤液的等电点接近于溶液A16的pH值,其值为5.35。
3.2.2 磷酸对提取效果的影响
①溶液在不同pH值下与离心后提取物质量之间的关系图:

图1 pH值与离心提取物质量关系
由图1可得:空白样本A1经过离心提取物的百分含量P1为55.56%。
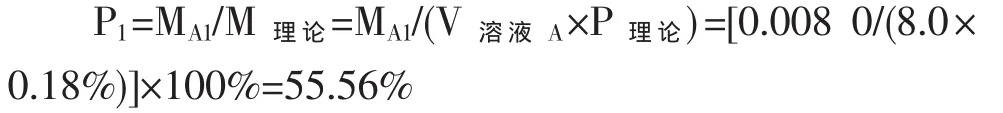
式中:MA1——溶液A1离心干燥提取的质量,同理MA5、MB1等;
V溶液A——滤液的实际加入体积;
P理论——滤液中蛋白质的理论百分含量。
当pH值为5.28时,即溶液在其蛋白质的等电点下,离心提取最多的量P2为90.28%。
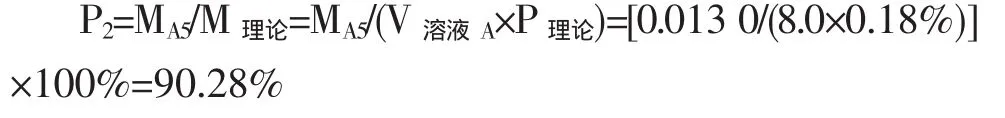
②产生明显分层现象后(静置约90 min),在溶液B1~B10中,选出分层的溶液,除去上清液,取絮状沉淀物干燥后的质量与对应的pH值,如图2可看出在pH值为5.28时,即在等电点下,其沉淀量达到最大,提取率P3为83.33%。

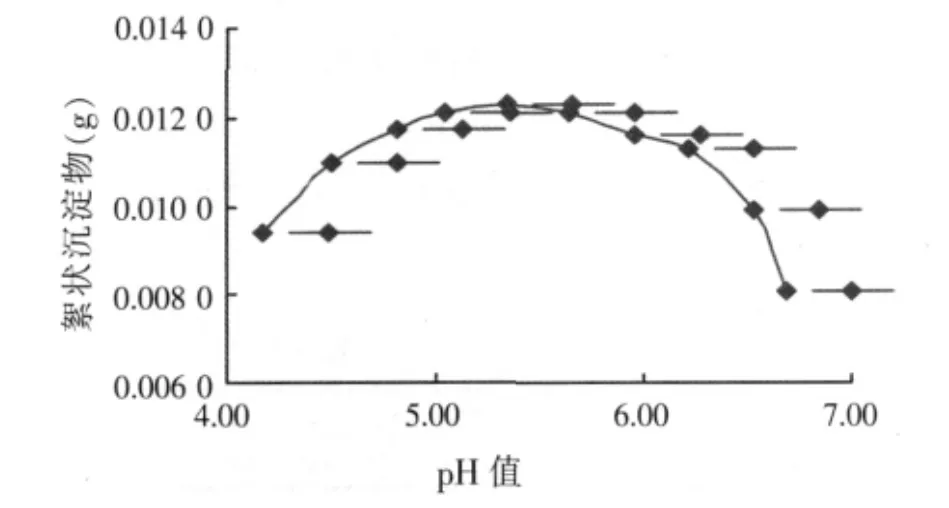
图2 絮状沉淀物的质量与pH值的关系
3.2.3 乙酸对提取效果的影响
①溶液A11~A20静置,离心,干燥,提取物质量与其对应的pH值之间的关系见图3。

图3 pH值与离心干燥质量的关系
由图3可得:
在pH值为6.69的情况时,空白式样A1,离心后蛋白质提取率P4为56.25%。

当pH值为5.35时,即等电点下,离心蛋白质提取率P5为85.41%。

②产生明显分层现象产生后(约100 min),在管B11~B20中,选出有分层现象的试管,去上清液,取絮状沉淀物干燥后所得质量与对应的pH值的关系,见图4。
由图4中可看出,当pH值为4.0~6.5之间,均有沉淀物出现,在其等电点下(pH值为5.35),其沉淀量达到最大。其提取率P6为79.86%。
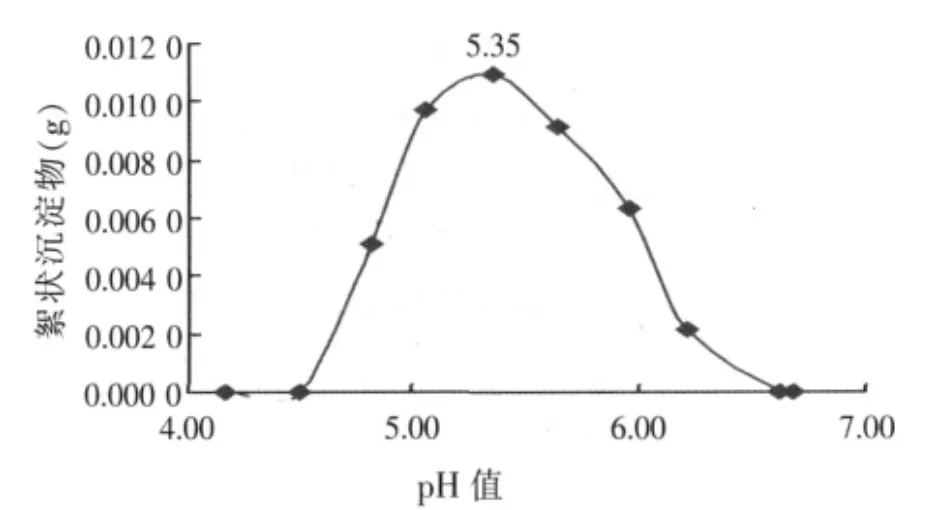
图4 沉淀物质量与pH值的关系

3.2.4 磷酸与乙酸对提取效果影响的对比分析
从提取率来看,磷酸的提取率略高于乙酸,并且在反应沉淀出的速率上来看,磷酸的效果优于乙酸。在提取物的质量上基本都能保证安全,新鲜。
从以上对比中可得,以磷酸作酸度调节剂更适合。
3.3 添加凝聚剂沉淀法的结果及分析
3.3.1 三氯化铁对提取效果的影响
以三氯化铁为凝聚剂,加入溶液A21~A30,在时间为0、30、80 min时溶液的混浊情况见表2。

表2 三氯化铁凝聚溶液的情况
从表2可看出,在一定范围内,刚开始的混浊度随着三氯化铁的加入量的增加而增加,当投入量达到一定量后渐趋于一个稳定数值。刚开始越混浊的溶液到最后也就越清晰,越清晰则说明沉淀得越完全。去除上清液,将絮状沉淀物干燥,所得的量与添加的三氯化铁的量的关系见图5。
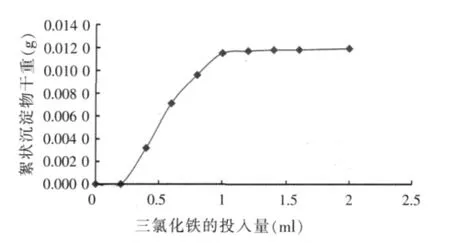
图5 三氯化铁的量与提取物的量的关系
从图5可看出,1.0 ml的1%的三氯化铁溶液于每8.0 ml溶液中,加1 ml水,即达接近最大值的提取率 P7为79.86%。

3.3.2 氯化铝对提取效果的影响
以氯化铝为凝聚剂,加入 A31~A40溶液,经 0、30、80 min,溶液的混浊情况见表3。
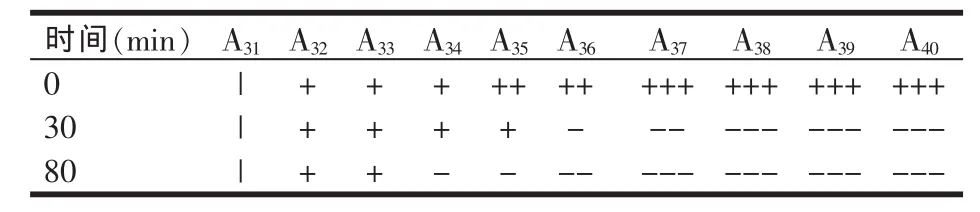
表3 氯化铝凝聚溶液的混浊情况
从表3中可知,其混浊与澄清趋势基本与添加三氯化铁溶液的变化趋势相同。
氯化铝的量与提取物质量的关系见图6。

图6 氯化铝的量与提取物质量的关系
如图6可得1%的氯化铝溶液为1.2 ml于8.0 ml滤液中,加0.8 ml水,其提取率P8为77.78%。
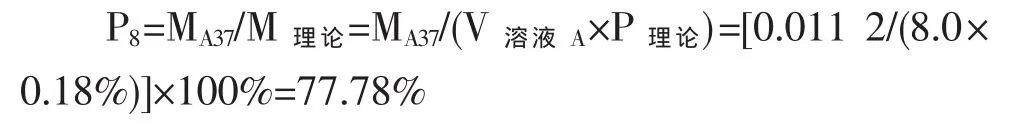
3.3.3 明矾对提取效果的影响
溶液A41~A50是以明矾作为凝聚剂,经0、30、80 min,溶液的混浊情况见表4。

表4 明矾作凝聚剂时溶液的混浊情况
从表4中可看出,其混浊度与澄清趋势与三氯化铁和氯化铝的变化趋势基本相同。
将上清液去除,絮状沉淀物直接进行干燥,其量与沉淀物质量的关系如图7。
如图7可见,明矾投入量为1.0mg时,沉淀物P9得率基本趋于最大,P9为75.69%。

图7 明矾加入量与沉淀物质量的关系

3.3.4 使用各种凝聚剂的对比分析
以上三种凝聚剂,在其一定范围内,沉淀物的质量都随着凝聚剂投入量的增加而增加,当投放量达到一定数值后,可沉淀出的物质基本趋于饱和。在最适点下提取率的高低顺序为:三氯化铁>氯化铝>明矾。
4 小结
由实验可知,鱼糜漂洗液中蛋白质的最适提取方法为等电点提取法,其提取条件在室温下,以0.1%磷酸调节pH值,所加体积比为:V溶液:V磷酸=5:1,静置时间约1 h,适当延长静置时间,沉淀效果更好,沉淀物中水分含量越少。
此方法操作简单,提取率高,提取影响因素小,成本低,适合于大量的生产。
[1]王天林.酶法水解草鱼鱼肉蛋白最适条件的研究[J].哈尔滨市食品药品监督管理局,2009(8).
[2]殷学锋.新编大学化学实验[M].北京:高等教育出版社,2002.
[3]韩喜平.测定纯水pH值方法的改进[J].浙江预防医学,2006(03).
[4]刘迎祥,张向京,许建成.从制药厂废醪中回收蛋白质[J].化工环保,2000(02).
[5]Onodenalore A C,Shahidi F.Protein dispersions and hydrolysates from shark (Isurus oxyrinchus)[J].Aquat.Food Prod.Technol.,1996(5):43-59.
[6]周利平.菜籽蛋白水溶液的超滤行为及在线控制膜污染的研究[J].食品与机械,2006(01).
[7]Abdul2Hamid A,Bakar J,Bee G H.Nutritional quality of spray dried protein rolysate from Black Tilapia (Oreochromis mossambicus)[J].Food Chem.,2002(78):69-74.
