注射用头孢唑肟钠与阿昔洛韦的配伍稳定性考察
2010-07-19陈阳建
陈阳建
浙江医药高等专科学校(315100)
头孢唑肟钠(Ceftizoxime Sodium)为半合成的第3代头孢菌素,具有广谱抗菌作,对多种革兰阳性菌和革兰阴性菌产生的广谱β-内酰胺酶(包括青霉素酶和头孢菌素酶)稳定,其临床应用广泛。阿昔洛韦(acyclovir) 为一临床使用频率较高的广谱抗病毒药,主用于治疗单纯疱疹病毒Ⅰ、Ⅱ型感染和带状疱疹病毒感染。临床上有时将两药配伍用于治疗病毒和细菌的混合型感染,但尚未见有两药配伍稳定性的相关报道。为给临床合理用药提供参考,本文参照临床使用剂量,对两药0.9%氯化钠注射液中的配伍稳定性进行了考察。
1 仪器与试剂
1.1 仪器
UV-2401PC紫外-可见分光光度计(日本岛津);pHS-3C型精密pH计(上海雷磁仪器厂);HH-420恒温水浴箱(上海比朗仪器有限公司);ZWF-J6激光注射液微粒分析仪(天津天河医疗仪器有限公司);BS110S 型分析天平(东莞万兴电子厂)。
1.2 试剂
注射用头孢唑肟钠(哈药集团制药总厂,批号为B20081007,规格为0.5g/瓶);头孢唑肟钠对照品(中国药品生物制品检定所,批号0484-9901);注射用阿昔洛韦(武汉普生制药有限公司,批号080515,规格:250mg/瓶);阿昔洛韦对照品(中国药品生物制品检定所,批号140630-200602);0.9%氯化钠注射液(石家庄四药有限公司,批号070201601,规格:250mL)。
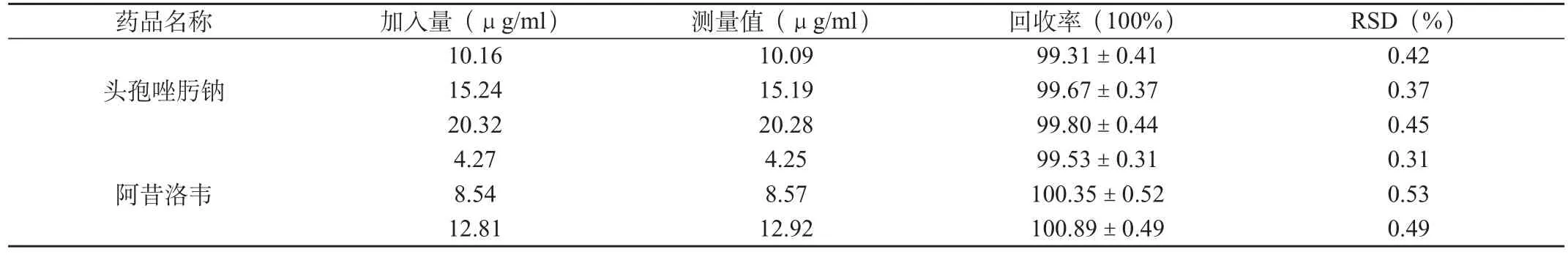
表1 头孢唑肟钠和阿昔洛韦的回收率(n=5)
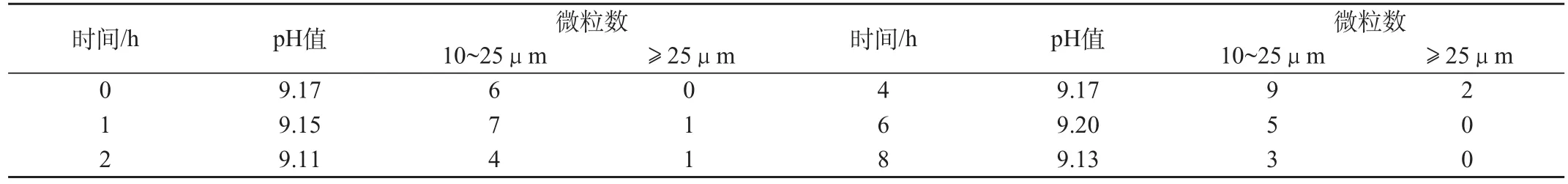
表2 不同时刻配伍液(1mL)的pH值和不溶性微粒数
2 方法与结果
2.1 测定波长的选择
分别以纯化水配制浓度为10μg/mL的头孢唑肟钠溶液和10μg/mL的阿昔洛韦溶液以及二者的混合溶液,以纯化水为空白,于200~400nm的波长范围内扫描,其紫外扫描图谱如图1所示,头孢唑肟钠和阿昔洛韦分别在234.2、252.6nm处有最大吸收,与文献报道基本一致[1,2],二者混合溶液的最大吸收波长在252nm左右。由图1可知,两种药物的紫外吸收在最大波长处有重叠,相互干扰较大,故选用双波长-等吸收消除法作为含量测定方法。头孢唑肟钠的测定波长为234.2nm,参比波长为287.5nm;阿昔洛韦的测定波长为252.6nm,参比波长为218.0nm。
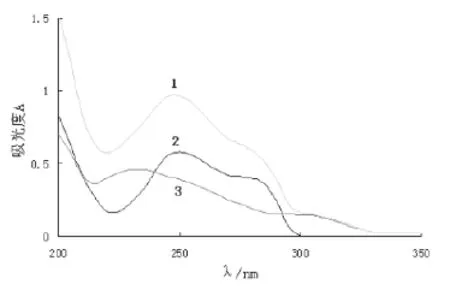
图1 紫外吸收光谱图(1.头孢唑肟钠+阿昔洛韦;2.阿昔洛韦;3.头孢唑肟钠)
2.2 标准曲线的绘制
精密称取头孢唑肟钠对照品40.0mg和阿昔洛韦对照品25.0mg分别置100mL容量瓶中,以纯化水溶解并稀释至刻度得浓度为400μg/mL的头孢唑肟钠溶液和浓度为250μg/mL的阿昔洛韦溶液。分别精密量取两种对照品溶液各1.0、2.0、3.0、4.0、5.0、6.0mL置100mL量瓶中,用纯化水稀释至刻度,摇匀,得浓度梯度为4.0~24.0μg/mL的系列头孢唑肟钠标准溶液和浓度梯度为2.5~15.0μg/mL的系列阿昔洛韦标准溶液。以纯化水为空白,在234.2和287.5nm波长处测定头孢唑肟钠溶液的吸光度值,计算二者吸光度的差值(ΔA=A234.2-A287.5),以ΔA对浓度C进行回归,得线性回归方程为C=32.57ΔA+0.049(r=0.9996,n=6,线性范围为4.0~24.0μg/ml);在252.6nm和218.0nm波长处测定阿昔洛韦溶液的吸光度值,计算二者吸光度的差值(ΔA=A252.6-A218.0),以ΔA对浓度C进行回归,得线性回归方程为C=25.85ΔA+0.036(r=0.9996,n=6,线性范围为2.5~15.0μg/mL)。
2.3 回收率试验
精密称取头孢唑肟钠和阿昔洛韦对照品各适量,用纯化水配成高、中、低3个质量浓度的头孢唑肟钠和阿昔洛韦的混合溶液;按照“2.2”项下操作测定吸光度值,所得数据代入回归方程并计算回收率,结果见表1。
2.4 精密度试验
精密量取头孢唑肟钠溶液和阿昔洛韦溶液适量,用纯化水配制成含头孢唑肟钠和阿昔洛韦分别为5.0、5.0μg/mL,10.0、7.5μg/mL,15.0、10.0μg/mL的混合液;按照“2.2”项下操作测定吸光度值,每种混合液分别测定5次,将所得数据代入回归方程后计算相对标准偏差(RSD)。浓度为5.0、5.0μg/mL的混合液:头孢唑肟钠RSD为0.79%(n=5),阿昔洛韦RSD为0.51%(n=5);浓度为10.0、7.5μg/mL的混合液:头孢唑肟钠RSD为0.67%(n=5),阿昔洛韦RSD为0.34%(n=5);浓度为15.0、10.0μg/mL的混合液:头孢唑肟钠RSD为0.38%(n=5),阿昔洛韦RSD为0.29%(n=5)。结果显示该方法进行含量测定,精密度较高,方法可行。
2.5 重复性试验
精密量取头孢唑肟钠溶液和阿昔洛韦溶液适量,平行配制头孢唑肟钠和阿昔洛韦浓度分别为7.5和15.0μg/mL的混合液5份;按照“2.2”项下操作测定吸光度值,将所得数据代入回归方程后计算二者的浓度,头孢唑肟钠RSD为0.41%(n=5),阿昔洛韦RSD为0.27%(n=5)。结果表明该测定方法误差较小,重复性较好。
2.6 配伍液稳定性考察
2.6.1 配伍液的制备
模拟临床用药浓度,取100mL容量瓶,加入注射用头孢唑肟钠和注射用阿昔洛韦各0.2g,用0.9%氯化钠注射液溶解、定容得到二者的配伍液。将配伍液于25℃条件下放置,并用0.9%氯化钠注射液配制等浓度的头孢唑肟钠和阿昔洛韦溶液作为对照液。
2.6.2 配伍液外观、pH值和微粒数变化
分别于0、1、2、4、6、8h观察配伍液在25℃条件下的外观、pH值并测定不溶性微粒数。头孢唑肟钠对照液和阿昔洛韦对照液均为无色澄明,其pH值分别为(6.59±0.07)和(11.02±0.03)。配伍液在8h内均呈微黄色澄明,颜色无明显变化,也无沉淀、结晶、气体产生;在各时刻测得的pH值和不溶性微粒数量见表2。
2.6.3 配伍液中的含量测定
分别于0、1、2、4、6、8h精密量取配伍液适量,用纯化水稀释至200倍,按照“2.2”项下操作测定吸光度值,所得数据代入回归方程后计算药品含量,并以0h时的测量值为标示量100%,再计算各时刻两种药品的百分含量,结果如表3所示。
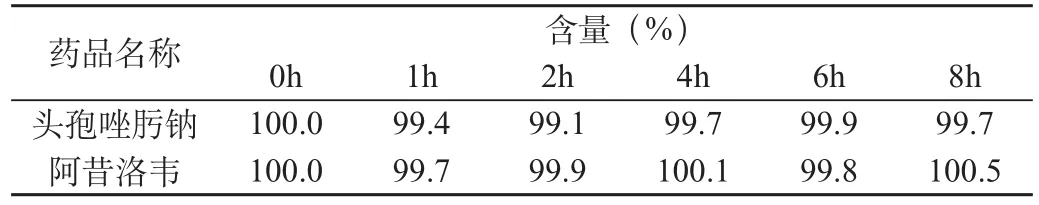
表3 配伍液中头孢唑肟钠与阿昔洛韦含量的变化情况
2.6.4 配伍液吸收曲线变化
以0.9 %氯化钠注射液为空白对照,对稀释后的配伍液在200~400nm范围扫描,在不同时间内配伍液的吸收曲线如吸收峰的峰形、峰位均无明显变化。
3 讨 论
阿昔洛韦是目前国内外广泛使用的具有高度选择性和较低毒性的抗病毒药物,在临床应用中经常将其与抗菌药联合用于治疗细菌和病毒的混合感染,已有很多文献报道阿昔洛韦与某些抗菌药的配伍稳定性研究[3],而头孢唑肟钠与阿昔洛韦的配伍稳定性尚未见报道,故本文研究二者的配伍稳定性问题,为临床用药提供参考。
头孢唑肟钠与阿昔洛韦的紫外吸收光谱有重叠,在含量测定时相互干扰较大,故选用双波长-等吸收消除法以消除干扰,该方法操作简单且样品无需处理。实验是模拟临床用药量进行配伍的,结果表明在25℃条件下,注射用头孢唑肟钠与阿昔洛韦配伍液在8h内外观、pH值及二者的含量均无显著变化,且紫外吸收曲线也没有明显变化,故注射用头孢唑肟钠与阿昔洛韦可以在临床上配伍。
[1] 陶玲玲,朱建国,金卫坤.头孢唑肟钠与三种常用输注配伍的稳定性考察[J].苏州医学院学报,1999,19(9): 1002-1003.
[2] 张碧玫,李娟.阿昔洛韦与3种注射液配伍稳定性试验[J].中国医院药学杂志,2005,25(4): 373-374.
[3] 闫双银,蒋瑾,杨琳.注射用阿昔洛韦的配伍稳定性研究进展[J].中国药业,2007,16(13):59-60.
