HBsAg阳性母亲其婴幼儿联合阻断后无/低应答状态及加强免疫效果
2010-07-16曾慧慧杨洪玲
曾慧慧,何 明,杨洪玲,闫 杰,庞 琳
1 资料与方法
1.1 一般资料 2004年 8月—2006年 12月于我院出生、母亲 HBsAg阳性的婴幼儿共 249例,其中男 129例,女 120例。跟踪随访婴幼儿,了解全程乙肝疫苗免疫接种后 (出生 7个月后)其应答状态,对其中无 HBV携带的无应答和低应答儿童,及时给予乙肝疫苗加强免疫,并不再计入下一年龄段的观察范围,同时剔除失访儿童及 HBV携带儿童。实际观察例数:7~11个月时为 249例,12~23个月时为120例,24~35个月时为 27例, ≥36个月时为 7例。随机选择全程免疫结束后无HBV携带的无/低应答幼儿共 50例进行乙肝疫苗加强免疫接种,其中男 26例,女 24例,年龄 7~26个月,平均 13.56个月。
1.2 方法 所有新生儿出生后按统一方案进行联合免疫阻断,生后 24 h内同时接种人乙型肝炎免疫球蛋白 (HBIG)200 U及乙肝疫苗 10μg各 1次,生后 30 d予HBIG 200 U(第 2次 ),按 0.1.6方案完成全程乙肝疫苗接种。跟踪随访婴幼儿,取其生后 7个月、12个月、24个月、36个月时的外周静脉血标本,送至本院免疫实验室采用发光免疫法检测乙肝五项表面抗原,总结全程免疫接种后的 7~11个月幼儿的应答状态,总结无 HBV携带的高应答幼儿在其后不同年龄阶段无应答和低应答的发生率。
随机选择全程免疫结束后无 HBV携带的无应答和低应答幼儿 50例,予以加强接种乙肝疫苗 10μg 1次,1个月后复查 HBsAb。应答状态标准:无应答 HB-sAb<10 mU/ml,低应答 10~100 mU/ml,高应答 >100 mU/ml。
1.3 统计学方法 采用 SPSS 13.0统计软件,对计数资料用百分率进行描述,对计量资料用均数及标准差进行描述;对组间差异进行配对 t检验和 χ2检验,以 P<0.05为差异有统计学意义。
2 结果
2.1 HBsAg阳性母亲其婴幼儿全程乙肝疫苗接种后 (出生后 7~11个月)的应答状态 249例幼儿在全程乙肝疫苗接种后出现无应答者 20例 (8.03%),低应答者 38例 (15.26%),高应答者 191例(76.71%),无应答及低应答的发生率为23.29%(58/249),其中 27.59%(16/58)为 HBV携带儿,72.41%(42/58)为无 HBV携带的婴幼儿。
2.2 全程乙肝疫苗接种后无 HBV携带的高应答儿在不同年龄段无应答及低应答的发生率 对无 HBV携带的高应答儿继续观察,120例高应答儿在 12~23个月间出现无应答或低应答者 45例,无应答及低应答的发生率为 37.50%;27例持续高应答儿在 24~35个月间出现无应答及低应答者 13例,无应答及低应答的发生率为 48.14%;7例在 36个月前持续高应答的幼儿在 36个月后有 3例出现无应答及低应答 (见表 1)。
2.3 无应答和低应答儿乙肝疫苗加强免疫接种后的应答状态 50例无应答和低应答儿乙肝疫苗加强免疫接种后 1个月,有 47例 (94%)呈高应答状态 (见表2)。
2.4 无应答及低应答儿乙肝疫苗加强免疫前后 HBsAb水平变化 干预前幼儿的HBsAb水平低于干预后的水平,差异有统计学意义 (P<0.05,见表3)。
2.5 性别和干预年龄对加强免疫后 HbsAb水平的影响 干预后对不同年龄及性别的幼儿的 HBsAb水平进行比较,发现男女幼儿 HBsAb水平间差异无统计学意义 (P>0.05),不同干预年龄儿的 HB-sAb水平间差异亦无统计学意义 (P>0.05)。

表 1 全程乙肝疫苗接种后无 HBV携带的高应答儿在不同年龄段无应答及低应答的发生率 〔n(%)〕Table 1 The non-response and low-respons incidence in high response HBV free infants vaccinated by hepatitis B at different ages
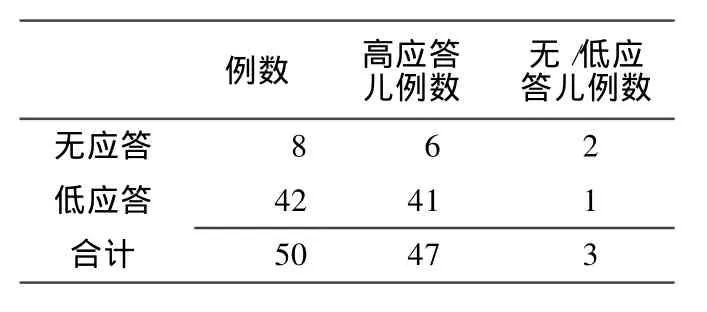
表 2 无应答和低应答儿乙肝疫苗加强免疫接种后的应答状态Table 2 The immune response status of no-response and low-response infants after booster doses hepatitis B vaccine
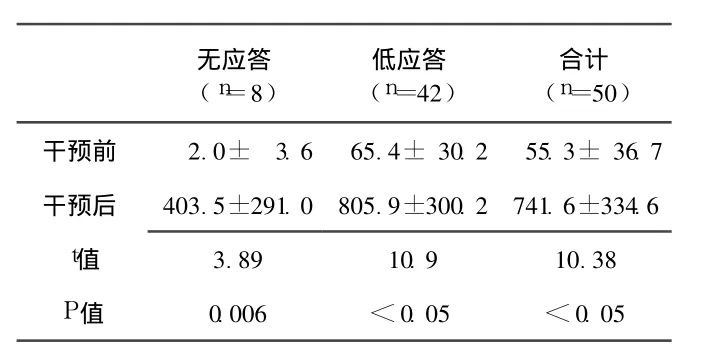
表 3 无应答及低应答儿干预前后 HBsAb水平比较(x±s)Table 3 The level of HBsAb in non-response and low response infants before and after intervention
3 讨论
目前,HBsAg阳性母亲其新生儿出生后联合免疫会取得高达 92%~96%的母婴阻断效果[2]。对阻断成功无 HBV感染的婴幼儿而言,为减少生后感染的风险,全程接种乙肝疫苗后生成足够的保护性抗体 HBsAb很重要。了解婴幼儿接种乙肝疫苗后无应答和低应答的发生率,了解乙肝疫苗加强免疫干预的效果,具有较为实用的临床意义。
既往有不少研究对乙肝疫苗接种后HBsAb的变化进行了观察总结。John等[3]认为乙肝疫苗接种后对成人的保护力可以高达 12年以上;Hassan等[4]对3 752位 6岁儿童进行分析发现 19.3%的儿童 HBsAb水平 <10 mU/mL,只有29.2%的儿童 >100 mU/mL;Ribeiro等[5]对进行全程免疫的婴幼儿随访 3年发现,7.92%的儿童无应答,50.5%低应答,41.58%高应答。本研究结果表明,经全程乙肝疫苗接种后,部分儿童存在无应答或低应答状态,而高应答儿在生后36个月后也可能转变为无应答或低应答状态。7~11个月的幼儿无应答和低应答的发生率为 23.29%;7~11个月时呈高应答的幼儿,12~23个月时无应答和低应答的发生率为 37.50%;12~23个月时持续呈高应答的幼儿,24~35个月时无应答和低应答的发生率为 48.14%,该结果提示临床上要重视对婴幼儿保护性抗体HBsAb水平的监测。
对乙肝疫苗全程免疫后无应答或低应答儿进行积极主动的干预,提高保护性抗体 HBsAb水平,是减少生后感染 HBV的有效措施之一。Chen[6]认为充分有效地发挥乙肝疫苗的作用,加强免疫非常必要。Bialek等[7]对生后全程免疫后的婴幼儿于生后第 15年进行研究发现,大部分儿童需要加强免疫接种,加强免疫后,47.9%的接种对象产生免疫记忆应答,其中 17.7%为低应答,30.2%为高应答。本研究对 50例低应答和无应答儿进行乙肝疫苗加强免疫接种,94%的儿童出现了高应答,加强免疫后其 HBsAb水平显著提高。本研究发现,加强免疫接种对干预前为低应答的幼儿的效果要好于无应答的幼儿,但由于观察的例数不多,结果供参考,有待扩大样本量进一步证实。本研究还发现性别、加强免疫时的年龄对加强免疫的效果无影响。
本研究观察到有 3例幼儿经加强免疫后,HBsAb水平仍处于低应答或无应答状态,跟踪随访这 3例幼儿的 HBsAb水平,发现单次及全程加强免疫均不能激发良好免疫记忆,再次加强免疫亦无效。其中有1位幼儿其父亲对乙肝疫苗亦反复呈无应答状态。Sjogren[8]认为,造成无应答或低应答状态的原因与基因倾向、免疫抑制及某些慢性疾病有关。了解有家族遗传倾向的无应答状态,并对其特异性的基因特点进行总结分析是必要的。Rubin等[9]认为监测乙肝疫苗应答效果具有重大的医疗和社会经济效益。乙肝疫苗免疫后 HB-sAg阳性母亲其婴幼儿的 HBsAb水平是动态变化的。无应答及低应答儿的客观存在,提示临床上需积极监测其 HBsAb水平。对无应答或低应答儿应给予乙肝疫苗加强免疫接种,将其 HBsAb维持在较高水平,以最大限度地降低 HBsAg阳性母亲的婴幼儿出生后感染 HBV的风险。
1 Mansoor OD,Salama P.Should hepatitis B vaccine be used for infants?[J].Expert Rev Vaccines,2007,6(1):29-33.
2 Kabir A,Alavian SM,Ahanchi N,et al.Combined passive and active immunoprophylaxis for preventing perinatal transmission of the hepatitis B virus in infants born to HBsAg positive mothers in comparison with vaccine alone[J].Hepatol Res,2006,36(4):265-271.
3 John TJ,Cooksley G.Hepatitis B vaccine boosters:is there a clinical need in high endemicity populations?[J].J Gastroenterol Hepatol,2005,20:5-10.
4 Hassan S,Ziba F.Antibody titer in Iranian children 6 years after hepatitis B vaccine administration[J].Vaccine,2007,25(17):3511-3514.
5 Ribeiro TM,Azevedo RS.Seroconversion of hepatitis B vaccine in infants related to the mother's serostatus in a community of Sao José dos Campos,state of So Paulo[J].Brazil Clinics,2006,61(5):387-394.
6 Chen DS.Hepatitis B vaccination:the key towards elimination and eradication of hepatitis B[J].J Hepatol,2009,50(4):805-816.
7 Bialek SR,Bower WA.Persistence of protection against hepatitis B virus infection among adolescents vaccinated with recombinant hepatitis B vaccine beginning at birth:a 15-year follow-up study[J].Pediatr Infect Dis J,2008,27(10):881-885.
8 Sjogren MH.Prevention of hepatitis B in nonresponders to initial hepatitis B virus vaccination[J].Am J Med,2005,118(Suppl 10A):34-39.
9 Rubin L,Hefer E,Dubnov Y,et al.An evaluation of the efficacy of thenational immunization programme for hepatitis[J].Public Health,2007,121(7):529-533.
